ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್
| Lung cancer | |
|---|---|
| Classification and external resources | |
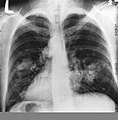
 Cross section of a human lung. The white area in the upper lobe is cancer; the black areas are discoloration due to smoking. | |
| ICD-10 | C33-C34 |
| ICD-9 | 162 |
| DiseasesDB | 7616 |
| MedlinePlus | 007194 |
| eMedicine | med/1333 med/1336 emerg/335 radio/807 radio/405 radio/406 |
| MeSH | D002283 |
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಎಂಬುದು ಒಂದು ಕಾಯಿಲೆಯಾಗಿದ್ದು, ಶ್ವಾಸಕೋಶದ ಅಂಗಾಂಶಗಳಲ್ಲಿನ ಅನಿಯಂತ್ರಿತವಾದ ಜೀವಕೋಶದ ಬೆಳವಣಿಗೆಯನ್ನು ಇದು ಒಳಗೊಂಡಿರುತ್ತದೆ. ಈ ಬೆಳವಣಿಗೆಯು ಸ್ಥಾನಾಂತರಣಕ್ಕೆ ಕಾರಣವಾಗಬಹುದು; ಅಂದರೆ ಇದು ಪಕ್ಕದ ಅಂಗಾಂಶದ ಮೇಲೆ ಆಕ್ರಮಣ ಮಾಡಬಹುದು ಮತ್ತು ಶ್ವಾಸಕೋಶಗಳಿಂದ ಆಚೆಗಿನ ಭಾಗಗಳಲ್ಲಿನ ಒಳವ್ಯಾಪಿಸುವಿಕೆಗೆ ಕಾರಣವಾಗಬಹುದು. ಶ್ವಾಸಕೋಶದ ಪ್ರಧಾನ ಕ್ಯಾನ್ಸರ್ಗಳ ಪೈಕಿಯ ಬಹುಪಾಲು ನಿದರ್ಶನಗಳು ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮಗಳಾಗಿದ್ದು , ಹೊರಪದರದ ಜೀವಕೋಶಗಳಿಂದ ಅವು ಜನ್ಯವಾದವುಗಳಾಗಿರುತ್ತವೆ. ಪುರುಷರು ಮತ್ತು ಮಹಿಳೆಯರಲ್ಲಿ ಕಂಡುಬರುವ ಕ್ಯಾನ್ಸರ್-ಸಂಬಂಧಿತ ಸಾವುಗಳಿಗೆ ಅತ್ಯಂತ ಸಾಮಾನ್ಯ ಕಾರಣವಾಗಿರುವ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್, ವಿಶ್ವಾದ್ಯಂತ ಕಂಡುಬರುವ 1.3 ದಶಲಕ್ಷ ಸಾವುಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಹೊಣೆಗಾರನಾಗಿದೆ. ಈ ಅಂಕಿ-ಅಂಶವು 2004ರ ವೇಳೆಗೆ ಇದ್ದಂತೆ ವಾರ್ಷಿಕವಾಗಿ ಕಂಡುಬಂದ ಸಂಖ್ಯೆಯಾಗಿದೆ.[೧] ಉಸಿರಾಟದಲ್ಲಿ ಕಂಡುಬರುವ ಅಲ್ಪತೆ, ಕೆಮ್ಮುವಿಕೆ (ಕೆಮ್ಮಿದಾಗ ರಕ್ತವು ಹೊರಬರುವುದೂ ಸೇರಿದಂತೆ) ಮತ್ತು ತೂಕನಷ್ಟ ಇವುಗಳು ಅತ್ಯಂತ ಸಾಮಾನ್ಯ ರೋಗಲಕ್ಷಣಗಳಾಗಿವೆ.[೨]
ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ ಮತ್ತು ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ - ಇವು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಮುಖ್ಯ ಬಗೆಗಳಾಗಿವೆ. ಕ್ಯಾನ್ಸರ್ನ ಬಗೆಯ ಅನುಸಾರ ಚಿಕಿತ್ಸೆಯು ಬದಲಾಗುವುದರಿಂದ ಈ ವೈಲಕ್ಷಣ್ಯವು ಪ್ರಮುಖವಾಗಿರುತ್ತದೆ; ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವನ್ನು (ನಾನ್-ಸ್ಮಾಲ್ ಸೆಲ್ ಲಂಗ್ ಕಾರ್ಸಿನೋಮ-NSCLC) ಶಸ್ತ್ರಚಿಕಿತ್ಸೆ ಮಾಡಿ ಕೆಲವೊಮ್ಮೆ ಉಪಚರಿಸಲಾದರೆ, ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವು (ಸ್ಮಾಲ್-ಸೆಲ್ ಲಂಗ್ ಕಾರ್ಸಿನೋಮ-SCLC) ಸಾಮಾನ್ಯವಾಗಿ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ ಮತ್ತು ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಗೆ ಉತ್ತಮವಾಗಿ ಪ್ರತಿಸ್ಪಂದಿಸುತ್ತದೆ.[೩] ತಂಬಾಕು ಹೊಗೆಗೆ ದೀರ್ಘಾವಧಿಗೆ ಒಡ್ಡಿಕೊಳ್ಳುವುದು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಅತ್ಯಂತ ಸಾಮಾನ್ಯ ಕಾರಣವಾಗಿದೆ.[೪] ಧೂಮಪಾನಿಗಳಲ್ಲದವರು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಈಡಾಗುವ ಪ್ರಮಾಣವು ಒಟ್ಟು ಪ್ರಕರಣಗಳ[೫] ಪೈಕಿ ಸುಮಾರು 15%ನಷ್ಟಿದ್ದು, ಇದಕ್ಕೆ ಅನೇಕ ಕಾರಣಗಳಿರಲು ಸಾಧ್ಯವಿದೆ; ಆನುವಂಶಿಕ ಅಂಶಗಳು,[೬][೭] ರೇಡಾನ್ ಅನಿಲ,[೮] ಕಲ್ನಾರು,[೯] ಮತ್ತು ಅನ್ಯಮೂಲದ ಹೊಗೆಯನ್ನು ಒಳಗೊಂಡಿರುವ ವಾಯುಮಾಲಿನ್ಯ[೧೦][೧೧][೧೨] ಇವುಗಳ ಒಂದು ಸಂಯೋಜನೆಯು ಧೂಮಪಾನಿಗಳಲ್ಲದವರಲ್ಲಿ ಕಂಡುಬರುವ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಅನೇಕವೇಳೆ ಕಾರಣವಾಗುತ್ತದೆ.[೧೩][೧೪]
ಎದೆಯ ರೇಡಿಯೋಗ್ರಾಫ್ ಮತ್ತು ಕಂಪ್ಯೂಟರ್ ಬಳಸಿ ಮಾಡಲಾದ ತಲಲೇಖನದ (ಕಂಪ್ಯೂಟರ್ ಟೋಮೋಗ್ರಫಿ) (CT ಕ್ಷಿಪ್ರಬಿಂಬ) ವಿಧಾನಗಳನ್ನು ಬಳಸಿಕೊಂಡು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಕಾಣಲು ಸಾಧ್ಯವಿದೆ. ಅಂಗಾಂಶ ಪರೀಕ್ಷೆಯೊಂದನ್ನು ಕೈಗೊಳ್ಳುವ ಮೂಲಕ ರೋಗನಿರ್ಣಯವನ್ನು ದೃಢೀಕರಿಸಲಾಗುತ್ತದೆ. ಬ್ರಾಂಕೋಸ್ಕೋಪಿ ಅಥವಾ CT-ನಿರ್ದೇಶಿತ ಅಂಗಾಂಶ ಪರೀಕ್ಷೆಯಿಂದ ಇದನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ನಿರ್ವಹಿಸಲಾಗುತ್ತದೆ. ಕ್ಯಾನ್ಸರ್ನ ಊತಕಶಾಸ್ತ್ರೀಯ ಬಗೆ, ಹಂತ (ಹರಡಿಕೆಯ ಮಟ್ಟ), ಮತ್ತು ರೋಗಿಯ ಕಾರ್ಯಕ್ಷಮತೆಯ ಸ್ಥಿತಿಯ ಮೇಲೆ ಚಿಕಿತ್ಸೆ ಮತ್ತು ಕಾಯಿಲೆಯ ಮುನ್ನರಿವು ಅವಲಂಬಿತವಾಗಿರುತ್ತವೆ. ಸಂಭಾವ್ಯ ಚಿಕಿತ್ಸೆಗಳಲ್ಲಿ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆ, ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ, ಮತ್ತು ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಗಳು ಸೇರಿವೆ. ಕಾಯಿಲೆಯ ಹಂತ, ಒಟ್ಟಾರೆ ಆರೋಗ್ಯ, ಮತ್ತು ಇತರ ಅಂಶಗಳನ್ನು ಅವಲಂಬಿಸಿ ರೋಗಿಯ ಬದುಕುಳಿಯುವಿಕೆಯು ಬದಲಾಗುತ್ತದೆಯಾದರೂ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಕಾಯಿಲೆಯಿರುವುದು ಪತ್ತೆಯಾದ ಎಲ್ಲಾ ವ್ಯಕ್ತಿಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತಿರುವ ಒಟ್ಟಾರೆ ಐದು-ವರ್ಷಗಳ ಬದುಕುಳಿಯುವಿಕೆಯ ಪ್ರಮಾಣವು 14%ನಷ್ಟಿದೆ ಎನ್ನಬಹುದು.[೨]
ವರ್ಗೀಕರಣ
[ಬದಲಾಯಿಸಿ]ಊತಕಶಾಸ್ತ್ರೀಯ ಬಗೆಯ ಅನುಸಾರವಾಗಿ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳನ್ನು ವರ್ಗೀಕರಿಸಲಾಗಿದೆ. ಕಾಯಿಲೆಯ ನೈದಾನಿಕ ನಿರ್ವಹಣೆ ಮತ್ತು ಮುನ್ನರಿವಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ, ಈ ವರ್ಗೀಕರಣವು ಪ್ರಮುಖ ಸೂಚಿತ ಪರಿಣಾಮಗಳನ್ನು ಹೊಂದಿದೆ. ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಬಹುಪಾಲು ನಿದರ್ಶನಗಳು ಕಾರ್ಸಿನೋಮಗಳಾಗಿದ್ದು, ಇವು ಹೊರಪದರದ ಜೀವಕೋಶಗಳಿಂದ ಉದ್ಭವಿಸುವ ವಿಷಮತೆಗಳಾಗಿವೆ. ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶ ದ ಮತ್ತು ಸಣ್ಣ-ಜೀವಕೋಶ ದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮಗಳೆಂಬ ಎರಡು ಬಗೆಗಳು ಅತ್ಯಂತ ಚಾಲ್ತಿಯಲ್ಲಿರುವ, ಶ್ವಾಸಕೋಶ ಕಾರ್ಸಿನೋಮದ ಊತಕಶಾಸ್ತ್ರೀಯ ಬಗೆಗಳಾಗಿವೆ; ಓರ್ವ ಊತಕರೋಗಶಾಸ್ತ್ರಜ್ಞನು ಸೂಕ್ಷ್ಮದರ್ಶಕವೊಂದರ ನೆರವಿನಿಂದ ಕಂಡುಕೊಂಡಂತೆ, ಪ್ರಾಣಾಂತಕ ಜೀವಕೋಶಗಳ ಗಾತ್ರ ಮತ್ತು ಹೊರನೋಟದಿಂದ ಈ ಬಗೆಗಳು ವರ್ಗೀಕರಿಸಲ್ಪಟ್ಟಿವೆ.[೧೫] ಕಾಯಿಲೆಯ ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಪ್ರಭೇದವು ನಿಸ್ಸಂಶಯವಾಗಿ ಅತ್ಯಂತ ಚಾಲ್ತಿಯಲ್ಲಿರುವ ಬಗೆಯಾಗಿದೆ (ಜೊತೆಯಲ್ಲಿರುವ ಕೋಷ್ಟಕವನ್ನು ನೋಡಿ).
| ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಊತಕಶಾಸ್ತ್ರೀಯ ಬಗೆಗಳ ಆವರ್ತನ [೧೫] | |
| ಊತಕಶಾಸ್ತ್ರೀಯ ಬಗೆ | ಆವರ್ತನ |
|---|---|
| ಸಣ್ಣದಲ್ಲದ-ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ | 80.4 |
| ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ | 16.8 |
| ಕಾರ್ಸಿನಾಯ್ಡ್[೧೬] | 0.8 |
| ಸಾರ್ಕೋಮ[೧೭] | 0.1 |
| ನಿರ್ದಿಷ್ಟವಾಗಿ ಹೇಳಲಾಗದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ | 1.9 |
ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ (NSCLC)
[ಬದಲಾಯಿಸಿ]
ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮಗಳ ಮುನ್ನರಿವು ಮತ್ತು ನಿರ್ವಹಣೆಗಳು ಒಂದೇ ರೀತಿಯವಾಗಿರುವುದರಿಂದ, ಅವುಗಳನ್ನು ಒಟ್ಟಾಗಿ ಗುಂಪುಮಾಡಲಾಗಿದೆ. ಇಲ್ಲಿ ಮೂರು ಮುಖ್ಯ ಉಪ-ಬಗೆಗಳು ಕಂಡುಬರುತ್ತವೆ. ಅವುಗಳೆಂದರೆ: ಪೊರೆಯುಕ್ತ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ, ಅಡಿನೊಕಾರ್ಸಿನೋಮ, ಮತ್ತು ದೊಡ್ಡ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ.
| ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಉಪ-ಬಗೆಗಳು: ಧೂಮಪಾನಿಗಳಲ್ಲಿ ಮತ್ತು ಎಂದಿಗೂ-ಧೂಮಪಾನಿಗಳಲ್ಲದವರಲ್ಲಿ [೧೮] ಕಂಡುಬರುವಂಥದ್ದು |
|||
| ಊತಕಶಾಸ್ತ್ರೀಯ ಉಪ-ಬಗೆ | ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳ ಆವರ್ತನ (%) | ||
|---|---|---|---|
| ಧೂಮಪಾನಿಗಳು | ಎಂದಿಗೂ-ಧೂಮಪಾನಿಗಳಲ್ಲದವರು | ||
| ಪೊರೆಯುಕ್ತ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ | 42 | 33 | |
| ಅಡಿನೊಕಾರ್ಸಿನೊಮ | ಅಡಿನೊಕಾರ್ಸಿನೋಮ (ಅನ್ಯಥಾ ನಿರ್ದಿಷ್ಟವಾಗಿ ಹೇಳಲಾಗದ್ದು) | 39 | 35 |
| ಶ್ವಾಸನಾಳದ ಸೂಕ್ಷ್ಮಕವಲಿನ ಕಿರುಗುಳಿಯ ಕಾರ್ಸಿನೋಮ | 4 | 10 | |
| ಕಾರ್ಸಿನಾಯ್ಡ್ | 7 | 16 | |
| ಇತರೆ | 8 | 6 | |
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳ[೧೯] ಪೈಕಿ 25%ನಷ್ಟು ಪಾಲು ಹೊಂದಿರುವ ಪೊರೆಯುಕ್ತ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವು, ಮಧ್ಯಭಾಗದ ಶ್ವಾಸನಾಳಿಕೆಯೊಂದರ ಸಮೀಪದಲ್ಲಿ ಸಾಮಾನ್ಯವಾಗಿ ಶುರುವಾಗುತ್ತದೆ. ಗೆಡ್ಡೆಯ ಮಧ್ಯಭಾಗದಲ್ಲಿ ಒಂದು ತಗ್ಗಾದ ಕುಹರ ಮತ್ತು ಸಂಬಂಧಿತ ಊತಕದ ಕ್ಷಯಿಸುವಿಕೆಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಕಂಡುಬರುತ್ತವೆ. ಸೂಕ್ತವಾಗಿ-ಪ್ರಭೇದ ಕಲ್ಪಿಸಲ್ಪಟ್ಟಿರುವ ಪೊರೆಯುಕ್ತ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳು, ಇತರ ಕ್ಯಾನ್ಸರ್ ಬಗೆಗಳಿಗಿಂತ ಅನೇಕವೇಳೆ ತುಂಬಾ ನಿಧಾನವಾಗಿ ಬೆಳೆಯುತ್ತವೆ.[೩]
ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳ ಪೈಕಿ ಅಡಿನೊಕಾರ್ಸಿನೋಮದ ಪಾಲು 40%ನಷ್ಟಿದೆ.[೧೯] ಶ್ವಾಸಕೋಶದ ಹೊರಮೈನ ಅಂಗಾಂಶದಲ್ಲಿ ಇದು ಸಾಮಾನ್ಯವಾಗಿ ಹುಟ್ಟಿಕೊಳ್ಳುತ್ತದೆ. ಅಡಿನೊಕಾರ್ಸಿನೋಮದ ಬಹುಪಾಲು ಪ್ರಕರಣಗಳು ಧೂಮಪಾನದೊಂದಿಗೆ ಸಂಬಂಧ ಹೊಂದಿರುತ್ತವೆ; ಆದಾಗ್ಯೂ, ಎಂದಿಗೂ ಧೂಮಪಾನಮಾಡದ ಜನರಲ್ಲಿ ("ಎಂದಿಗೂ-ಧೂಮಪಾನಿಗಳಲ್ಲದವರು") ಕಂಡುಬರುವ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಪೈಕಿ ಅಡಿನೊಕಾರ್ಸಿನೋಮವು ಅತ್ಯಂತ ಸಾಮಾನ್ಯವಾಗಿದೆ.[೨೦] ಶ್ವಾಸನಾಳದ ಸೂಕ್ಷ್ಮಕವಲಿನ ಕಿರುಗುಳಿಯ ಕಾರ್ಸಿನೋಮ ಎಂಬುದು ಅಡಿನೊಕಾರ್ಸಿನೋಮದ ಒಂದು ಉಪಬಗೆಯಾಗಿದ್ದು, ಎಂದಿಗೂ-ಧೂಮಪಾನಿಗಳಲ್ಲದ ಮಹಿಳೆಯರಲ್ಲಿ ಇದು ಹೆಚ್ಚು ಸಾಮಾನ್ಯವಾಗಿದೆ, ಮತ್ತು ಈ ನಿದರ್ಶನದಲ್ಲಿ ಚಿಕಿತ್ಸೆಗೆ ವಿಭಿನ್ನ ಪ್ರತಿಸ್ಪಂದನಗಳು ದೊರೆಯಬಹುದು.[೨೧]
ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ (SCLC)
[ಬದಲಾಯಿಸಿ]
ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವು ಅಪರೂಪವೆಂಬಂತೆ ಕಂಡುಬರುತ್ತದೆ. ಇದನ್ನು ಹಿಂದೆ "ಓಟ್ ಜೀವಕೋಶ"ದ ಕಾರ್ಸಿನೋಮ ಎಂಬುದಾಗಿ ಉಲ್ಲೇಖಿಸಲಾಗುತ್ತಿತ್ತು.[೨೨] ಬಹುಪಾಲು ಪ್ರಕರಣಗಳು ದೊಡ್ಡದಾದ ವಾಯುಮಾರ್ಗಗಳಲ್ಲಿ (ಪ್ರಾಥಮಿಕ ಮತ್ತು ದ್ವಿತೀಯಕ ಶ್ವಾಸನಾಳಿಕೆಗಳು) ಹುಟ್ಟಿಕೊಳ್ಳುತ್ತವೆ ಮತ್ತು ಕ್ಷಿಪ್ರವಾಗಿ ಬೆಳೆದು ಸಾಕಷ್ಟು ದೊಡ್ಡದಾಗಿ ಮಾರ್ಪಡುತ್ತವೆ.[೨೩] ಸಣ್ಣಕಾಳುಗಳಂಥ ರಚನೆಯುಳ್ಳ ದಟ್ಟವಾದ ನರಸ್ರಾವಕಗಳನ್ನು (ನರ-ಅಂತಃಸ್ರಾವಕ ಹಾರ್ಮೋನುಗಳನ್ನು ಹೊಂದಿರುವ ಕೋಶಕಗಳು) ಸಣ್ಣ ಜೀವಕೋಶಗಳು ಒಳಗೊಂಡಿದ್ದು, ಇವು ಈ ಗೆಡ್ಡೆಗೆ ಒಂದು ಅಂತಃಸ್ರಾವಕ/ಸದೃಶನವೋತಕದ ಸಹಲಕ್ಷಣಗಳ ಸಹಯೋಗವನ್ನು ನೀಡುತ್ತವೆ.[೨೪] ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ ಮತ್ತು ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಗೆ ಇದು ಆರಂಭದಲ್ಲಿ ಹೆಚ್ಚು ಸಂವೇದನಾಶೀಲವಾಗಿರುವಂತೆಯೇ, ಪ್ರಸ್ತುತಿಯ ಸಂದರ್ಭದಲ್ಲಿ ಅನೇಕವೇಳೆ ಸ್ಥಾನಾಂತರಣದ ಲಕ್ಷಣವನ್ನು ಹೊಂದಿರುತ್ತದೆ, ಮತ್ತು ಅಂತಿಮವಾಗಿ ಒಂದು ಕೆಟ್ಟದಾದ ಕಾಯಿಲೆಯ ಮುನ್ನರಿವನ್ನು ಒಯ್ಯುತ್ತದೆ. ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳು ಬಹಳ ಹಿಂದೆಯೇ ಎರಡು ಹಂತಗಳಾಗಿ ವಿಭಜಿಸಲ್ಪಟ್ಟಿವೆ. ಅವುಗಳೆಂದರೆ: ಸೀಮಿತ ಹಂತದ ಕಾಯಿಲೆ ಮತ್ತು ವ್ಯಾಪಕ ಹಂತದ ಕಾಯಿಲೆ. ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಈ ಬಗೆಯು ಧೂಮಪಾನದೊಂದಿಗೆ ದೃಢವಾದ ಸಂಬಂಧವನ್ನು ಹೊಂದಿದೆ.[೨೫]
ಇತರ ಬಗೆಗಳು
[ಬದಲಾಯಿಸಿ]ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳು ಅತೀವವಾದ ಮಿಶ್ರರೂಪವನ್ನು ಹೊಂದಿರುವ ವಿಷಮತೆಗಳಾಗಿದ್ದು, ಅತ್ಯಂತ ಸಾಮಾನ್ಯವಾಗಿರುವ ಒಂದಕ್ಕಿಂತ ಹೆಚ್ಚಿನ ಉಪಬಗೆಯನ್ನು ಇದರ ಗೆಡ್ಡೆಗಳು ಹೊಂದಿರುತ್ತವೆ.[೨೬]
ಶ್ವಾಸಕೋಶ ಮತ್ತು ಎದೆಗೂಡಿನ ಗೆಡ್ಡೆಗಳ ಊತಕಶಾಸ್ತ್ರೀಯ ಪ್ರಭೇದ ಕಲ್ಪಿಸುವಿಕೆಯ 4ನೇ ಪರಿಷ್ಕೃತ ರೂಪವು, ಪ್ರಸಕ್ತವಾಗಿ ಅತ್ಯಂತ ವ್ಯಾಪಕವಾಗಿ ಗುರುತಿಸಲ್ಪಟ್ಟಿರುವ ಮತ್ತು ಬಳಸಿಕೊಳ್ಳಲಾಗಿರುವ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ವರ್ಗೀಕರಣ ಪದ್ಧತಿಯಾಗಿದೆ; ವಿಶ್ವ ಆರೋಗ್ಯ ಸಂಸ್ಥೆ ಹಾಗೂ ಇಂಟರ್ನ್ಯಾಷನಲ್ ಅಸೋಸಿಯೇಷನ್ ಫಾರ್ ದಿ ಸ್ಟಡಿ ಆಫ್ ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ ಎಂಬ ಸಂಸ್ಥೆಯ ವತಿಯಿಂದ ಆದ ಒಂದು ಸಹಕಾರಿ ಪ್ರಯತ್ನವಾಗಿ ಈ ಪರಿಷ್ಕೃತ ರೂಪವು 2004ರಲ್ಲಿ ಪ್ರಕಟಿಸಲ್ಪಟ್ಟಿತು. ಹಲವಾರು ಹೆಚ್ಚುವರಿ ಉಪಬಗೆಗಳಾಗಿ ವ್ಯವಸ್ಥೆಗೊಳಿಸಲಾದ, ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದ ಇತರ ಹಲವಾರು ವಿಶಿಷ್ಟ ಊತಕ-ರೋಗಶಾಸ್ತ್ರೀಯ ಅಸ್ತಿತ್ವಗಳನ್ನು ಇದು ಗುರುತಿಸುತ್ತದೆ; ಸಾರ್ಕೋಮಾಟಾಯ್ಡ್ ಕಾರ್ಸಿನೋಮ, ಲಾಲಾ ಗ್ರಂಥಿಯ ಗೆಡ್ಡೆಗಳು, ಕಾರ್ಸಿನಾಯ್ಡ್ ಗೆಡ್ಡೆ, ಮತ್ತು ಅಡಿನೋಸ್ಕ್ವಾಮಸ್ ಕಾರ್ಸಿನೋಮ ಇವು ಇಂಥ ಹೆಚ್ಚುವರಿ ಉಪಬಗೆಗಳಲ್ಲಿ ಸೇರಿವೆ. ಮೇಲೆ ಹೇಳಿದ್ದರ ಪೈಕಿ ಕೊನೆಯ ಉಪಬಗೆಯು, ಕನಿಷ್ಟಪಕ್ಷ ತಲಾ 10%ನಷ್ಟು ಅಡಿನೊಕಾರ್ಸಿನೋಮ ಮತ್ತು ಪೊರೆಯುಕ್ತ ಜೀವಕೋಶದ ಕಾರ್ಸಿನೋಮವನ್ನು ಒಳಗೊಂಡಿರುವ ಗೆಡ್ಡೆಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಸಣ್ಣ ಜೀವಕೋಶದ ಕಾರ್ಸಿನೋಮ ಮತ್ತು ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಕಾರ್ಸಿನೋಮ ಈ ಎರಡನ್ನೂ ಒಳಗೊಂಡ ಒಂದು ಮಿಶ್ರಣವನ್ನು ಗೆಡ್ಡೆಯೊಂದು ಹೊಂದಿರುವುದು ಕಂಡುಬಂದಾಗ, ಇದನ್ನು ಸಣ್ಣ ಜೀವಕೋಶದ ಕಾರ್ಸಿನೋಮದ ಒಂದು ಭಿನ್ನರೂಪವಾಗಿ ವರ್ಗೀಕರಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ಇದನ್ನು ಒಂದು ಸಂಯೋಜಿತ ಸಣ್ಣ ಜೀವಕೋಶದ ಕಾರ್ಸಿನೋಮ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಸಂಯೋಜಿತ ಸಣ್ಣ ಜೀವಕೋಶದ ಕಾರ್ಸಿನೋಮವು, ಪ್ರಸಕ್ತವಾಗಿ ಗುರುತಿಸಲ್ಪಟ್ಟಿರುವ ಸಣ್ಣ ಜೀವಕೋಶದ ಕಾರ್ಸಿನೋಮದ ಏಕೈಕ ಭಿನ್ನರೂಪವಾಗಿದೆ.
ಶಿಶುಗಳಲ್ಲಿ ಮತ್ತು ಮಕ್ಕಳಲ್ಲಿ, ಪ್ಲ್ಯೂರೋಪಲ್ಮನರಿ ಬ್ಲಾಸ್ಟೋಮಾ ಮತ್ತು ಕಾರ್ಸಿನಾಯ್ಡ್ ಗೆಡ್ಡೆಗಳು ಅತ್ಯಂತ ಸಾಮಾನ್ಯವಾಗಿ ಕಂಡುಬರುವ ಪ್ರಧಾನವಾದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳಾಗಿವೆ.[೨೭]
ದ್ವಿತೀಯಕ ಕ್ಯಾನ್ಸರ್ಗಳು
[ಬದಲಾಯಿಸಿ]
ಶ್ವಾಸಕೋಶವು ಶರೀರದ ಇತರ ಭಾಗಗಳಿಂದ ಆಗುವ ಗೆಡ್ಡೆಗಳ ಸ್ಥಾನಾಂತರಣಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತಿರುವ ಒಂದು ಸಾಮಾನ್ಯ ಸ್ಥಳವಾಗಿದೆ. ದ್ವಿತೀಯಕ ಕ್ಯಾನ್ಸರ್ಗಳನ್ನು ಅವುಗಳ ಹುಟ್ಟಿನ ತಾಣದ ಆಧಾರದ ಮೇಲೆ ವರ್ಗೀಕರಿಸಲಾಗುತ್ತದೆ; ಉದಾಹರಣೆಗೆ, ಶ್ವಾಸಕೋಶಕ್ಕೆ ಹಬ್ಬಿಕೊಂಡಿರುವ ಎದೆಯಭಾಗದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಸ್ತನ ಕ್ಯಾನ್ಸರ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಸ್ಥಾನಾಂತರಣಗಳು ಅನೇಕವೇಳೆ ಒಂದು ವಿಶಿಷ್ಟವಾದ ದುಂಡನೆಯ ಹೊರನೋಟವನ್ನು ಹೊಂದಿರುವುದು ಎದೆಯ ರೇಡಿಯೋಗ್ರಾಫ್ ವಿಧಾನದಲ್ಲಿ ಕಂಡುಬರುತ್ತದೆ.[೨೮] ಶ್ವಾಸಕೋಶದ ಒಂಟಿಯಾಗಿರುವ ದುಂಡನೆಯ ಗಂಟುಗಳು, ಒಂದು ಅನಿಶ್ಚಿತವಾದ ವ್ಯಾಧಿಕಾರಣ ವಿಜ್ಞಾನದ ಅನುಸಾರ ವಿರಳವಾಗಿರದ ರಚನೆಗಳಾಗಿದ್ದು, ಅವು ಶ್ವಾಸಕೋಶದ ಅಂಗಾಂಶ ಪರೀಕ್ಷೆಯೊಂದನ್ನು ಸೂಚಿಸಬಹುದು.
ಮಕ್ಕಳಲ್ಲಿ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳ ಬಹುಪಾಲು ನಿದರ್ಶನಗಳು ದ್ವಿತೀಯಕವಾಗಿರುತ್ತವೆ.[೨೭]
ಪ್ರಾಥಮಿಕ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳು ಅತ್ಯಂತ ಸಾಮಾನ್ಯವಾಗಿ ಅಡ್ರೀನಲ್ ಗ್ರಂಥಿಗಳು, ಪಿತ್ತಜನಕಾಂಗ, ಮಿದುಳು, ಮತ್ತು ಮೂಳೆಗೆ ಸ್ವತಃ ಸ್ಥಾನಾಂತರಗೊಳ್ಳುತ್ತವೆ.[೩]
ಹಂತ ನಿರ್ಣಯಿಸುವಿಕೆ
[ಬದಲಾಯಿಸಿ]ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಹಂತದ ನಿರ್ಣಯಿಸುವಿಕೆಯು, ತನ್ನ ಮೂಲ ಆಕರದಿಂದ ಹರಡಲ್ಪಟ್ಟಿರುವ ಕ್ಯಾನ್ಸರ್ನ ಮಟ್ಟದ ಒಂದು ನಿರ್ಧಾರಣೆಯಾಗಿದೆ. ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಕಾಯಿಲೆಯ ಮುನ್ನರಿವು ಮತ್ತು ಸಂಭಾವ್ಯ ಚಿಕಿತ್ಸೆಯ ಮೇಲೆ ಪ್ರಭಾವ ಬೀರುವಲ್ಲಿ ಇದೊಂದು ಪ್ರಮುಖ ಅಂಶವೆನಿಸಿಕೊಂಡಿದೆ. ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವನ್ನು IA ಹಂತದಿಂದ ("ಒಂದು A"; ಕಾಯಿಲೆಯ ಅತ್ಯುತ್ತಮ ಮುನ್ನರಿವು) IV ಹಂತದವರೆಗೆ ("ನಾಲ್ಕು"; ಕಾಯಿಲೆಯ ಕೆಟ್ಟ ಮುನ್ನರಿವು) ನಿರ್ಣಯಿಸಲಾಗುತ್ತದೆ.[೨೯] ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವು ಒಂದುವೇಳೆ ಎದೆಯ ಒಂದರ್ಧ ಭಾಗಕ್ಕೆ ಸೀಮಿತಗೊಳಿಸಲ್ಪಟ್ಟಿದ್ದರೆ ಮತ್ತು ಅದು ಒಂದು ಏಕ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯ ಕ್ಷೇತ್ರದ ವ್ಯಾಪ್ತಿಯೊಳಗಿದ್ದರೆ, ಅದನ್ನು ಸೀಮಿತ ಹಂತ ಎಂಬುದಾಗಿ ವರ್ಗೀಕರಿಸಲಾಗುತ್ತದೆ; ಇಲ್ಲವಾದಲ್ಲಿ, ಅದನ್ನು ವ್ಯಾಪಕ ಹಂತ ಎಂಬುದಾಗಿ ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ.[೨೩]
ಚಿಹ್ನೆಗಳು ಹಾಗೂ ರೋಗಲಕ್ಷಣಗಳು
[ಬದಲಾಯಿಸಿ]ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಸೂಚಿಸುವ ರೋಗಲಕ್ಷಣಗಳಲ್ಲಿ ಇವು ಸೇರಿವೆ:[೩೦]
- ಕಟ್ಟುಸಿರು (ಉಸಿರಿನ ಅಲ್ಪತೆ)
- ಹಿಮೋಪ್ಟೈಸಿಸ್ (ರಕ್ತದ ಕೆಮ್ಮುವಿಕೆ)
- ದೀರ್ಘಕಾಲದ ಕೆಮ್ಮುವಿಕೆ ಅಥವಾ ಕೆಮ್ಮುವಿಕೆಯ ನಿಯತವಾದ ಮಾದರಿಯಲ್ಲಿನ ಬದಲಾವಣೆ
- ಉಬ್ಬಸಪಡುವಿಕೆ
- ಎದೆ ನೋವು ಅಥವಾ ಕಿಬ್ಬೊಟ್ಟೆಯಲ್ಲಿನ ನೋವು
- ಸೊರಗಿ ಹೋಗಿರುವಿಕೆ (ತೂಕದ ನಷ್ಟ), ಬಳಲಿಕೆ, ಮತ್ತು ಹಸಿವಿನ ನಷ್ಟ
- ಡಿಸ್ಫೋನಿಯಾ (ಒರಟೊರಟಾದ ಧ್ವನಿ)
- ಬೆರಳ ಉಗುರುಗಳ ಒಂದುಗೂಡುವಿಕೆ (ವಿರಳವಾದುದು)
- ಡಿಸ್ಫ್ಯಾಜಿಯಾ (ನುಂಗುವಿಕೆಯಲ್ಲಿನ ತೊಡಕು).
ಒಂದು ವೇಳೆ ವಾಯುಮಾರ್ಗದಲ್ಲಿ ಕ್ಯಾನ್ಸರ್ ಬೆಳೆದಿದ್ದೇ ಆದಲ್ಲಿ, ಅದು ಗಾಳಿಯ ಹರಿವಿಗೆ ತಡೆಯೊಡ್ಡಬಹುದು ಮತ್ತು ಅದರಿಂದಾಗಿ ಉಸಿರಾಟದಲ್ಲಿನ ತೊಡಕುಗಳು ಕಂಡುಬರಬಹುದು. ಇದರಿಂದಾಗಿ ತಡೆಗಟ್ಟಿದ ಪ್ರದೇಶದ ಹಿಂಭಾಗದಲ್ಲಿ ಸ್ರವಿಕೆಗಳು ಸಂಗ್ರಹಗೊಂಡು, ರೋಗಿಯು ನ್ಯುಮೋನಿಯಾಕ್ಕೆ ಒಳಗಾಗುವಂಥ ಸ್ಥಿತಿಯು ರೂಪುಗೊಳ್ಳಬಹುದು. ಅನೇಕ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳಿಗೆ ಸಮೃದ್ಧ ಪ್ರಮಾಣದಲ್ಲಿ ರಕ್ತದ ಪೂರೈಕೆಯಾಗುತ್ತದೆ. ಕ್ಯಾನ್ಸರ್ನ ಮೇಲ್ಮೈ ಭಾಗವು ನವಿರಾಗಿರಬಹುದಾದ್ದರಿಂದ, ಕ್ಯಾನ್ಸರ್ ಭಾಗದಿಂದ ವಾಯುಮಾರ್ಗದೊಳಗೆ ರಕ್ತಸ್ರಾವವಾಗುವ ಸಾಧ್ಯತೆಗಳಿರುತ್ತವೆ. ಇದೇ ರಕ್ತವು ತರುವಾಯದಲ್ಲಿ ಕೆಮ್ಮಲ್ಪಡಬಹುದು.
ಗೆಡ್ಡೆಯ ಬಗೆಯನ್ನು ಅವಲಂಬಿಸಿ, ಸದೃಶ ನವೋತಕದ ಸಂಗತಿಗಳು ಎಂದು ಕರೆಯಲ್ಪಡುವ ವಿದ್ಯಮಾನಗಳು ಆರಂಭದಲ್ಲಿ ಕಾಯಿಲೆಯೆಡೆಗೆ ಗಮನವನ್ನು ಸೆಳೆಯಬಹುದು.[೩೧] ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಲ್ಲಿ, ಈ ಸಂಗತಿಗಳಲ್ಲಿ ಇವೆಲ್ಲವೂ ಸೇರಿರಬಹುದು: ಲ್ಯಾಂಬರ್ಟ್-ಏಟನ್ ಸ್ನಾಯು ದೌರ್ಬಲ್ಯದ ಸಹಲಕ್ಷಣಗಳು (ಸ್ವತಂತ್ರ-ಪ್ರತಿಕಾಯಗಳ ಕಾರಣದಿಂದಾಗಿ ಕಂಡುಬರುವ ಸ್ನಾಯು ದುರ್ಬಲತೆ), ಹೈಪರ್ಕ್ಯಾಲ್ಸಿಮಿಯಾ, ಅಥವಾ ಅನುಚಿತವಾದ ಮೂತ್ರವರ್ಧನ-ನಿರೋಧಕ ಹಾರ್ಮೋನಿನ ಸಹಲಕ್ಷಣಗಳು (ಸಿಂಡ್ರೋಮ್ ಆಫ್ ಇನ್ಅಪ್ರೋಪ್ರಿಯೇಟ್ ಆಂಟಿಡೈಯುರೆಟಿಕ್ ಹಾರ್ಮೋನ್-SIADH). ಪ್ಯಾನ್ಕೋಸ್ಟ್ ಗೆಡ್ಡೆಗಳು[೩೨] ಎಂಬುದಾಗಿ ಕರೆಯಲ್ಪಡುವ, ಶ್ವಾಸಕೋಶದ ತುದಿಯಲ್ಲಿ (ಶೃಂಗದಲ್ಲಿ) ಇರುವ ಗೆಡ್ಡೆಗಳು ಅನುವೇದನಾ ನರವ್ಯೂಹದ ಸ್ಥಳೀಯ ಭಾಗದ ಮೇಲೆ ದಾಳಿಮಾಡಬಹುದು; ಇದರಿಂದಾಗಿ, ಬೆವರುವಿಕೆಯ ಮಾದರಿಗಳು ಬದಲಾಯಿಸಲ್ಪಡುವುದು ಹಾಗೂ ಕಣ್ಣಿನ ಸ್ನಾಯು ಸಮಸ್ಯೆಗಳು (ಹಾರ್ನರ್ನ ಸಹಲಕ್ಷಣಗಳು ಎಂದು ಕರೆಯಲ್ಪಡುವ ಒಂದು ಸಂಯೋಜನೆ) ಕಂಡುಬರುತ್ತವೆ. ಅಷ್ಟೇ ಅಲ್ಲ, ತೋಳಿನ ನರಜಾಲದ ಮೇಲೆ ಆಗುವ ಆಕ್ರಮಣದ ಕಾರಣದಿಂದಾಗಿ, ಕೈಗಳಲ್ಲಿ ಸ್ನಾಯು ದುರ್ಬಲತೆಯು ಕಂಡುಬರುತ್ತದೆ.
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಅನೇಕ ರೋಗಲಕ್ಷಣಗಳು (ಮೂಳೆ ನೋವು, ಜ್ವರ, ಮತ್ತು ತೂಕ ನಷ್ಟ) ಅನಿರ್ದಿಷ್ಟವಾಗಿವೆ; ವಯಸ್ಸಾದವರಲ್ಲಿ ಈ ರೋಗಲಕ್ಷಣಗಳಿಗೆ ಹೆಚ್ಚುವರಿ ರೋಗಲಕ್ಷಣದ ಅಸ್ವಸ್ಥತೆಯು ಕಾರಣವಾಗಿರಬಹುದು.[೩] ಅನೇಕ ರೋಗಿಗಳಲ್ಲಿ, ಅವರಿಗೆ ರೋಗಲಕ್ಷಣಗಳ ಅರಿವಾಗಿ ವೈದ್ಯಕೀಯ ನಿಗಾವಣೆಯನ್ನು ಅರಸಿಕೊಂಡು ಹೋಗುವ ವೇಳೆಗೆ, ಕ್ಯಾನ್ಸರ್ ತನ್ನ ಮೂಲತಾಣದಿಂದ ಆಚೆಗೆ ಹರಡಿಬಿಟ್ಟಿರುತ್ತದೆ. ಸ್ಥಾನಾಂತರಣದ ಸಾಮಾನ್ಯ ತಾಣಗಳಲ್ಲಿ ಮಿದುಳು, ಮೂಳೆ, ಅಡ್ರೀನಲ್ ಗ್ರಂಥಿಗಳು, ವಿರುದ್ಧ-ಪಾರ್ಶ್ವದ (ಎದುರಿನ) ಶ್ವಾಸಕೋಶ, ಪಿತ್ತಜನಕಾಂಗ, ಹೃದಯಾವರಣ, ಮತ್ತು ಮೂತ್ರಪಿಂಡಗಳು ಸೇರಿವೆ.[೩೩] ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಸಮಸ್ಯೆಯಿಂದ ಬಳಲುತ್ತಿರುವ ಜನರ ಪೈಕಿ ಸುಮಾರು 10%ನಷ್ಟು ಮಂದಿ ರೋಗನಿರ್ಣಯದ ವೇಳೆಯಲ್ಲಿ ರೋಗಲಕ್ಷಣಗಳನ್ನು ಹೊರಹೊಮ್ಮಿಸುವುದಿಲ್ಲ; ವಾಡಿಕೆಯಂತೆ ನಡೆಸುವ ಎದೆಯ ರೇಡಿಯೋಗ್ರಾಫ್ ಪರೀಕ್ಷೆಯಲ್ಲಿ ಈ ಕ್ಯಾನ್ಸರ್ಗಳು ಗೌಣವಾಗಿ ಕಂಡುಬರುತ್ತವೆ.[೨]
ಕಾರಣಗಳು
[ಬದಲಾಯಿಸಿ]ಯಾವುದೇ ಬಗೆಯ ಕ್ಯಾನ್ಸರಿನ ಮುಖ್ಯ ಕಾರಣಗಳಲ್ಲಿ ಕ್ಯಾನ್ಸರು ಜನಕಗಳು (ತಂಬಾಕು ಹೊಗೆಯಲ್ಲಿ ಇರುವಂಥವು), ಅಯಾನೀಕರಿಸುವ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆ, ಮತ್ತು ವೈರಾಣುವಿನ ಸೋಂಕು ಇವೆಲ್ಲವೂ ಸೇರಿಕೊಂಡಿರುತ್ತವೆ. ಈ ತೆರನಾದ ಒಡ್ಡಿಕೊಳ್ಳುವಿಕೆಯು, ಶ್ವಾಸಕೋಶಗಳ ಶ್ವಾಸನಾಳಿಕೆಗಳನ್ನು ಆವರಿಸಿರುವ ಅಂಗಾಂಶದಲ್ಲಿನ (ಶ್ವಾಸನಾಳಿಕೆಯ ಕವಲುಗಳ ಹೊರಪದರವನ್ನು ರೂಪಿಸುವ ಊತಕ) DNAಗೆ ಸಂಚಿತ ಬದಲಾವಣೆಗಳನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ. ಹೆಚ್ಚು ಹೆಚ್ಚು ಅಂಗಾಂಶವು ಹಾನಿಗೊಳಗಾದಂತೆ, ಅದರ ಪರಿಣಾಮವಾಗಿ ಒಂದು ಕ್ಯಾನ್ಸರ್ ಬೆಳೆಯುತ್ತಾ ಹೋಗುತ್ತದೆ.[೩]
ಧೂಮಪಾನ
[ಬದಲಾಯಿಸಿ]
ಧೂಮಪಾನವು, ಅದರಲ್ಲೂ ನಿರ್ದಿಷ್ಟವಾಗಿ ಸಿಗರೇಟುಗಳನ್ನು ಸೇದುವ ಅಭ್ಯಾಸವು, ನಿಸ್ಸಂಶಯವಾಗಿ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಕಾರಣವಾಗುವ ಮುಖ್ಯ ಕೊಡುಗೆದಾರನಾಗಿದೆ.[೩೪] ಸಿಗರೇಟಿನ ಹೊಗೆಯು 60ಕ್ಕೂ ಹೆಚ್ಚಿನ ಜ್ಞಾತ ಕ್ಯಾನ್ಸರು ಜನಕಗಳನ್ನು[೩೫] ಒಳಗೊಂಡಿದ್ದು, ಅವುಗಳಲ್ಲಿ ರೇಡಾನ್ ಕ್ಷಯಿಸುವಿಕೆಯ ಸರಣಿಯಿಂದ ಬಂದ ವಿಕಿರಣಶೀಲ ಐಸೊಟೋಪುಗಳು, ನೈಟ್ರೋಸಮೈನ್, ಮತ್ತು ಬೆಂಜೋಪೈರೀನ್ ಸೇರಿವೆ. ಇದರ ಜೊತೆಗೆ, ಒಡ್ಡಿಕೊಂಡಿರುವ ಅಂಗಾಂಶದಲ್ಲಿ ಕಾಣುವ ಪ್ರಾಣಾಂತಕ ಬೆಳವಣಿಗೆಗಳಿಗೆ ತೋರಿಸಬೇಕಾದ ಪ್ರತಿರಕ್ಷಣಾ ಪ್ರತಿಸ್ಪಂದನೆಯನ್ನು ನಿಕೋಟಿನ್ ತಗ್ಗಿಸುವಂತೆ ಕಂಡುಬರುತ್ತದೆ.[೩೬] ಅಭಿವೃದ್ಧಿ ಹೊಂದಿರುವ ದೇಶಗಳಾದ್ಯಂತ ಕಂಡುಬರುವ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಸಂಬಂಧಿ ಸಾವುಗಳ ಪೈಕಿ ಸರಿಸುಮಾರು 90%ನಷ್ಟು ಪ್ರಕರಣಗಳು ಧೂಮಪಾನದಿಂದ ಸಂಭವಿಸುತ್ತವೆ.[೩೭] ಅಮೆರಿಕಾ ಸಂಯುಕ್ತ ಸಂಸ್ಥಾನಗಳಲ್ಲಿನ ಸುಮಾರು 87%ನಷ್ಟು (ಪುರುಷರಲ್ಲಿ 90% ಮತ್ತು ಮಹಿಳೆಯರಲ್ಲಿ 85%) ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಪ್ರಕರಣಗಳಿಗೆ ಧೂಮಪಾನವೇ ಕಾರಣ ಎಂಬುದಾಗಿ ಅಂದಾಜಿಸಲಾಗಿದೆ.[೩೮] ಪುರುಷ ಧೂಮಪಾನಿಗಳ ಪೈಕಿ, ಜೀವಿತಾವಧಿಯಲ್ಲಿ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಬೆಳೆಸಿಕೊಳ್ಳುವುದರ ಅಪಾಯವು 17.2%ನಷ್ಟಿದ್ದರೆ, ಮಹಿಳಾ ಧೂಮಪಾನಿಗಳ ಪೈಕಿ ಈ ಅಪಾಯವು 11.6%ನಷ್ಟಿದೆ. ಧೂಮಪಾನಿಗಳಲ್ಲದವರಲ್ಲಿ ಈ ಅಪಾಯವು ಗಣನೀಯವಾಗಿ ಕಡಿಮೆ ಮಟ್ಟದಲ್ಲಿದ್ದು, ಪುರುಷರಲ್ಲಿ ಅದು 1.3%ನಷ್ಟಿದ್ದರೆ, ಮಹಿಳೆಯರಲ್ಲಿ 1.4%ನಷ್ಟಿದೆ.[೩೯]
ಧೂಮಪಾನ ಮಾಡುವ (ಹಿಂದಿನ ಧೂಮಪಾನಿಗಳು ಮತ್ತು ಪ್ರಸಕ್ತ ಧೂಮಪಾನಿಗಳು) ಮತ್ತು ಹಾರ್ಮೋನು ಚಿಕಿತ್ಸೆಯನ್ನು ತೆಗೆದುಕೊಳ್ಳುವ ಮಹಿಳೆಯರಲ್ಲಿ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಿಂದಾಗಿ ಸಾಯುವ ಅಪಾಯವು ಹೆಚ್ಚಿನ ಮಟ್ಟದಲ್ಲಿರುತ್ತದೆ. ಚೆಲ್ಬೊವ್ಸ್ಕಿ ಮತ್ತು ಇತರರಿಂದ ನಡೆಸಲ್ಪಟ್ಟು 2009ರಲ್ಲಿ ಪ್ರಕಟಿಸಲ್ಪಟ್ಟ ಅಧ್ಯಯನವೊಂದರಲ್ಲಿ ಬಿಂಬಿತವಾಗಿದ್ದ ಅಂಶದ ಅನುಸಾರ, ಪರೀಕ್ಷಾ-ಪ್ರಯೋಗಗಳ ಒಂದು ಹುಸಿಮದ್ದನ್ನು ತೆಗೆದುಕೊಳ್ಳುತ್ತಿರುವ ಮಹಿಳೆಯರಿಗೆ ಹೋಲಿಸಿದಾಗ ಹಾರ್ಮೋನುಗಳನ್ನು ತೆಗೆದುಕೊಳ್ಳುತ್ತಿರುವ ಮಹಿಳೆಯರು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಕಾಯಿಲೆಯಿಂದಾಗಿ ಸಾಯುವ ಸಂಭಾವ್ಯತೆಯು ಸುಮಾರು 60%ನಷ್ಟು ಹೆಚ್ಚಿತ್ತು. ಆಶ್ಚರ್ಯಕ್ಕೆ ಆಸ್ಪದವೇ ಇಲ್ಲವೆಂಬಂತೆ, ಪ್ರಸಕ್ತ ಧೂಮಪಾನಿಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಅಪಾಯವು ಅತಿಹೆಚ್ಚಿನದಾಗಿ ಕಂಡುಬಂದಿದ್ದರೆ, ಹಿಂದೆ ಧೂಮಪಾನ ಮಾಡುತ್ತಿದ್ದವರದು ನಂತರದ ಸ್ಥಾನವಾಗಿತ್ತು, ಮತ್ತು ಎಂದಿಗೂ ಧೂಮಪಾನಿಗಳಾಗಿಲ್ಲದವರಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಈ ಪ್ರಮಾಣವು ಅತ್ಯಂತ ಕಡಿಮೆಯದಾಗಿತ್ತು. ಧೂಮಪಾನ ಮಾಡಿದ ಮಹಿಳೆಯರ ಪೈಕಿ (ಹಿಂದಿನ ಅಥವಾ ಪ್ರಸಕ್ತ ಧೂಮಪಾನಿಗಳು), ಹಾರ್ಮೋನು ಚಿಕಿತ್ಸೆಯನ್ನು ತೆಗೆದುಕೊಳ್ಳುತ್ತಿದ್ದ 3.4%ನಷ್ಟು ಮಂದಿ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಿಂದ ಸತ್ತಿದ್ದರೆ, ಹುಸಿಮದ್ದನ್ನು ತೆಗೆದುಕೊಳ್ಳುತ್ತಿದ್ದ ಮಹಿಳೆಯರಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಈ ಪ್ರಮಾಣವು 2.3%ನಷ್ಟಿತ್ತು.[೪೦]
ಓರ್ವ ವ್ಯಕ್ತಿಯು ಮಾಡುವ ಧೂಮಪಾನದ ಅವಧಿಯು (ಮತ್ತು ಧೂಮಪಾನದ ಪ್ರಮಾಣವು), ಸದರಿ ವ್ಯಕ್ತಿಯು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಬೆಳೆಸಿಕೊಳ್ಳುವುದರ ಸಾಧ್ಯತೆಯನ್ನು ಹೆಚ್ಚಿಸುತ್ತದೆ. ಒಂದು ವೇಳೆ ವ್ಯಕ್ತಿಯೋರ್ವನು ಧೂಮಪಾನವನ್ನು ನಿಲ್ಲಿಸಿದರೆ, ಈ ಸಾಧ್ಯತೆಯು ಏಕಪ್ರಕಾರವಾಗಿ ತಗ್ಗುತ್ತದೆ; ಏಕೆಂದರೆ, ಶ್ವಾಸಕೋಶಗಳಿಗೆ ಆಗುವ ಹಾನಿಯು ದುರಸ್ತಿಯಾಗುತ್ತದೆ ಮತ್ತು ಮಾಲಿನ್ಯಕಾರಕ ಕಣಗಳು ಕ್ರಮೇಣವಾಗಿ ತೆಗೆಯಲ್ಪಡುತ್ತವೆ.[೪೧] ಇದರ ಜೊತೆಗೆ, ಧೂಮಪಾನಿಗಳಲ್ಲಿ[೪೨] ಕಂಡುಬರುವುದಕ್ಕೆ ಹೋಲಿಸಿದಾಗ, ಎಂದಿಗೂ-ಧೂಮಪಾನಿಗಳಲ್ಲದವರಲ್ಲಿನ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಕಾಯಿಲೆಯು ಒಂದು ಉತ್ತಮವಾದ ಮುನ್ನರಿವನ್ನು ಹೊಂದಿರುತ್ತದೆ ಎಂಬುದಕ್ಕೆ ಪುರಾವೆಯು ಲಭ್ಯವಿದೆ. ಅಷ್ಟೇ ಅಲ್ಲ, ಧೂಮಪಾನದ ಅಭ್ಯಾಸವನ್ನು ಕೈಬಿಟ್ಟವರಿಗೆ ಹೋಲಿಸಿದಾಗ, ರೋಗನಿರ್ಣಯದ ಸಮಯದಲ್ಲಿ ಧೂಮಪಾನ ಮಾಡುವ ರೋಗಿಗಳು, ಮೊಟುಕಾಗಿಸಿದ ಬದುಕುಳಿಯುವಿಕೆಯ ಅವಧಿಗಳನ್ನು ಹೊಂದಿರುತ್ತಾರೆ ಎಂಬುದಕ್ಕೂ ಪುರಾವೆಯಿದೆ.[೪೩]
ಮತ್ತೋರ್ವರು ಮಾಡುವ ಧೂಮಪಾನದಿಂದ ಹೊರಬಿಡಲ್ಪಟ್ಟ ಹೊಗೆಯ ಒಳಗೆಳೆದುಕೊಳ್ಳುವಿಕೆ ಎನಿಸಿರುವ ನಿಷ್ಕ್ರಿಯ ಧೂಮಪಾನವು, ಧೂಮಪಾನಿಗಳಲ್ಲದವರಲ್ಲಿ ಕಂಡುಬರುವ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಒಂದು ಕಾರಣವಾಗಿದೆ. ಓರ್ವ ಧೂಮಪಾನಿಯೊಂದಿಗೆ ವಾಸಿಸುತ್ತಿರುವ ಅಥವಾ ಕೆಲಸ ಮಾಡುತ್ತಿರುವ ಯಾರಾದರೊಬ್ಬ ವ್ಯಕ್ತಿಯನ್ನು ಓರ್ವ ನಿಷ್ಕ್ರಿಯ ಧೂಮಪಾನಿ ಎಂಬುದಾಗಿ ವರ್ಗೀಕರಿಸಲಾಗುತ್ತದೆ. ನಿಷ್ಕ್ರಿಯ ಧೂಮಪಾನಕ್ಕೆ ಒಡ್ಡಿಕೊಂಡಿರುವವರ ಪೈಕಿ ಕಂಡುಬರುವ ತುಲನಾತ್ಮಕ ಅಪಾಯದಲ್ಲಿ ಒಂದು ಗಣನೀಯ ಹೆಚ್ಚಳವಾಗಿರುವುದನ್ನು U.S.,[೪೪] ಯುರೋಪ್,[೪೫] UK,[೪೬] ಮತ್ತು ಆಸ್ಟ್ರೇಲಿಯಾ[೪೭] ಇವೇ ಮೊದಲಾದ ವಲಯಗಳಿಗೆ ಸೇರಿದ ಅಧ್ಯಯನಗಳು ಸುಸಂಗತವಾಗಿ ತೋರಿಸಿವೆ. ಪಾರ್ಶ್ವಹರಿವಿನ ಹೊಗೆಯ ಕುರಿತಾದ ಇತ್ತೀಚಿನ ತನಿಖೆಯು ಸೂಚಿಸುವ ಪ್ರಕಾರ, ನೇರವಾಗಿ ಒಳಗೆಳೆದುಕೊಳ್ಳುವ ಧೂಮಪಾನದ ಹೊಗೆಗಿಂತ ಪಾರ್ಶ್ವಹರಿವಿನ ಹೊಗೆಯು ಹೆಚ್ಚು ಅಪಾಯಕಾರಿಯಾಗಿದೆ.[೪೮]
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಈಡಾದ 10–15%ನಷ್ಟು ರೋಗಿಗಳು ಎಂದಿಗೂ ಧೂಮಪಾನ ಮಾಡದವರಾಗಿರುತ್ತಾರೆ.[೪೯] ಅಮೆರಿಕಾ ಸಂಯುಕ್ತ ಸಂಸ್ಥಾನದಲ್ಲಿ ಪ್ರತಿ ವರ್ಷವೂ ಎಂದಿಗೂ-ಧೂಮಪಾನ ಮಾಡದ 20,000ರಿಂದ 30,000ದಷ್ಟು ಸಂಖ್ಯೆಯ ಜನರು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಈಡಾಗುತ್ತಿದ್ದಾರೆ ಎಂಬುದು ಇದರರ್ಥ. ಐದು-ವರ್ಷ ಅವಧಿಯ ಬದುಕುಳಿಯುವಿಕೆಯ ಪ್ರಮಾಣದ ಕಾರಣದಿಂದಾಗಿ, ಎಂದಿಗೂ-ಧೂಮಪಾನ ಮಾಡದ ಜನರು U.S.ನಲ್ಲಿ ಪ್ರತಿ ವರ್ಷವೂ ಹೆಚ್ಚು ಪ್ರಮಾಣದಲ್ಲಿ ಸಾಯುತ್ತಾರೆ; ರಕ್ತದ ಕ್ಯಾನ್ಸರ್, ಅಂಡಾಶಯದ ಕ್ಯಾನ್ಸರ್, ಅಥವಾ AIDSನಿಂದ ಬಳಲುತ್ತಿರುವ ರೋಗಿಗಳ ಸಾವಿಗಿಂತ ಇವರ ಸಾವಿನ ಪ್ರಮಾಣ ಹೆಚ್ಚಿದೆ ಎಂಬುದು ಗಮನಾರ್ಹ ಸಂಗತಿ.[೫೦]
ರೇಡಾನ್ ಅನಿಲ
[ಬದಲಾಯಿಸಿ]ರೇಡಾನ್ ಎಂಬುದು ಒಂದು ವರ್ಣರಹಿತ ಮತ್ತು ವಾಸನೆರಹಿತ ಅನಿಲವಾಗಿದ್ದು, ವಿಕಿರಣಶೀಲ ರೇಡಿಯಂನ ವಿಘಟನೆಯಿಂದ ಅದು ಉತ್ಪಾದಿಸಲ್ಪಡುತ್ತದೆ; ವಿಕಿರಣಶೀಲ ರೇಡಿಯಂ ಕೂಡಾ ಭೂಮಿಯ ಹೊರಪದರದಲ್ಲಿ ಕಂಡುಬರುವ ಯುರೇನಿಯಂನ ಕ್ಷಯಿಸುವಿಕೆಯ ಉತ್ಪನ್ನವಾಗಿದೆ. ವಿಕಿರಣ ಕ್ಷಯಿಸುವಿಕೆಯ ಉತ್ಪನ್ನಗಳು ತಳೀಯ ಮೂಲದ್ರವ್ಯವನ್ನು ಅಯಾನುಗಳಾಗಿ ಪರಿವರ್ತಿಸುವುದರಿಂದ (ಅಂದರೆ, ಅಯಾನೀಕರಿಸುವುದರಿಂದ) ಹಠಾತ್ ಬದಲಾವಣೆಗಳು ಉಂಟಾಗಿ, ಕೆಲವೊಮ್ಮೆ ಅವು ಕ್ಯಾನ್ಸರ್ಯುಕ್ತವಾಗಿಯೂ ಬದಲಾಗುತ್ತವೆ. ರೇಡಾನ್ಗೆ ಒಡ್ಡಿಕೊಳ್ಳುವ ಪ್ರಕ್ರಿಯೆಯು, ಸಾಮಾನ್ಯ ಜನಸಮುದಾಯದಲ್ಲಿ ಕಂಡುಬರುವ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಎರಡನೇ ಪ್ರಮುಖ ಕಾರಣವಾಗಿದ್ದು, ಅದು ಧೂಮಪಾನದ[೮] ನಂತರದ ಸ್ಥಾನದಲ್ಲಿದೆ. ರೇಡಾನ್[೫೧] ಸಾಂದ್ರತೆಯಲ್ಲಿನ ಪ್ರತಿ 100 Bq/m^3 ಹೆಚ್ಚಳಕ್ಕೆ ಅಪಾಯದ ಪ್ರಮಾಣವು 8%ನಷ್ಟು ಹೆಚ್ಚಳಗೊಂಡು 16%ನಷ್ಟು ಮಟ್ಟಕ್ಕೆ ತಲುಪುತ್ತದೆ ಎಂಬ ಅಂಶವು ಈ ಕಳವಳಕ್ಕೆ ಪುಷ್ಟಿನೀಡುತ್ತದೆ. ನಿರ್ದಿಷ್ಟ ತಾಣ ಹಾಗೂ ಆಧಾರವಾಗಿರುವ ಮಣ್ಣು ಮತ್ತು ಬಂಡೆಗಳ ಸಂಯೋಜನೆಯ ಅನುಸಾರವಾಗಿ ರೇಡಾನ್ ಅನಿಲದ ಮಟ್ಟಗಳು ಬದಲಾಗುತ್ತಾ ಹೋಗುತ್ತವೆ. ಉದಾಹರಣೆಗೆ, UKಯಲ್ಲಿನ ಕಾರ್ನ್ವಾಲ್ನಂಥ ಪ್ರದೇಶಗಳಲ್ಲಿ (ಈ ಪ್ರದೇಶವು ಗ್ರಾನೈಟ್ನ್ನು ಉಪ-ಸ್ತರಶ್ರೇಣಿಗಳಾಗಿ ಹೊಂದಿದೆ), ರೇಡಾನ್ ಅನಿಲವು ಒಂದು ಪ್ರಮುಖ ಸಮಸ್ಯೆಯಾಗಿದೆ, ಮತ್ತು ರೇಡಾನ್ ಅನಿಲದ ಸಾಂದ್ರತೆಗಳನ್ನು ತಗ್ಗಿಸುವ ಸಲುವಾಗಿ ಇಲ್ಲಿನ ಕಟ್ಟಡಗಳಿಗೆ ಪಂಖಗಳನ್ನು ಬಳಸಿಕೊಂಡು ಬಲವಂತವಾಗಿ-ಗಾಳಿಬೆಳಕಿನ ವ್ಯವಸ್ಥೆ ಮಾಡಬೇಕಾಗಿ ಬರುತ್ತದೆ. ಅಮೆರಿಕಾ ಸಂಯುಕ್ತ ಸಂಸ್ಥಾನಗಳ ಪರಿಸರೀಯ ಸಂರಕ್ಷಣಾ ಸಂಸ್ಥೆಯು (ಎನ್ವಿರಾನ್ಮೆಂಟಲ್ ಪ್ರೊಟೆಕ್ಷನ್ ಏಜೆನ್ಸಿ-EPA) ಅಂದಾಜಿಸುವ ಪ್ರಕಾರ,
U.S.ನಲ್ಲಿನ 15 ಮನೆಗಳ ಪೈಕಿ ಒಂದು ಮನೆಯಲ್ಲಿ ಶಿಫಾರಿತ ಮಾರ್ಗದರ್ಶಿ ಸೂತ್ರಕ್ಕಿಂತ ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದಲ್ಲಿ, ಅಂದರೆ ಪ್ರತಿ ಲೀಟರ್ಗೆ 4 ಪಿಕೋಕ್ಯೂರಿಗಳಷ್ಟು ಇರಬೇಕಾದುದಕ್ಕಿಂತ (pCi/L) (148 Bq/m³) ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದಲ್ಲಿ ರೇಡಾನ್ ಮಟ್ಟಗಳಿವೆ.[೫೨] ಐಯೊವಾ ನಗರವು ಅಮೆರಿಕಾ ಸಂಯುಕ್ತ ಸಂಸ್ಥಾನಗಳಲ್ಲಿನ ಅತಿಹೆಚ್ಚಿನ ಸರಾಸರಿ ರೇಡಾನ್ ಸಾಂದ್ರತೆಯನ್ನು ಹೊಂದಿರುವ ನಗರ ಎನಿಸಿಕೊಂಡಿದೆ; ಅಲ್ಲಿ ನಿರ್ವಹಿಸಲ್ಪಟ್ಟ ಅಧ್ಯಯನಗಳು ನಿರೂಪಿಸಿರುವ ಪ್ರಕಾರ, EPAಯು ಶಿಫಾರಸು ಮಾಡಿರುವ ಕ್ರಿಯಾ ಮಟ್ಟವಾದ 4 pCi/Lಗಿಂತ ಮೇಲಿರುವ ಪ್ರಮಾಣದ ರೇಡಾನ್ಗೆ ದೀರ್ಘಕಾಲದವರೆಗೆ ಒಡ್ಡಿಕೊಳ್ಳುವುದರಿಂದ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಈಡಾಗುವ ಅಪಾಯವು 50%ನಷ್ಟು ಹೆಚ್ಚಳವಾಗುತ್ತದೆ.[೫೩][೫೪]
ಕಲ್ನಾರು
[ಬದಲಾಯಿಸಿ]
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಸೇರಿದಂತೆ, ಶ್ವಾಸಕೋಶದ ವೈವಿಧ್ಯಮಯ ಕಾಯಿಲೆಗಳನ್ನು ಕಲ್ನಾರು ಉಂಟುಮಾಡಬಲ್ಲದು. ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ರೂಪುಗೊಳ್ಳುವಿಕೆಯಲ್ಲಿ, ತಂಬಾಕು ಸೇದುವಿಕೆ ಮತ್ತು ಕಲ್ನಾರಿನ ನಡುವೆ ಒಂದು ಸಹಕ್ರಿಯೆಯ ಪರಿಣಾಮವಿದೆ.[೯] UKಯಲ್ಲಿನ ಪುರುಷ ಸಮುದಾಯದಲ್ಲಿ ಸಂಭವಿಸುವ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಸಂಬಂಧಿ ಸಾವಿನ ನಿದರ್ಶನಗಳ ಪೈಕಿ ಸುಮಾರು 2–3%ನಷ್ಟು ಭಾಗಕ್ಕೆ ಕಲ್ನಾರು ಕಾರಣವಾಗುತ್ತದೆ.[೫೫] ಮೀಸೋಥೆಲಿಯೋಮಾ (ಇದು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಿಂತ ವಿಭಿನ್ನವಾಗಿದೆ) ಎಂದು ಕರೆಯಲ್ಪಡುವ ಶ್ವಾಸಕೋಶಾವರಣದ ಕ್ಯಾನ್ಸರ್ಗೂ ಸಹ ಕಲ್ನಾರು ಕಾರಣವಾಗಬಲ್ಲದು.
ವೈರಾಣುಗಳು
[ಬದಲಾಯಿಸಿ]ವೈರಾಣುಗಳು ಪ್ರಾಣಿಗಳಲ್ಲಿ[೫೬][೫೭] ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಉಂಟುಮಾಡುತ್ತವೆ ಎಂಬುದು ತಿಳಿದ ವಿಷಯವಾಗಿದ್ದು, ಮಾನವರಲ್ಲಿಯೂ ಅಂಥದೊಂದು ಸ್ಥಿತಿಯನ್ನು ಹುಟ್ಟುಹಾಕುವ ಸಾಮರ್ಥ್ಯವನ್ನು ಅವು ಹೊಂದಿವೆ ಎಂಬುದಾಗಿ ಇತ್ತೀಚಿನ ಪುರಾವೆಯು ಸೂಚಿಸುತ್ತದೆ. ಇದಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ ಸೂಚಿಸಲ್ಪಟ್ಟಿರುವ ವೈರಾಣುಗಳಲ್ಲಿ ಇವು ಸೇರಿವೆ: ಮಾನವ ಪ್ಯಾಪಿಲ್ಲೋಮಾ ವೈರಾಣು,[೫೮] JC ವೈರಾಣು,[೫೯] ಸಿಮಿಯನ್ ವೈರಾಣು 40 (SV40), BK ವೈರಾಣು, ಮತ್ತು ಸೈಟೋಮೆಗಾಲೊ ವೈರಾಣು.[೬೦] ಈ ವೈರಾಣುಗಳು ಜೀವಕೋಶ ಚಕ್ರದ ಮೇಲೆ ಪ್ರಭಾವ ಬೀರಬಹುದು ಮತ್ತು ಅಪೋಪ್ಟೋಸಿಸ್ನ್ನು ಪ್ರತಿಬಂಧಿಸಬಹುದು; ಇದರಿಂದಗಿ ಅನಿಯಂತ್ರಿತ ಜೀವಕೋಶ ವಿಭಜನೆಗೆ ಅವಕಾಶನೀಡಿದಂತಾಗುತ್ತದೆ.
ಪೃಥಕ್ಕಣ ವಸ್ತು
[ಬದಲಾಯಿಸಿ]ಅಮೆರಿಕನ್ ಕ್ಯಾನ್ಸರ್ ಸೊಸೈಟಿಯು ಕೈಗೊಂಡಿರುವ ಅಧ್ಯಯನಗಳು ನೀಡಿರುವ ಮಾಹಿತಿಯ ಪ್ರಕಾರ, ಪೃಥಕ್ಕಣ ವಸ್ತುವಿಗೆ ಒಡ್ಡಿಕೊಳ್ಳುವಿಕೆ ಹಾಗೂ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ನಡುವೆ ಒಂದು ನೇರವಾದ ಸಂಬಂಧವಿದೆ. ಉದಾಹರಣೆಗೆ, ಒಂದು ವೇಳೆ ವಾಯುವಿನಲ್ಲಿನ ಕಣಗಳ ಸಾಂದ್ರತೆಯು ಕೇವಲ 1%ನಷ್ಟು ಹೆಚ್ಚಳಗೊಂಡರೂ ಸಹ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಬೆಳೆಸಿಕೊಳ್ಳುವುದರ ಅಪಾಯವು 14%ನಷ್ಟು ಹೆಚ್ಚುತ್ತದೆ.[೬೧][೬೨] ಮೇಲಾಗಿ, ಅತಿಸೂಕ್ಷ್ಮವಾಗಿರುವ ಕಣಗಳು ಶ್ವಾಸಕೋಶಗಳೊಳಗೆ ಮತ್ತಷ್ಟು ತೂರಿಕೊಳ್ಳುವುದರಿಂದ, ಕಣಗಳ ಗಾತ್ರವೂ ಲೆಕ್ಕಕ್ಕೆ ಬರುತ್ತದೆ ಎಂಬುದು ಸಮರ್ಥಿಸಲ್ಪಟ್ಟಿದೆ.[೬೩]
ರೋಗೋತ್ಪತ್ತಿ
[ಬದಲಾಯಿಸಿ]ಇತರ ಅನೇಕ ಕ್ಯಾನ್ಸರ್ಗಳ ರೀತಿಯಲ್ಲಿಯೇ, ಗೆಡ್ಡೆ ನಿರೋಧಕ ಜೀನುಗಳ ನಿಷ್ಕ್ರಿಯಕರಣ ಅಥವಾ ಗ್ರಂಥಿಜನಕ ಜೀನುಗಳ ಚುರುಕುಗೊಳಿಸುವಿಕೆಯಿಂದ (ಸಕ್ರಿಯೀಕರಣ) ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಚಾಲನೆ ಸಿಗುತ್ತದೆ.[೬೪] ಗ್ರಂಥಿಜನಕ ಜೀನುಗಳು, ಕ್ಯಾನ್ಸರ್ ಕಾಯಿಲೆಗೆ ಜನರು ಹೆಚ್ಚಾಗಿ ಈಡಾಗುವಂತೆ ಮಾಡುತ್ತವೆ ಎಂದು ಭಾವಿಸಲಾಗಿರುವ ಜೀನುಗಳಾಗಿವೆ. ಮೂಲ-ಗ್ರಂಥಿಜನಕ ಜೀನುಗಳು ನಿರ್ದಿಷ್ಟ ಕ್ಯಾನ್ಸರು ಜನಕಗಳಿಗೆ ಒಡ್ಡಲ್ಪಟ್ಟಾಗ, ಅವು ಗ್ರಂಥಿಜನಕ ಜೀನುಗಳಾಗಿ ಬದಲಾಗುತ್ತವೆ ಎಂದು ನಂಬಲಾಗಿದೆ.[೬೫] K-ರಾಸ್ ಮೂಲ-ಗ್ರಂಥಿಜನಕ ಜೀನಿನಲ್ಲಿನ ಹಠಾತ್ ಬದಲಾವಣೆಗಳು 10–30%ನಷ್ಟು ಶ್ವಾಸಕೋಶ ಅಡಿನೊಕಾರ್ಸಿನೋಮಗಳಿಗೆ ಹೊಣೆಗಾರರಾಗಿವೆ.[೬೬][೬೭] ಹೊರಚರ್ಮದ ಬೆಳವಣಿಗೆಯ ಅಂಶದ ಗ್ರಾಹಿಯು (ಎಪಿಡರ್ಮಲ್ ಗ್ರೋತ್ ಫ್ಯಾಕ್ಟರ್ ರಿಸೆಪ್ಟಾರ್-EGFR), ಜೀವಕೋಶದ ತ್ವರಿತ ಪ್ರಸರಣ, ಅಪೋಪ್ಟೋಸಿಸ್, ರಕ್ತನಾಳದ-ಜನ್ಯತೆ, ಮತ್ತು ಗೆಡ್ಡೆಯ ಆಕ್ರಮಣ ಇವುಗಳನ್ನು ನಿಯಂತ್ರಿಸುತ್ತದೆ.[೬೬] EGFRನ ಹಠಾತ್ ಬದಲಾವಣೆಗಳು ಮತ್ತು ವರ್ಧಿಸುವಿಕೆಗಳು ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಲ್ಲಿ ಸಾಮಾನ್ಯವಾಗಿರುತ್ತವೆ ಮತ್ತು EGFR-ಪ್ರತಿಬಂಧಕಗಳೊಂದಿಗಿನ ಚಿಕಿತ್ಸೆಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಆಧಾರವನ್ನು ಒದಗಿಸುತ್ತವೆ. Her2/neu ಎಂಬುದು ವಿರಳವಾಗಿ ಪ್ರಭಾವಕ್ಕೊಳಗಾಗುತ್ತದೆ.[೬೬] ವರ್ಣತಂತುವಿನ ಹಾನಿಯು
ಭಿನ್ನಯುಗ್ಮಜೀಯತೆಯ ನಷ್ಟಕ್ಕೆ ಕಾರಣವಾಗಬಲ್ಲದು. ಇದು ಗೆಡ್ಡೆ ನಿರೋಧಕ ಜೀನುಗಳ ನಿಷ್ಕ್ರಿಯಕರಣವನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ. 3p, 5q, 13q, ಮತ್ತು 17p ವರ್ಣತಂತುಗಳಿಗೆ ಆಗುವ ಹಾನಿಯು, ನಿರ್ದಿಷ್ಟವಾಗಿ ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದಲ್ಲಿ ಸಾಮಾನ್ಯವಾಗಿರುತ್ತದೆ. 17p ವರ್ಣತಂತುವಿನ ಮೇಲೆ ನೆಲೆಗೊಂಡಿರುವ p53 ಗೆಡ್ಡೆ ನಿರೋಧಕ ಜೀನು, 60-75%ನಷ್ಟು ಪ್ರಕರಣಗಳಲ್ಲಿ ಹಾನಿಗೊಳಗಾಗುತ್ತದೆ.[೬೮] ಅನೇಕವೇಳೆ ಹಠಾತ್ ಬದಲಾವಣೆಗೊಳಪಟ್ಟ ಅಥವಾ ವರ್ಧಿಸಲ್ಪಟ್ಟ ಇತರ ಜೀನುಗಳೆಂದರೆ, c-MET , NKX2-1 , LKB1 , PIK3CA , ಮತ್ತು BRAF .[೬೬]
ಹಲವಾರು ತಳೀಯ ಬಹುರೂಪತೆಗಳು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನೊಂದಿಗೆ ಸಂಬಂಧವನ್ನು ಹೊಂದಿವೆ. ಇಂಟರ್ಲ್ಯೂಕಿನ್-1,[೬೯] ಸೈಟೋಕ್ರೋಮ್ P450ಗಳಿಗೆ[೭೦] ಸಂಬಂಧಿಸಿದಂತೆ ಸಂಕೇತಿಸುವಿಕೆಯಲ್ಲಿ ತೊಡಗಿಸಿಕೊಂಡಿರುವ ಜೀನುಗಳಲ್ಲಿ, ಕ್ಯಾಪ್ಸೇಸ್-8ನಂಥ[೭೧] ಅಪೋಪ್ಟೋಸಿಸ್ ಪ್ರವರ್ತಕಗಳಲ್ಲಿ ಮತ್ತು XRCC1ನಂಥ DNA ದುರಸ್ತಿ ಕಣಗಳಲ್ಲಿ ಇರುವ ಬಹುರೂಪತೆಗಳು ಇವುಗಳಲ್ಲಿ ಸೇರಿವೆ.[೭೨] ಈ ಬಹುರೂಪತೆಗಳನ್ನು ಹೊಂದಿರುವ ಜನರು, ಕ್ಯಾನ್ಸರು ಜನಕಗಳಿಗೆ ಒಡ್ಡಿಕೊಂಡ ನಂತರ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಬೆಳೆಸಿಕೊಳ್ಳುವ ಸಾಧ್ಯತೆ ಹೆಚ್ಚು.
ಇತ್ತೀಚಿನ ಅಧ್ಯಯನವೊಂದು ಸೂಚಿಸಿರುವ ಪ್ರಕಾರ, MDM2 309G ಆಲೀಲ್ ಎಂಬುದು ಏಷ್ಯನ್ನರಲ್ಲಿ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಬೆಳೆಯುವುದಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ ಇರುವ, ಒಂದು ಕಡಿಮೆ ಪ್ರಮಾಣದಲ್ಲಿ-ಭೇದಿಸಿಕೊಂಡು ಹೋಗುವ ಅಪಾಯದ ಅಂಶವಾಗಿದೆ.[೭೩]
ರೋಗನಿರ್ಣಯ
[ಬದಲಾಯಿಸಿ]
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಸೂಚಿಸಬಹುದಾದ ರೋಗಲಕ್ಷಣಗಳನ್ನು ಒಂದು ವೇಳೆ ರೋಗಿಯೊಬ್ಬನು ವರದಿಮಾಡಿದರೆ, ಎದೆಯ ರೇಡಿಯೋಗ್ರಾಫ್ ಪರೀಕ್ಷೆಯನ್ನು ಕೈಗೊಳ್ಳುವುದು ರೋಗನಿರ್ಣಯದ ಮೊದಲ ಹಂತವೆನಿಸಿಕೊಳ್ಳುತ್ತದೆ. ಇದು ಒಂದು ಸ್ಪಷ್ಟವಾದ ರಾಶಿ, ವಿಭಾಜಕ ಭಿತ್ತಿಯು ಅಗಲವಾಗಿರುವಿಕೆ (ಅಲ್ಲಿರುವ ದುಗ್ಧಗ್ರಂಥಿಗಳಿಗೆ ಹರಡಿಕೆಯಾಗಿರುವುದರ ಸೂಚಕ), ಅಟಿಲೆಕ್ಟಾಸಿಸ್ (ಕುಸಿತ), ಗಟ್ಟಿಗೊಳಿಸುವಿಕೆ (ನ್ಯುಮೋನಿಯಾ), ಅಥವಾ ಎದೆಗೂಡಿನ ನಿಸ್ರಾವ ಇವೇ ಮೊದಲಾದ ಲಕ್ಷಣಗಳನ್ನು ಹೊರಗೆಡಹಬಹುದು. ಒಂದು ವೇಳೆ, ರೇಡಿಯೋಗ್ರಫಿ ವಿಧಾನದ ಮೂಲಕ ಕಾಯಿಲೆಯ ಕುರಿತಾದ ಯಾವುದೇ ಲಕ್ಷಣಗಳು ಕಂಡುಬರದಿದ್ದರೂ ಶಂಕೆಯು ಹೆಚ್ಚಿನ ಮಟ್ಟದಲ್ಲಿದ್ದರೆ (ಅಂದರೆ, ಸಂಬಂಧಿತ ವ್ಯಕ್ತಿಯು ರಕ್ತದ-ಕಲೆಯಿರುವ ಶ್ಲೇಷ್ಮವನ್ನು ಉಗುಳುವ ಓರ್ವ ಮಿರಿಮೀರಿದ ಧೂಮಪಾನಿಯಾಗಿರುವಂಥ ನಿದರ್ಶನಗಳಲ್ಲಿ), ಬ್ರಾಂಕೋಸ್ಕೋಪಿ ಮತ್ತು/ಅಥವಾ ಒಂದು CT ಕ್ಷಿಪ್ರಬಿಂಬವು ಅವಶ್ಯಕ ಮಾಹಿತಿಗಳನ್ನು ಒದಗಿಸಬಹುದು. ಬ್ರಾಂಕೋಸ್ಕೋಪಿ ಅಥವಾ CT-ನಿರ್ದೇಶಿತ ಅಂಗಾಂಶ ಪರೀಕ್ಷೆಯನ್ನು ಗೆಡ್ಡೆಯ ಬಗೆಯನ್ನು ಗುರುತಿಸಲೆಂದು ಅನೇಕವೇಳೆ ಬಳಸಲಾಗುತ್ತದೆ.[೨]
ಶ್ಲೇಷ್ಮದಲ್ಲಿನ ಜೀವಕೋಶಗಳಲ್ಲಿ ಕಂಡುಬರುವ ಅತಿರೇಕದ ಅಂಶಗಳು ("ಏಟಿಪಿಯಾ"), ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಅಪಾಯಕ್ಕೆ ಈಡಾಗಿರುವ ಒಂದು ಹೆಚ್ಚಿನ ಸಾಧ್ಯತೆಯೊಂದಿಗೆ ಸಂಬಂಧವನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಇತರ ರೋಗನಿದಾನ ಪರೀಕ್ಷೆಗಳೊಂದಿಗೆ ಸಂಯೋಜಿಸಲ್ಪಟ್ಟ ಶ್ಲೇಷ್ಮದ ಕೋಶವಿಜ್ಞಾನದ ಪರೀಕ್ಷೆಯು, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಸಾಕಷ್ಟು ಮುಂಚಿತವಾಗಿ ಪತ್ತೆಹಚ್ಚುವಲ್ಲಿ ಒಂದು ಪಾತ್ರವನ್ನು ವಹಿಸಬಹುದು.[೭೪]

ಎದೆಯ ರೇಡಿಯೋಗ್ರಾಫ್ ಪರೀಕ್ಷೆಯಲ್ಲಿ ವೈಪರೀತ್ಯಗಳನ್ನು ತೋರಿಸುವ ರೋಗಿಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತಿರುವ ಸಾಂದರ್ಭಿಕ ರೋಗನಿರ್ಣಯದಲ್ಲಿ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಮಾತ್ರವೇ ಅಲ್ಲದೇ ಪ್ರಾಣಾಂತಕವಲ್ಲದ ಕಾಯಿಲೆಗಳೂ ಸೇರಿಕೊಂಡಿರುತ್ತವೆ. ಕ್ಷಯರೋಗ ಅಥವಾ ನ್ಯುಮೋನಿಯಾದಂಥ ಸಾಂಕ್ರಾಮಿಕ ಕಾರಣಗಳು, ಅಥವಾ ಸಾರ್ಕಾಯ್ಡೋಸಿಸ್ನಂಥ ಉರಿಯೂತಕಾರಕ ಸ್ಥಿತಿಗತಿಗಳನ್ನು ಇವು ಒಳಗೊಳ್ಳುತ್ತವೆ. ಈ ಕಾಯಿಲೆಗಳು ಮೀಡಿಯಸ್ಟೀನಲ್ ಲಿಂಫಾಡೆನೊಪತಿ ಅಥವಾ ಶ್ವಾಸಕೋಶದ ಗಂಟುಗಳಲ್ಲಿ ಪರ್ಯಾವಸಾನಗೊಳ್ಳಬಹುದು, ಮತ್ತು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗಳನ್ನು ಕೆಲವೊಮ್ಮೆ ಅನುಕರಿಸಬಹುದು.[೩] ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಎಂಬುದು ಒಂದು ಪ್ರಾಸಂಗಿಕ ಆವಿಷ್ಕಾರವಾಗಿರಲೂ ಸಾಧ್ಯವಿದೆ: ಸಂಬಂಧಿಸದ ಕಾರಣವೊಂದಕ್ಕಾಗಿ ತೆಗೆದುಕೊಳ್ಳಲಾದ ಎದೆಯ ರೇಡಿಯೋಗ್ರಾಫ್ ಅಥವಾ CT ಕ್ಷಿಪ್ರಬಿಂಬದ ಪರೀಕ್ಷೆಯೊಂದರಲ್ಲಿ ಕಂಡುಬರುವ ಒಂದು ಒಂಟಿಯಾಗಿರುವ ಶ್ವಾಸಕೋಶದ ಗಂಟು (ಇದಕ್ಕೆ ಒಂದು ನಾಣ್ಯದಂತಿರುವ ಹಾನಿ ಎಂದೂ ಕರೆಯಲಾಗುತ್ತದೆ) ಇದಕ್ಕೊಂದು ನಿದರ್ಶನ.
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ನಿರ್ಣಾಯಕ ರೋಗನಿರ್ಣಯ ಮತ್ತು ಅದರ ವರ್ಗೀಕರಣ (ಮೇಲೆ ವಿವರಿಸಲ್ಪಟ್ಟಿರುವುದು) ಇವುಗಳು, ಸಂಶಯಾಸ್ಪದ ಅಂಗಾಂಶವನ್ನು ಸೂಕ್ಷ್ಮದರ್ಶಕದ ಅಡಿಯಲ್ಲಿ ಪರೀಕ್ಷಿಸುವುದನ್ನು ಆಧರಿಸಿವೆ.
ತಡೆಗಟ್ಟುವಿಕೆ
[ಬದಲಾಯಿಸಿ]ತಡೆಗಟ್ಟುವಿಕೆಯು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ವಿರುದ್ಧ ಹೋರಾಡುವುದಕ್ಕೆಂದು ಇರುವ ಅತ್ಯಂತ ವೆಚ್ಚ-ಪರಿಣಾಮಶೀಲ ವಿಧಾನವಾಗಿದೆ. ಬಹುತೇಕ ದೇಶಗಳಲ್ಲಿ ಕೈಗಾರಿಕಾ ಮತ್ತು ಗೃಹಬಳಕೆಯ ಕ್ಯಾನ್ಸರು ಜನಕಗಳನ್ನು ಗುರುತಿಸಿ ನಿಷೇಧಿಸಲಾಗಿದೆಯಾದರೂ, ತಂಬಾಕು ಧೂಮಪಾನವು ಈಗಲೂ ವ್ಯಾಪಕವಾಗಿ ಹಬ್ಬಿದೆ. ತಂಬಾಕು ಸೇದುವಿಕೆಯನ್ನು ತೆಗೆದುಹಾಕುವುದು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ತಡೆಗಟ್ಟುವಿಕೆಯಲ್ಲಿನ ಒಂದು ಪ್ರಧಾನ ಗುರಿಯಾಗಿದೆ, ಮತ್ತು ಈ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಧೂಮಪಾನದ ನಿಲುಗಡೆಯು ಒಂದು ಪ್ರಮುಖ ನಿರೋಧಕ ಸಾಧನ ಎಂದು ಕರೆಸಿಕೊಂಡಿದೆ.[೭೫] ಯುವಜನತೆಯನ್ನು ಉದ್ದೇಶಿಸಿ ಹಮ್ಮಿಕೊಳ್ಳಲಾಗಿರುವ ತಡೆಗಟ್ಟುವಿಕೆಯ ಕಾರ್ಯಸೂಚಿಗಳು ಅವುಗಳ ಪೈಕಿ ಅತೀವ ಪ್ರಾಮುಖ್ಯತೆಯನ್ನು ಹೊಂದಿವೆ. 1998ರಲ್ಲಿ, ಮಾಸ್ಟರ್ ಸೆಟ್ಲ್ಮೆಂಟ್ ಅಗ್ರಿಮೆಂಟ್ ಎಂಬ ಒಡಂಬಡಿಕೆಯು, ತಂಬಾಕು ಕಂಪನಿಗಳಿಂದ ಬರಬೇಕಾದ ಒಂದು ವಾರ್ಷಿಕ ಪಾವತಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ USAಯಲ್ಲಿನ 46 ಸಂಸ್ಥಾನಗಳಿಗೆ ಅರ್ಹತೆಯನ್ನು ನೀಡಿತು.[೭೬] ಫೈಸಲಾತಿಯ ಹಣ ಮತ್ತು ತಂಬಾಕು ತೆರಿಗೆಗಳ ನಡುವೆ, ಪ್ರತಿ ಸಂಸ್ಥಾನದ ಸಾರ್ವಜನಿಕ ಆರೋಗ್ಯ ಇಲಾಖೆಯು ತಡೆಗಟ್ಟುವಿಕೆಯ ಕುರಿತಾದ ತನ್ನ ಕಾರ್ಯಸೂಚಿಗಳಿಗೆ ಧನಸಹಾಯವನ್ನು ನೀಡುತ್ತದೆಯಾದರೂ, ಸಂಸ್ಥಾನಗಳ ಪೈಕಿ ಯಾವೊಂದೂ ಸಹ ಸೆಂಟರ್ ಫಾರ್ ಡಿಸೀಸ್ ಕಂಟ್ರೋಲ್ ವತಿಯಿಂದ ಶಿಫಾರಿತವಾಗಿರುವ ಮೊತ್ತದವರೆಗೆ ಖರ್ಚುಮಾಡುತ್ತಿಲ್ಲ; ಅಂದರೆ ಈ ತಡೆಗಟ್ಟುವಿಕೆಯ ಪ್ರಯತ್ನಗಳ ಮೇಲೆ ಅವು, ತಂಬಾಕು ತೆರಿಗೆಗಳು ಮತ್ತು ಫೈಸಲಾತಿ ಆದಾಯಗಳ ಪೈಕಿಯ 15 ಪ್ರತಿಶತದಷ್ಟು ಮೊತ್ತವನ್ನು ಮಾತ್ರವೇ ಖರ್ಚುಮಾಡುತ್ತಿವೆ.[೭೬]
ಭೋಜನಗೃಹಗಳು ಮತ್ತು ಕಾರ್ಯಕ್ಷೇತ್ರಗಳಂಥ ಸಾರ್ವಜನಿಕ ಪ್ರದೇಶಗಳಲ್ಲಿ ನಿಷ್ಕ್ರಿಯ ಧೂಮಪಾನವನ್ನು ತಗ್ಗಿಸುವುದಕ್ಕೆ ಸಂಬಂಧಿಸಿದ ಕಾರ್ಯನೀತಿಯ ಮಧ್ಯಸ್ಥಿಕೆಗಳು ಅನೇಕ ಪಾಶ್ಚಾತ್ಯ ದೇಶಗಳಲ್ಲಿ ಹೆಚ್ಚು ಸಾಮಾನ್ಯವಾಗಿ ಮಾರ್ಪಟ್ಟಿದ್ದು, ಇದಕ್ಕೆ ಪುಷ್ಟಿನೀಡುವಂತೆ ಕ್ಯಾಲಿಫೋರ್ನಿಯಾವು ಸಾರ್ವಜನಿಕ ಸಂಸ್ಥೆಗಳಲ್ಲಿ ಧೂಮಪಾನವನ್ನು ನಿಷೇಧಿಸುವ ಒಂದು ಕ್ರಮವನ್ನು ಕೈಗೊಳ್ಳಲು 1998ರಲ್ಲಿ ಮುಂದಾಯಿತು. 2004ರಲ್ಲಿ ಐರ್ಲೆಂಡ್ ಇದೇ ರೀತಿಯ ಪಾತ್ರವೊಂದನ್ನು ಯುರೋಪ್ನಲ್ಲಿ ನಿರ್ವಹಿಸಿತು. ಈ ಮೇಲ್ಪಂಕ್ತಿಯನ್ನು ಇಟಲಿ ಮತ್ತು ನಾರ್ವೆ 2005ರಲ್ಲಿ ಅನುಸರಿಸಿದರೆ, 2006ರಲ್ಲಿ ಸ್ಕಾಟ್ಲೆಂಡ್ ಹಾಗೂ ಇನ್ನಿತರ ದೇಶಗಳು, 2007ರಲ್ಲಿ ಇಂಗ್ಲಂಡ್, 2008ರಲ್ಲಿ ಫ್ರಾನ್ಸ್ ಮತ್ತು 2009ರಲ್ಲಿ ಟರ್ಕಿ ಈ ಬಗೆಯ ಕ್ರಮಗಳಿಗೆ ಮುಂದಾದವು. ನ್ಯೂಜಿಲೆಂಡ್ ದೇಶವು 2004ರ ವೇಳೆಗೆ ಸಾರ್ವಜನಿಕ ಸ್ಥಳಗಳಲ್ಲಿ ಧೂಮಪಾನವನ್ನು ನಿಷೇಧಿಸಿತು. ಭೂತಾನ್ ರಾಜ್ಯವು 2005ರಿಂದಲೂ ಸಂಪೂರ್ಣ ಧೂಮಪಾನ ನಿಷೇಧದ ಕಟ್ಟುಪಾಡೊಂದನ್ನು ಪಾಲಿಸಿಕೊಂಡು ಬಂದಿದೆ.[೭೭] ಅನೇಕ ದೇಶಗಳಲ್ಲಿ, ಇದೇ ರೀತಿಯ ನಿಷೇಧಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಒತ್ತಡದ ಗುಂಪುಗಳು ಪ್ರಚಾರ ಮಾಡುತ್ತಿವೆ. 2007ರಲ್ಲಿ, ಚಂಡೀಗಢ ನಗರವು ಭಾರತದಲ್ಲಿನ ಮೊಟ್ಟಮೊದಲ ಹೊಗೆ-ಮುಕ್ತ ನಗರ ಎನಿಸಿಕೊಂಡಿತು. ಭಾರತವು 2008ರ ಅಕ್ಟೋಬರ್ 2ರಂದು, ಸಾರ್ವಜನಿಕ ಸ್ಥಳಗಳಲ್ಲಿ ಧೂಮಪಾನ ಮಾಡುವುದರ ಮೇಲೆ ಒಂದು ಸಂಪೂರ್ಣ ನಿಷೇಧವನ್ನು ಹೇರುವ ಕ್ರಮವನ್ನು ಜಾರಿಗೆ ತಂದಿತು.
ಧೂಮಪಾನದ ಅಪರಾಧೀಕರಣ, ಕಳ್ಳ ಸಾಗಾಣಿಕೆಯ ಅಪಾಯವು ಹೆಚ್ಚಳವಾಗುವುದು, ಮತ್ತು ಇಂಥದೊಂದು ನಿಷೇಧವು ಜಾರಿಮಾಡಲಾಗದಿರುವಂಥ ಅಪಾಯ ಇವೆಲ್ಲವೂ ಇಂಥ ನಿಷೇಧಗಳ ವಿರುದ್ಧವಾಗಿ ಉಲ್ಲೇಖಿಸಲ್ಪಟ್ಟ ವಾದಗಳಾಗಿವೆ.[೭೮]
C ಜೀವಸತ್ವ, E ಜೀವಸತ್ವ ಮತ್ತು ಫೋಲೇಟ್ನಂಥ ಪೂರಕವಾದ ಬಹುಜೀವಸತ್ವಗಳ ದೀರ್ಘಾವಧಿ ಬಳಕೆಯು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಅಪಾಯವನ್ನು ತಗ್ಗಿಸುವುದಿಲ್ಲ. E ಜೀವಸತ್ವದ ಪೂರಕ ಅಂಶಗಳನ್ನು ಹೆಚ್ಚಿನ ಪ್ರಮಾಣಗಳಲ್ಲಿ ದೀರ್ಘಾವಧಿಯವರೆಗೆ ಸೇವಿಸುವುದರಿಂದ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಈಡಾಗುವ ಅಪಾಯವು ಅವಶ್ಯವಾಗಿ ಮತ್ತಷ್ಟು ಹೆಚ್ಚಾಗಲೂಬಹುದು.[೭೯]
ಯುವಜನತೆಯು ಧೂಮಪಾನದೆಡೆಗೆ ಆಕರ್ಷಿತವಾಗುವುದನ್ನು ತಡೆಗಟ್ಟಲೆಂದು, ತಂಬಾಕು ಜಾಹೀರಾತಿನ ಮೇಲೆ ಒಂದು ಸಂಪೂರ್ಣ ನಿಷೇಧವನ್ನು ಹೇರುವುದಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ ವಿಶ್ವ ಆರೋಗ್ಯ ಸಂಸ್ಥೆಯು ಸರ್ಕಾರಗಳಿಗೆ ಕರೆನೀಡಿದೆ. ಈಗಾಗಲೇ ಇಂಥ ನಿಷೇಧಗಳು ಹೇರಲ್ಪಟ್ಟಿರುವ ಪ್ರದೇಶಗಳಲ್ಲಿ ತಂಬಾಕು ಸೇವನೆಯು 16%ನಷ್ಟು ತಗ್ಗಿದೆ ಎಂಬ ಅಂಕಿ-ಅಂಶವನ್ನು ಅದು ಈ ಸಂದರ್ಭದಲ್ಲಿ ನೀಡಿದೆ.[೮೦]
ರೋಗನಿದಾನ
[ಬದಲಾಯಿಸಿ]ರೋಗವಾಹಕರಾಗಿರುವ ಜನರಲ್ಲಿನ ಕಾಯಿಲೆಯನ್ನು ಪತ್ತೆಹಚ್ಚಲೆಂದು ಬಳಸಲಾಗುವ ವೈದ್ಯಕೀಯ ಪರೀಕ್ಷೆಗಳಿಗೆ ರೋಗನಿದಾನ ಎಂದು ಉಲ್ಲೇಖಿಸಲಾಗುತ್ತದೆ. ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಸಂಬಂಧಿಸಿದಂತಿರುವ ಸಂಭಾವ್ಯ ರೋಗನಿದಾನ ಪರೀಕ್ಷೆಗಳಲ್ಲಿ ಎದೆಯ ರೇಡಿಯೋಗ್ರಾಫ್ ಅಥವಾ ಕಂಪ್ಯೂಟರ್ ಬಳಸಿ ಮಾಡಲಾದ ತಲಲೇಖನ (CT) ಇವು ಸೇರಿವೆ. 2009ರ ಡಿಸೆಂಬರ್ ವೇಳೆಗೆ ಇದ್ದಂತೆ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಸಂಬಂಧಿಸಿದಂತಿರುವ ರೋಗನಿದಾನದ ಕಾರ್ಯಸೂಚಿಗಳು ಯಾವುದೇ ಪ್ರಯೋಜನವನ್ನು ನಿರೂಪಿಸಿಲ್ಲ.[೮೧][೮೨]
ಚಿಕಿತ್ಸೆ
[ಬದಲಾಯಿಸಿ]ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಸಂಬಂಧಿಸಿದ ಚಿಕಿತ್ಸೆಯು, ಕ್ಯಾನ್ಸರ್ನ ನಿರ್ದಿಷ್ಟ ಜೀವಕೋಶದ ಬಗೆ, ಎಲ್ಲಿಯವರೆಗೆ ಅದು ಹರಡಿಕೆಯಾಗಿದೆ, ಮತ್ತು ರೋಗಿಯ ಕಾರ್ಯಕ್ಷಮತೆ ಸ್ಥಿತಿಯೇನು ಎಂಬ ಅಂಶಗಳ ಮೇಲೆ ಅವಲಂಬಿಸುತ್ತದೆ. ಶಸ್ತ್ರಚಿಕಿತ್ಸೆ, ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ, ಮತ್ತು ವಿಕಿರಣ ಚಿಕಿತ್ಸೆ ಇವುಗಳು ಸಾಮಾನ್ಯ ಚಿಕಿತ್ಸೆಗಳಲ್ಲಿ ಸೇರಿವೆ.[೨][೮೩]
ಶಸ್ತ್ರಚಿಕಿತ್ಸೆ
[ಬದಲಾಯಿಸಿ]
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಇರುವುದನ್ನು ಒಂದು ವೇಳೆ ತನಿಖೆಗಳು ದೃಢೀಕರಿಸಿದರೆ, ಕಾಯಿಲೆಯು ಸ್ಥಳೀಕರಿಸಲ್ಪಟ್ಟಿದೆಯೇ ಅಥವಾ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಗೆ ಸಗ್ಗುವ ರೀತಿಯಲ್ಲಿದೆಯೇ ಎಂಬುದನ್ನು ನಿರ್ಣಯಿಸಲು ಅಥವಾ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯ ಮೂಲಕವೂ ವಾಸಿಮಾಡಲಾಗದ ಹಂತಕ್ಕೆ ಅದು ಹರಡಿಕೊಂಡಿದೆಯೇ ಎಂಬುದನ್ನು ಅವಲೋಕಿಸಲು, CT ಕ್ಷಿಪ್ರಬಿಂಬ ವಿಧಾನವನ್ನು ಮತ್ತು ಅನೇಕವೇಳೆ ಪಾಸಿಟ್ರಾನ್ ಉತ್ಸರ್ಜನ ತಲಲೇಖನವನ್ನು (ಪಾಸಿಟ್ರಾನ್ ಎಮಿಷನ್ ಟೋಮೋಗ್ರಫಿ-PET) ಬಳಸಲಾಗುತ್ತದೆ.
ರೋಗಿಯು ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಗೊಳಗಾಗುವಷ್ಟು ಸಮರ್ಥನಾಗಿದ್ದಾನೆಯೇ ಇಲ್ಲವೇ ಎಂಬುದನ್ನು ನಿರ್ಣಯಿಸಲು, ರಕ್ತ ಪರೀಕ್ಷೆಗಳು ಮತ್ತು ಶ್ವಾಸಕೋಶ ಮಾಪನಗಳೂ (ಶ್ವಾಸಕೋಶ ಚಟುವಟಿಕೆ ಪರೀಕ್ಷಿಸುವಿಕೆ) ಸಹ ಅವಶ್ಯವಾಗಿರುತ್ತವೆ. ಒಂದು ವೇಳೆ ಶ್ವಾಸಕೋಶ ಮಾಪನವು ಉಸಿರಾಟದ ಮೀಸಲು ಕಳಪೆಯಾಗಿರುವುದನ್ನು ಹೊರಗೆಡಹಿದರೆ (ಅನೇಕವೇಳೆ ಇದು ತಡೆಯೊಡ್ಡುವ ದೀರ್ಘಕಾಲದ ಶ್ವಾಸಕೋಶದ ಕಾಯಿಲೆಯಿಂದ ಉಂಟಾಗುತ್ತದೆ), ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯು ವಿರುದ್ಧಚಿಹ್ನೆಯನ್ನು ತೋರಿಸಬಹುದು.
ರೋಗಿಯ ಶ್ವಾಸಕೋಶದ ಚಟುವಟಿಕೆ ಮತ್ತು ಇತರ ಅಪಾಯಕಾರಿ ಅಂಶಗಳನ್ನು ಅವಲಂಬಿಸಿ, ಸುಮಾರು 4.4%ನಷ್ಟಿರುವ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯಿಂದಾದ ಸಾವಿನ ಒಂದು ಪ್ರಮಾಣವನ್ನು ಸ್ವತಃ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯು ಹೊಂದಿದೆ.[೮೪] ಒಂದು ಶ್ವಾಸಕೋಶಕ್ಕಷ್ಟೇ ಸೀಮಿತವಾಗಿರುವ, IIIA ಹಂತದವರೆಗೆ ತಲುಪಿರುವ, ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದಲ್ಲಿ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆ ಎಂಬುದು ಸಾಮಾನ್ಯವಾಗಿ ಕೇವಲ ಒಂದು ಆಯ್ಕೆಯಾಗಿರುತ್ತದೆಯಷ್ಟೇ. ಇದನ್ನು ವೈದ್ಯಕೀಯ ಬಿಂಬಚಿತ್ರಣದ ವಿಧಾನವನ್ನು (ಕಂಪ್ಯೂಟರ್ ಬಳಸಿ ಮಾಡಲಾದ ತಲಲೇಖನ, ಪಾಸಿಟ್ರಾನ್ ಉತ್ಸರ್ಜನ ತಲಲೇಖನ) ಬಳಸಿಕೊಂಡು ನಿರ್ಣಯಿಸಲಾಗುತ್ತದೆ. ಅಂಗಾಂಶವು ತೆಗೆಯಲ್ಪಟ್ಟ ನಂತರ ಸಾಕಷ್ಟು ಪ್ರಮಾಣದಲ್ಲಿ ಶ್ವಾಸಕೋಶದ ಚಟುವಟಿಕೆಗೆ ಅವಕಾಶನೀಡುವ ಸಲುವಾಗಿ, ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಗೆ-ಮುಂಚಿನ ಒಂದು ಉಸಿರಾಟದ ಮೀಸಲು ಹೇರಳವಾಗಿರಬೇಕಾದುದು ಅಗತ್ಯವಾಗಿರುತ್ತದೆ.
ಕಾರ್ಯವಿಧಾನಗಳಲ್ಲಿ ಇವೆಲ್ಲವೂ ಸೇರಿವೆ: ಬೆಣೆರಚನೆಯಿಂದ ಮಾಡಿದ ಅಂಶಛೇದನ (ಹಾಲೆಯೊಂದರ ಭಾಗವನ್ನು ತೆಗೆದುಹಾಕುವುದು), ಸೆಗ್ಮೆಂಟೆಕ್ಟಮಿ (ಶ್ವಾಸಕೋಶದ ನಿರ್ದಿಷ್ಟ ಹಾಲೆಯೊಂದರ ಅಂಗರಚನೆಯ ವಿಭಾಗವೊಂದನ್ನು ತೆಗೆದುಹಾಕುವುದು), ಹಾಲೆಕಡಿತ (ಒಂದು ಹಾಲೆ), ಎರಡು ಹಾಲೆಕಡಿತ (ಎರಡು ಹಾಲೆಗಳು), ಅಥವಾ ಶ್ವಾಸಕೋಶಛೇದನೆ (ಇಡೀ ಶ್ವಾಸಕೋಶ). ಹಾಲೆಕಡಿತವು ಸ್ಥಳೀಯ ಪ್ರತ್ಯಾವರ್ತನೆಯ ಅವಕಾಶವನ್ನು ತಗ್ಗಿಸುವುದರಿಂದ, ಸಾಕಾಗುವಷ್ಟು ಪ್ರಮಾಣದಲ್ಲಿ ಉಸಿರಾಟದ ಮೀಸಲನ್ನು ಹೊಂದಿರುವ ರೋಗಿಗಳಲ್ಲಿ, ಹಾಲೆಕಡಿತವು ಆದ್ಯತೆಯ ಆಯ್ಕೆಯಾಗಿರುತ್ತದೆ. ಇದನ್ನು ನೆರವೇರಿಸುವುದಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ, ಒಂದು ವೇಳೆ ರೋಗಿಯು ಸಾಕಷ್ಟು ಕ್ರಿಯಾತ್ಮಕವಾಗಿರುವ ಶ್ವಾಸಕೋಶವನ್ನು ಹೊಂದಿಲ್ಲವಾದಲ್ಲಿ, ಬೆಣೆರಚನೆಯಿಂದ ಮಾಡಿದ ಅಂಶಛೇದನವನ್ನು ನಿರ್ವಹಿಸಬೇಕಾಗಬಹುದು.[೮೫] ಬೆಣೆರಚನೆಯಿಂದ ಮಾಡಿದ ಛೇದನದ ಅಂಚುಗಳಲ್ಲಿ ಮಾಡಲಾಗುವ ವಿಕಿರಣಶೀಲ ಅಯೋಡಿನ್ ಹೃಸ್ವಚಿಕಿತ್ಸೆಯು, ಹಾಲೆಕಡಿತಕ್ಕೆ ಸಂಬಂಧಿಸಿದ ಪ್ರತ್ಯಾವರ್ತನೆಯನ್ನು ತಗ್ಗಿಸಬಹುದು.[೮೬]
ದೃಶ್ಯಭಾಗದ-ನೆರವಿನ ಥೊರಾಕೋಸ್ಕೋಪಿಕ್ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆ ಮತ್ತು VATS ಹಾಲೆಕಡಿತದ ಚಿಕಿತ್ಸೆಗಳು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಗೆ ಸಂಬಂಧಿಸಿದ, ಕನಿಷ್ಟತಮ ಪ್ರಮಾಣದಲ್ಲಿ ಆಕ್ರಮಣಶೀಲವಾಗಿರುವ ವಿಧಾನಗಳಿಗಾಗಿ ಅವಕಾಶ ನೀಡಿವೆ; ಕ್ಷಿಪ್ರವಾದ ಚೇತರಿಕೆ, ಅಲ್ಪಾವಧಿಯ ಆಸ್ಪತ್ರೆ-ವಾಸ ಮತ್ತು ತಗ್ಗಿದ ಆಸ್ಪತ್ರೆ-ವೆಚ್ಚಗಳಂಥ ಪ್ರಯೋಜನಗಳನ್ನು ಈ ವಿಧಾನಗಳು ಹೊಂದಿರಲು ಸಾಧ್ಯವಿದೆ.[೮೭]
ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ
[ಬದಲಾಯಿಸಿ]ಗೆಡ್ಡೆಯ ಬಗೆಯ ಮೇಲೆ ಸಂಯೋಜನೆಯ ಕಟ್ಟುಪಾಡು ಅವಲಂಬಿಸುತ್ತದೆ. ಒಂದು ವೇಳೆ ತುಲನಾತ್ಮಕವಾಗಿ ಆರಂಭಿಕ ಹಂತದಲ್ಲಿದ್ದರೂ ಸಹ, ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವನ್ನು ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ ಮತ್ತು ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯ[೮೮] ನೆರವಿನಿಂದ ಉಪಚರಿಸಲಾಗುತ್ತದೆ; ಬದುಕುಳಿಯುವಿಕೆಯ ಮೇಲೆ ಪ್ರಮಾಣೀಕರಿಸಲು ಸಾಧ್ಯವಾಗುವ ಯಾವುದೇ ಪ್ರಭಾವವನ್ನು ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯು ಹೊಂದಿಲ್ಲದಿರುವುದೇ ಇದಕ್ಕೆ ಕಾರಣ. ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದಲ್ಲಿ, ಸಿಸ್ಪ್ಲೇಟಿನ್ ಮತ್ತು ಎಟೊಪೊಸೈಡ್ಗಳನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ.[೮೯] ಕಾರ್ಬೋಪ್ಲೇಟಿನ್, ಜೆಮ್ಸಿಟ್ಯಾಬೈನ್, ಪ್ಯಾಕ್ಲಿಟ್ಯಾಕ್ಸೆಲ್, ವಿನೋರೆಲ್ಬೈನ್, ಟೋಪೋಟೆಕಾನ್, ಮತ್ತು ಇರಿನೋಟೆಕಾನ್ ಜೊತೆಗಿನ ಸಂಯೋಜನೆಗಳನ್ನೂ ಸಹ ಬಳಸಲಾಗುತ್ತದೆ.[೯೦][೯೧] ವ್ಯಾಪಕ-ಹಂತಕ್ಕೆ ತಲುಪಿರುವ ಸಣ್ಣ-ಜೀವಕೋಶ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಲ್ಲಿ, ಸೆಲೆಕೋಕ್ಸಿಬ್ ಒಂದು ಪಾತ್ರವನ್ನು ವಹಿಸಬಹುದು.[೯೨]
ಸ್ಥಾನಾಂತರಣದ ಲಕ್ಷಣವನ್ನು ಹೊಂದಿರುವ, ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದಲ್ಲಿ ಪ್ರಾಥಮಿಕ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯನ್ನೂ ಸಹ ನೀಡಲಾಗುತ್ತದೆ. ಮುಂದುವರಿದ ಹಂತದ, ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವನ್ನು ಸಿಸ್ಪ್ಲೇಟಿನ್ ಅಥವಾ ಕಾರ್ಬೋಪ್ಲೇಟಿನ್ ಬಳಸಿಕೊಂಡು ಅನೇಕವೇಳೆ ಉಪಚರಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ಇವುಗಳೊಂದಿಗೆ ಜೆಮ್ಸಿಟ್ಯಾಬೈನ್, ಪ್ಯಾಕ್ಲಿಟ್ಯಾಕ್ಸೆಲ್, ಡೊಸೆಟ್ಯಾಕ್ಸೆಲ್, ಎಟೊಪೊಸೈಡ್, ಅಥವಾ ವಿನೋರೆಲ್ಬೈನ್ನ್ನು ಸಂಯೋಜಿಸಲಾಗುತ್ತದೆ ಎಂಬುದು ವಿಶೇಷ.[೯೩] ಸಮಂಜಸವಾದ ಸಾಮಾನ್ಯ ಕಾರ್ಯಕ್ಷಮತೆಯ ಸ್ಥಿತಿಯನ್ನು ಹೊಂದಿರುವ 70 ವರ್ಷಗಳಿಗಿಂತ ಕಡಿಮೆ ವಯಸ್ಸಿನ ರೋಗಿಗಳಲ್ಲಿ, ಪ್ಯಾಕ್ಲಿಟ್ಯಾಕ್ಸೆಲ್ ಮತ್ತು ಕಾರ್ಬೋಪ್ಲೇಟಿನ್ ಬಳಸಿಕೊಂಡು ಉಪಚರಿಸಲಾದ ಪೊರೆರಹಿತ ಕ್ಯಾನ್ಸರ್ಗಳಲ್ಲಿನ ಫಲಿತಾಂಶಗಳನ್ನು ಬೆವಾಸಿಜುಮಾಬ್ ಸುಧಾರಿಸುತ್ತದೆ.[೯೪] ಶ್ವಾಸನಾಳದ ಕಿರುಗುಳಿಯ ಕಾರ್ಸಿನೋಮ ಎಂಬುದು, ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದ ಒಂದು ಉಪಬಗೆಯಾಗಿದ್ದು, ಅದು ಜೆಫಿಟಿನಿಬ್[೯೫] ಮತ್ತು ಎರ್ಲೋಟಿನಿಬ್ಗಳಿಗೆ ಪ್ರತಿಸ್ಪಂದಿಸಬಹುದಾಗಿರುತ್ತದೆ.[೯೬]
ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ, ಆಣ್ವಿಕ ಆನುವಂಶಿಕ ಉಪಬಗೆಗೆ ಸಂಬಂಧಿಸಿದ ಪರೀಕ್ಷಿಸುವಿಕೆಯು, ಅತ್ಯಂತ ಸೂಕ್ತವಾದ ಆರಂಭಿಕ ಚಿಕಿತ್ಸೆಯನ್ನು[೯೭] ಆಯ್ದುಕೊಳ್ಳುವಲ್ಲಿ ನೆರವಾಗಬಹುದು; ಉದಾಹರಣೆಗೆ, ಹೊರಚರ್ಮದ ಬೆಳವಣಿಗೆಯ ಅಂಶದ ಗ್ರಾಹಿ ಜೀನಿನ[೯೮] ಹಠಾತ್ ಬದಲಾವಣೆಯು, ನಿರ್ದಿಷ್ಟ ಪ್ರತಿಬಂಧಕವನ್ನು ಬಳಸಿಕೊಂಡು ಮಾಡುವ ಆರಂಭಿಕ ಚಿಕಿತ್ಸೆಯು ಹೆಚ್ಚು ಪ್ರಯೋಜನಕಾರಿಯೇ ಅಥವಾ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯನ್ನು ಬಳಸಿಕೊಂಡು ಮಾಡುವ ಆರಂಭಿಕ ಚಿಕಿತ್ಸೆಯು ಹೆಚ್ಚು ಪ್ರಯೋಜನಕಾರಿಯೇ ಎಂಬುದನ್ನು ಮುನ್ನುಡಿಯಬಹುದು.[೯೯]
ಮುಂದುವರಿದ ಹಂತದ ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಲ್ಲಿ, ಚಿಕಿತ್ಸೆಗೆ ದೊರಕಿದ ಒಂದು ಆರಂಭಿಕ ಪ್ರತಿಸ್ಪಂದನದ ನಂತರ ಚಿಕಿತ್ಸೆಯನ್ನು ಮುಂದುವರಿಸುವುದಕ್ಕೆ ನಿರ್ವಹಣಾ ಚಿಕಿತ್ಸೆ ಎಂದು ಉಲ್ಲೇಖಿಸಲಾಗುತ್ತದೆ.[೧೦೦] ಆರಂಭಿಕ ಚಿಕಿತ್ಸೆಗಿಂತಲೂ ವಿಭಿನ್ನವಾದ ಔಷಧೀಕರಣಗಳಿಗೆ ಸ್ವಿಚ್ಚು ನಿರ್ವಹಣೆಯು ಬದಲಾವಣೆಯಾಗುತ್ತದೆ ಮತ್ತು ಪೆಮೆಟ್ರೆಕ್ಸ್ಡ್,[೧೦೧] ಎರ್ಲೋಟಿನಿಬ್,[೧೦೨] ಮತ್ತು ಡೊಸೆಟ್ಯಾಕ್ಸೆಲ್[೧೦೩] ಇವೇ ಮೊದಲಾದವುಗಳನ್ನು ಅದು ಬಳಸಬಲ್ಲದಾಗಿರುತ್ತದೆ; ಆದರೂ ಪೊರೆರಹಿತ NSCLCಯಲ್ಲಿ ಮಾತ್ರವೇ ಪೆಮೆಟ್ರೆಕ್ಸ್ಡ್ನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.[೧೦೪]
NSCLCಗೆ ಸಂಬಂಧಿಸಿದ ಸಹೌಷಧದ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ
[ಬದಲಾಯಿಸಿ]ಚಿಕಿತ್ಸೆಯ ಪರಿಣಾಮವನ್ನು ಸುಧಾರಿಸುವ ಸಲುವಾಗಿ, ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯ ನಂತರ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯ ಬಳಕೆ ಮಾಡುವುದನ್ನು ಸಹೌಷಧದ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯ ಸಂದರ್ಭದಲ್ಲಿ, ದುಗ್ಧಗ್ರಂಥಿಗಳಿಂದ ಮಾದರಿಗಳನ್ನು ತೆಗೆದುಕೊಳ್ಳಲಾಗುತ್ತದೆ. ಒಂದು ವೇಳೆ ಈ ಮಾದರಿಗಳು ಕ್ಯಾನ್ಸರ್ನ್ನು ಒಳಗೊಂಡಿದ್ದರೆ, ರೋಗಿಯು IIನೇ ಹಂತದ ಅಥವಾ IIIನೇ ಹಂತದ ಕಾಯಿಲೆಯನ್ನು ಹೊಂದಿರುತ್ತಾನೆ. ಈ ಸನ್ನಿವೇಶದಲ್ಲಿ, ಸಹೌಷಧದ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯು ಬದುಕುಳಿಯುವಿಕೆಯ ಸಾಧ್ಯತೆಯನ್ನು 15%ನಷ್ಟರವರೆಗೆ ಸುಧಾರಿಸಬಹುದು.[೧೦೫][೧೦೬] ಪ್ಲಾಟಿನಮ್-ಆಧರಿಸಿದ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯನ್ನು (ಸಿಸ್ಪ್ಲೇಟಿನ್ ಅಥವಾ ಕಾರ್ಬೋಪ್ಲೇಟಿನ್ನ್ನು ಒಳಗೊಂಡಂತೆ) ನೀಡುವುದು ಅನೇಕವೇಳೆ ಪ್ರಮಾಣಕ ಪರಿಪಾಠ ಎನಿಸಿಕೊಳ್ಳುತ್ತದೆ.[೧೦೭] ಆದಾಗ್ಯೂ, ಪ್ಲಾಟಿನಮ್-ಆಧರಿತ ಸಹೌಷಧದ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯ ಪ್ರಯೋಜನವು, ಕಡಿಮೆ ಮಟ್ಟದ ERCC1 (ಎಕ್ಸಿಷನ್ ರಿಪೇರ್ ಕ್ರಾಸ್-ಕಾಂಪ್ಲಿಮೆಂಟಿಂಗ್ 1) ಚಟುವಟಿಕೆಯೊಂದಿಗಿನ ಗೆಡ್ಡೆಗಳನ್ನು ಹೊಂದಿದ್ದ ರೋಗಿಗಳಿಗೆ ಸೀಮಿತಗೊಳಿಸಲ್ಪಟ್ಟಿತ್ತು.[೧೦೮]
IB ಹಂತದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಹೊಂದಿರುವ ರೋಗಿಗಳಿಗೆ ಸಂಬಂಧಿಸಿದ ಸಹೌಷಧದ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯು ವಿವಾದಾಸ್ಪದವಾಗಿದೆ, ಏಕೆಂದರೆ, ಬದುಕುಳಿಯುವಿಕೆಯ ಪ್ರಯೋಜನವೊಂದನ್ನು ವೈದ್ಯಕೀಯ ಪರೀಕ್ಷಾ-ಪ್ರಯೋಗಗಳು ಸ್ಪಷ್ಟವಾಗಿ ನಿರೂಪಿಸಿಲ್ಲ.[೧೦೯][೧೧೦] ಅಂಶಚ್ಛೇದನ ಮಾಡಬಲ್ಲ, ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದಲ್ಲಿನ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಗೆ-ಮುಂಚಿನ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯ (ಪುನರುಜ್ಜೀವಿತವಾದ-ಸಹೌಷಧದ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ) ಪರೀಕ್ಷಾ-ಪ್ರಯೋಗಗಳು ಅನಿರ್ಣಾಯಕವಾಗಿ ಹೊರಹೊಮ್ಮಿವೆ.[೧೧೧]
ವಿಕಿರಣ ಚಿಕಿತ್ಸೆ
[ಬದಲಾಯಿಸಿ]ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯನ್ನು ಬಹುತೇಕವಾಗಿ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯೊಂದಿಗೆ ಒಟ್ಟಾಗಿ ನೀಡಲಾಗುತ್ತದೆ; ಅಷ್ಟೇ ಅಲ್ಲ, ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಗಾಗಿ ಅರ್ಹರಲ್ಲದವರು ಎನಿಸಿಕೊಂಡಿರುವ, ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮಕ್ಕೆ ಈಡಾಗಿರುವ ರೋಗಿಗಳಲ್ಲಿ ಈ ಚಿಕಿತ್ಸೆಯನ್ನು ರೋಗಪರಿಹಾರಕ ಆಶಯದೊಂದಿಗೆ ಬಳಸಬಹುದು. ಉನ್ನತ ತೀವ್ರತೆಯನ್ನು ಹೊಂದಿರುವ ಈ ಸ್ವರೂಪದ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಗೆ ರೋಗಮೂಲಹಾರಿ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.[೧೧೨] ನಿರಂತರವಾಗಿದ್ದು ಅಧಿಕವಾಗಿ-ಅಂಶೀಕರಿಸಲ್ಪಟ್ಟ ತ್ವರಿತಗೊಳಿಸಿದ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆ (ಕಂಟಿನ್ಯುಯಸ್ ಹೈಪರ್ಫ್ರಾಕ್ಷನೇಟೆಡ್ ಆಕ್ಸಿಲರೇಟೆಡ್ ರೇಡಿಯೋಥೆರಪಿ-CHART) ಎಂಬುದು ಈ ಕೌಶಲದ ಒಂದು ಪರಿಷ್ಕೃತ ರೂಪವಾಗಿದ್ದು, ಈ ಚಿಕಿತ್ಸೆಯಲ್ಲಿ ಉನ್ನತ ಪ್ರಮಾಣದ ಒಂದು ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯನ್ನು ಒಂದು ಅಲ್ಪ ಕಾಲಾವಧಿಯಲ್ಲಿ ನೀಡಲಾಗುತ್ತದೆ.[೧೧೩] ಸಂಭಾವ್ಯವಾಗಿ ವಾಸಿಮಾಡಬಹುದಾದ ಲಕ್ಷಣವನ್ನು ಹೊಂದಿರುವ, ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ ಪ್ರಕರಣಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ, ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯ ಜೊತೆಜೊತೆಗೆ ಎದೆಯ ವಿಕಿರಣದ ಚಿಕಿತ್ಸೆಯನ್ನು ಅನೇಕವೇಳೆ ಶಿಫಾರಸು ಮಾಡಲಾಗುತ್ತದೆ.[೧೧೪] ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ, ರೋಗಪರಿಹಾರಕ ಆಶಯದ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯನ್ನು ಅನುಸರಿಸಿಕೊಂಡು, ಸಹೌಷಧದ ಎದೆಗೂಡಿನ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯನ್ನು ಬಳಕೆ ಮಾಡುವ ಪರಿಪಾಠಕ್ಕೆ ಉತ್ತಮವಾದ ಸಮರ್ಥನೆಯು ಸಿಕ್ಕಿಲ್ಲ ಮತ್ತು ಇದು ವಿವಾದಾಸ್ಪದವಾಗಿದೆ. ಒಂದು ವೇಳೆ ಏನಾದರೂ ಪ್ರಯೋಜನಗಳಿದ್ದರೆ, ಮೀಡಿಯಸ್ಟೀನಲ್ ದುಗ್ಧಗ್ರಂಥಿಗಳಿಗೆ ಹರಡಿಕೊಂಡಿರುವ ಗೆಡ್ಡೆಯನ್ನು ಹೊಂದಿರುವವರಿಗೆ ಮಾತ್ರವೇ ಅದು ಸೀಮಿತವಾಗಿರಬಹುದು.[೧೧೫][೧೧೬]
ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮ ಮತ್ತು ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದಂಥ ಎರಡೂ ಪ್ರಭೇದಗಳ ರೋಗಿಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ, ರೋಗಲಕ್ಷಣದ ಹತೋಟಿಯ (ಉಪಶಾಮಕ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆ) ಪರಿಣಾಮವನ್ನು ನೀಡುವುದಕ್ಕಾಗಿ, ಸಣ್ಣದಾದ ಪ್ರಮಾಣಗಳಲ್ಲಿ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯನ್ನು ಎದೆಗೆ ನೀಡಬಹುದು. ಇತರ ಚಿಕಿತ್ಸೆಗಳಿಗಿಂತ ಭಿನ್ನವಾಗಿ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಊತಕಶಾಸ್ತ್ರೀಯ ರೋಗನಿರ್ಣಯವನ್ನು ದೃಢೀಕರಿಸದೆಯೇ ಉಪಶಾಮಕ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯನ್ನು ನೀಡಲು ಸಾಧ್ಯವಿದೆ.
ಶ್ವಾಸನಾಳಿಕೆಯ ಒಂದು ಕಿರುವಿಭಾಗದ ಮೇಲೆ ಕ್ಯಾನ್ಸರ್ ತನ್ನ ಸೋಂಕನ್ನು ಉಂಟುಮಾಡಿದಾಗ, ಹೃಸ್ವಚಿಕಿತ್ಸೆಯನ್ನು (ಸ್ಥಳೀಕರಿಸಲ್ಪಟ್ಟ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆ) ವಾಯುಮಾರ್ಗದ ಒಳಭಾಗದಲ್ಲಿ ನೇರವಾಗಿ ನೀಡಬಹುದು.[೧೧೭] ಶಸ್ತ್ರಚಿಕಿತ್ಸೆ ಮಾಡಲಾಗದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್, ದೊಡ್ಡ ವಾಯುಮಾರ್ಗವೊಂದರಲ್ಲಿ ಅಡಚಣೆಯನ್ನು ಉಂಟುಮಾಡಿದಾಗ ಇದನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.[೧೧೮]
ಸೀಮಿತ ಹಂತದ ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವನ್ನು ಹೊಂದಿರುವ ರೋಗಿಗಳಿಗೆ, ಸಾಮಾನ್ಯವಾಗಿ ಕಪಾಲದ ರೋಗನಿರೋಧಕ ವಿಕಿರಣ ಪ್ರಭಾವವನ್ನು (ಪ್ರೊಫೈಲ್ಯಾಕ್ಟಿಕ್ ಕ್ರೇನಿಯಲ್ ಇರ್ರೇಡಿಯೇಷನ್-PCI) ನೀಡಲಾಗುತ್ತದೆ. ಇದು ಮಿದುಳಿಗೆ ನೀಡಲಾಗುವ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯ ಒಂದು ಬಗೆಯಾಗಿದ್ದು, ಸ್ಥಾನಾಂತರಣದ ಅಪಾಯವನ್ನು ತಗ್ಗಿಸಲು ಇದನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.[೧೧೯] ತೀರಾ ಇತ್ತೀಚೆಗೆ, ವ್ಯಾಪಕವಾಗಿರುವ ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಹೊಂದಿರುವವರಲ್ಲಿ, PCI ಚಿಕಿತ್ಸೆಯು ಪ್ರಯೋಜನಕಾರಿಯಾಗಿರುವುದು ಕಂಡುಬಂದಿದೆ. ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯ ಒಂದು ಅನುಕ್ರಮವನ್ನು ಅನುಸರಿಸಿದ ನಂತರ ಕ್ಯಾನ್ಸರ್ ಸುಧಾರಣೆಯಾಗಿರುವ ರೋಗಿಗಳಲ್ಲಿ, ಮಿದುಳು ಸ್ಥಾನಾಂತರಣಗಳ ಸಂಚಿತ ಅಪಾಯವನ್ನು ಒಂದು ವರ್ಷದೊಳಗಾಗಿ 40.4%ನಿಂದ 14.6%ನಷ್ಟು ಪ್ರಮಾಣಕ್ಕೆ PCI ತಗ್ಗಿಸುತ್ತದೆ ಎಂಬುದು ಕಂಡುಬಂದಿದೆ.[೧೨೦]
ಗುರಿಮಾಡುವಿಕೆ ಮತ್ತು ಬಿಂಬವನ್ನು ರೂಪಿಸುವಿಕೆಯಲ್ಲಿನ ಇತ್ತೀಚಿನ ಸುಧಾರಣೆಗಳು, ಆರಂಭಿಕ-ಹಂತದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಉಪಚಾರದಲ್ಲಿ ಬಳಸಲಾಗುವ ಕಪಾಲದ ಹೊರಗಣ ಸ್ಟಿರಿಯೋಟ್ಯಾಕ್ಟಿಕ್ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯ ಅಭಿವೃದ್ಧಿಯಾಗುವುದಕ್ಕೆ ಕಾರಣವಾಗಿವೆ. ಈ ಸ್ವರೂಪದ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯಲ್ಲಿ, ಗುರಿಮಾಡುವಿಕೆಯ ಸ್ಟಿರಿಯೋಟ್ಯಾಕ್ಟಿಕ್ ಕೌಶಲಗಳನ್ನು ಬಳಸಿಕೊಂಡು, ಒಂದು ಸಣ್ಣ ಸಂಖ್ಯೆಯ ಅವಧಿಗಳಲ್ಲಿ ಅತ್ಯಂತ ಹೆಚ್ಚಿನ ಪ್ರಮಾಣಗಳಲ್ಲಿ ಔಷಧಿಗಳನ್ನು ನೀಡಲಾಗುತ್ತದೆ. ವೈದ್ಯಕೀಯವಾಗಿ ಹೆಚ್ಚುವರಿಯಿರುವ ರೋಗಲಕ್ಷಣಗಳ ಕಾರಣದಿಂದಾಗಿ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯ ಪರೀಕ್ಷಾರ್ಥಿಗಳಾಗಿರದ ರೋಗಿಗಳಲ್ಲಿ ಇದನ್ನು ಪ್ರಧಾನವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ.[೧೨೧]
ಮಧ್ಯಸ್ಥಿಕೆಯ ವಿಕಿರಣಶೀಲತೆಯ ಶಾಸ್ತ್ರ
[ಬದಲಾಯಿಸಿ]ರೇಡಿಯೋ ಆವೃತ್ತಿಯ ಅಂಗಚ್ಛೇದನವನ್ನು ಪ್ರಸಕ್ತವಾಗಿ, ಶ್ವಾಸನಾಳಜನ್ಯ ಕಾರ್ಸಿನೋಮದ ಚಿಕಿತ್ಸೆಯಲ್ಲಿನ ಒಂದು ತನಿಖಾತ್ಮಕ ಕೌಶಲವಾಗಿ ಪರಿಗಣಿಸಬೇಕಾಗಿದೆ. ಗೆಡ್ಡೆಯ ಜೀವಕೋಶಗಳನ್ನು ಕೊಲ್ಲುವ ಸಲುವಾಗಿ ಗೆಡ್ಡೆಯೊಳಗೆ ಒಂದು ಸಣ್ಣದಾದ ಬಿಸಿ ಶೋಧಕವನ್ನು ತೂರಿಸುವ ಮೂಲಕ ಇದನ್ನು ನೆರವೇರಿಸಲಾಗುತ್ತದೆ.[೧೨೨]
ನಿರ್ದೇಶಿತ ಚಿಕಿತ್ಸೆ
[ಬದಲಾಯಿಸಿ]ಇತ್ತೀಚಿನ ವರ್ಷಗಳಲ್ಲಿ, ಮುಂದುವರಿದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಚಿಕಿತ್ಸೆಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಹಲವಾರು ಆಣ್ವಿಕ ನಿರ್ದೇಶಿತ ಚಿಕಿತ್ಸೆಗಳನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ. ಜೆಫಿಟಿನಿಬ್ (ಇರೆಸ್ಸಾ) ಎಂಬುದು ಇಂಥದೊಂದು ಔಷಧಿಯಾಗಿದ್ದು, ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದ ಅನೇಕ ಪ್ರಕರಣಗಳಲ್ಲಿ ಅಭಿವ್ಯಕ್ತಿಸಲ್ಪಟ್ಟ ಹೊರಚರ್ಮದ ಬೆಳವಣಿಗೆಯ ಅಂಶ ಗ್ರಾಹಿಯ (ಎಪಿಡರ್ಮಲ್ ಗ್ರೋತ್ ಫ್ಯಾಕ್ಟರ್ ರಿಸೆಪ್ಟರ್-EGFR) ಟೈರೋಸಿನ್ ಕೈನೇಸ್ ಕ್ಷೇತ್ರವನ್ನು ಅದು ಗುರಿಯಾಗಿರಿಸಿಕೊಳ್ಳುತ್ತದೆ. ಬದುಕುಳಿಯುವಿಕೆಯ ಅವಧಿಯನ್ನು ಇದು ಹೆಚ್ಚಿಸುತ್ತದೆ ಎಂಬ ರೀತಿಯಲ್ಲಿ ಇದು ಅಭಿವ್ಯಕ್ತಿಸಲ್ಪಡಲಿಲ್ಲವಾದರೂ, ಮಹಿಳೆಯರು, ಏಷ್ಯನ್ನರು, ಧೂಮಪಾನಿಗಳಲ್ಲದವರು, ಮತ್ತು ಶ್ವಾಸನಾಳದ ಸೂಕ್ಷ್ಮಕವಲಿನ ಕಿರುಗುಳಿಯ ಕಾರ್ಸಿನೋಮವನ್ನು ಹೊಂದಿರುವವರು, ಜೆಫಿಟಿನಿಬ್ನಿಂದ ಹೆಚ್ಚಿನ ಪ್ರಯೋಜನವನ್ನು ಪಡೆಯುವಂತೆ ಕಾಣಿಸುತ್ತದೆ.[೨೧][೧೨೩]
ಮತ್ತೊಂದು ಟೈರೋಸಿನ್ ಕೈನೇಸ್ ಪ್ರತಿಬಂಧಕವಾಗಿರುವ ಎರ್ಲೋಟಿನಿಬ್ (ಟಾರ್ಸೆವಾ), ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ರೋಗಿಗಳಲ್ಲಿ[೧೨೪] ಬದುಕುಳಿಯುವಿಕೆಯ ಅವಧಿಯನ್ನು ಹೆಚ್ಚಿಸುತ್ತದೆ ಎಂಬುದಾಗಿ ತೋರಿಸಲ್ಪಟ್ಟಿದೆ ಮತ್ತು ಮುಂದುವರಿದ ಹಂತದ ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮದ ಎರಡನೇ-ಹಂತದ ಚಿಕಿತ್ಸೆಗೆ ಸಂಬಂಧಿಸಿದಂತೆ FDAಯಿಂದ ಇತ್ತೀಚೆಗಷ್ಟೇ ಅಂಗೀಕರಿಸಲ್ಪಟ್ಟಿದೆ. ಜೆಫಿಟಿನಿಬ್ನ್ನು ಹೋಲುವ ರೀತಿಯಲ್ಲಿಯೇ, ಇದೂ ಸಹ ಮಹಿಳೆಯರು, ಏಷ್ಯನ್ನರು, ಧೂಮಪಾನಿಗಳಲ್ಲದವರು, ಮತ್ತು ಶ್ವಾಸನಾಳದ ಸೂಕ್ಷ್ಮಕವಲಿನ ಕಿರುಗುಳಿಯ ಕಾರ್ಸಿನೋಮವನ್ನು ಹೊಂದಿರುವವರಲ್ಲಿ ಅತ್ಯುತ್ತಮವಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತದೆ ಎಂಬುದು ಕಂಡುಬಂದಿದೆ; ಅದರಲ್ಲೂ ನಿರ್ದಿಷ್ಟವಾಗಿ, EGFRನಲ್ಲಿ ನಿರ್ದಿಷ್ಟ ಹಠಾತ್ ಬದಲಾವಣೆಗಳನ್ನು ಹೊಂದಿರುವವರಲ್ಲಿ ಇದರ ಪ್ರಭಾವ ಹೆಚ್ಚು.[೧೨೩]
ರಕ್ತನಾಳದ-ಜನನದ ಪ್ರತಿಬಂಧಕವಾಗಿರುವ ಬೆವಾಸಿಜುಮಾಬ್, (ಪ್ಯಾಕ್ಲಿಟ್ಯಾಕ್ಸೆಲ್ ಮತ್ತು ಕಾರ್ಬೋಪ್ಲೇಟಿನ್ ಜೊತೆಗಿನ ಸಂಯೋಜನೆಯಲ್ಲಿ), ಮುಂದುವರಿದ ಹಂತದ ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವನ್ನು ಹೊಂದಿರುವ ರೋಗಿಗಳ ಬದುಕುಳಿಯುವಿಕೆಯ ಅವಧಿಯನ್ನು ಸುಧಾರಿಸುತ್ತದೆ.[೧೨೫] ಆದಾಗ್ಯೂ, ಇದು ಶ್ವಾಸಕೋಶದ ರಕ್ತಸ್ರಾವದ ಅಪಾಯವನ್ನು ಹೆಚ್ಚಿಸುತ್ತದೆ, ಅದರಲ್ಲೂ ನಿರ್ದಿಷ್ಟವಾಗಿ ಪೊರೆಯುಕ್ತ ಜೀವಕೋಶ ಕಾರ್ಸಿನೋಮವನ್ನು ಹೊಂದಿರುವ ರೋಗಿಗಳಲ್ಲಿ ಈ ಅಪಾಯವು ಹೆಚ್ಚಾಗಿ ಕಂಡುಬರುತ್ತದೆ.
ಕೋಶವಿಷದ ಔಷಧಿಗಳು,[೧೨೬] ಫಾರ್ಮ್ಯಾಕೋಜೆನೆಟಿಕ್ಸ್[೧೨೭] ಮತ್ತು ನಿರ್ದೇಶಿತ ಔಷಧಿ ವಿನ್ಯಾಸ[೧೨೮] ದಲ್ಲಿನ ಪ್ರಗತಿಗಳು ಭರವಸೆಯನ್ನು ತೋರಿಸಿವೆ. ಹಲವಾರು ಉದ್ದೇಶಿತ ಕಾರಕವಸ್ತುಗಳು ವೈದ್ಯಕೀಯ ಸಂಶೋಧನೆಯ ಆರಂಭಿಕ ಹಂತಗಳಲ್ಲಿವೆ. ಅವುಗಳೆಂದರೆ: ಸೈಕ್ಲೋ-ಆಕ್ಸಿಜನೇಸ್-2 ಪ್ರತಿಬಂಧಕಗಳು,[೧೨೯] ಅಪೋಪ್ಟೋಸಿಸ್ ಪ್ರವರ್ತಕ ಎಕ್ಸಿಸುಲಿಂಡ್,[೧೩೦] ಪ್ರೋಟಿಯಾಸೋಮ್ ಪ್ರತಿಬಂಧಕಗಳು,[೧೩೧] ಬೆಕ್ಸರೊಟೀನ್,[೧೩೨] ಹೊರಚರ್ಮದ ಬೆಳವಣಿಗೆಯ ಅಂಶದ ಗ್ರಾಹಿ ಪ್ರತಿಬಂಧಕವಾದ ಸೆಟುಕ್ಸಿಮ್ಯಾಬ್,[೧೩೩] ಮತ್ತು ಲಸಿಕೆಗಳು.[೧೩೪] ಸಂಶೋಧನೆಯ ಭವಿಷ್ಯದ ಕ್ಷೇತ್ರಗಳಲ್ಲಿ ಇವು ಸೇರಿವೆ: ರಾಸ್ ಮೂಲ-ಗ್ರಂಥಿಜನಕ ಜೀನು ಪ್ರತಿಬಂಧ, ಫಾಸ್ಫೋಇನೋಸಿಟೈಡ್ 3-ಕೈನೇಸ್ ಪ್ರತಿಬಂಧ, ಹಿಸ್ಟೋನ್ ಡೀಅಸಿಟೈಲೇಸ್ ಪ್ರತಿಬಂಧ, ಮತ್ತು ಗೆಡ್ಡೆ ನಿರೋಧಕ ಜೀನು ಬದಲಾವಣೆ.[೧೩೫]
ವ್ಯಾಧಿಯ ಮುನ್ನರಿವು
[ಬದಲಾಯಿಸಿ]ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಲ್ಲಿನ ಪೂರ್ವಸೂಚಕ ಅಂಶಗಳಲ್ಲಿ ಇವು ಸೇರಿವೆ: ಶ್ವಾಸಕೋಶದ ರೋಗಲಕ್ಷಣಗಳ ಹಾಜರಿ ಅಥವಾ ಗೈರುಹಾಜರಿ, ಗೆಡ್ಡೆಯ ಗಾತ್ರ, ಜೀವಕೋಶದ ಬಗೆ (ಊತಕಶಾಸ್ತ್ರ), ಹರಡಿಕೆಯ ಮಟ್ಟ (ಹಂತ) ಮತ್ತು ಅನೇಕ ದುಗ್ಧಗ್ರಂಥಿಗಳಿಗೆ ಆಗುವ ಸ್ಥಾನಾಂತರಣಗಳು, ಹಾಗೂ ನಾಳೀಯ ಅತಿಕ್ರಮಣ. ಶಸ್ತ್ರಚಿಕಿತ್ಸೆ ಮಾಡಲಾಗದ ಕಾಯಿಲೆಯನ್ನು ಹೊಂದಿರುವ ರೋಗಿಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ, ಕಳಪೆ ಕಾರ್ಯಕ್ಷಮತೆಯ ಸ್ಥಿತಿ ಹಾಗೂ 10%ಗೂ ಹೆಚ್ಚಿನ ತೂಕದ ನಷ್ಟ ಇವುಗಳು ಕಾಯಿಲೆಯ ಮುನ್ನರಿವಿನ ಮೇಲೆ ಪ್ರತಿಕೂಲವಾದ ಪ್ರಭಾವ ಬೀರುತ್ತವೆ.[೧೩೬] ಸಣ್ಣ-ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಲ್ಲಿನ ಪೂರ್ವಸೂಚಕ ಅಂಶಗಳಲ್ಲಿ ಇವು ಸೇರಿವೆ: ಕಾರ್ಯಕ್ಷಮತೆಯ ಸ್ಥಿತಿ, ಲಿಂಗ, ಕಾಯಿಲೆಯ ಹಂತ, ರೋಗನಿರ್ಣಯದ ಸಮಯದಲ್ಲಿನ ಮಧ್ಯಭಾಗದ ನರವ್ಯೂಹ ಅಥವಾ ಪಿತ್ತಜನಕಾಂಗದ ಒಳಗೊಳ್ಳುವಿಕೆ.[೧೩೭]
ಸಣ್ಣದಲ್ಲದ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮಕ್ಕೆ (NSCLC) ಸಂಬಂಧಿಸಿದಂತೆ, ಕಾಯಿಲೆಯ ಮುನ್ನರಿವು ಸಾಮಾನ್ಯವಾಗಿ ಕಳಪೆಯದಾಗಿರುತ್ತದೆ. IA ಹಂತದ ಕಾಯಿಲೆಯ ಸಂಪೂರ್ಣ ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯ ಅಂಶಛೇದನವನ್ನು ಅನುಸರಿಸಿಕೊಂಡು ಬರುವ, ಐದು-ವರ್ಷ ಅವಧಿಯ ಬದುಕುಳಿಯುವಿಕೆಯು 67%ನಷ್ಟಿರುತ್ತದೆ. IB ಹಂತದ ಕಾಯಿಲೆಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಹೇಳುವುದಾದರೆ, ಐದು-ವರ್ಷ ಅವಧಿಯ ಬದುಕುಳಿಯುವಿಕೆಯು 57%ನಷ್ಟಿರುತ್ತದೆ.[೧೩೮] IV ಹಂತದ NSCLCಯೊಂದಿಗಿನ ರೋಗಿಗಳ ಐದು-ವರ್ಷ ಅವಧಿಯ ಬದುಕುಳಿಯುವಿಕೆಯ ಪ್ರಮಾಣವು ಸುಮಾರು 1%ನಷ್ಟಿರುತ್ತದೆ.[೪]
ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ, ಕಾಯಿಲೆಯ ಮುನ್ನರಿವೂ ಸಹ ಸಾಮಾನ್ಯವಾಗಿ ಕಳಪೆಯಾಗಿರುತ್ತದೆ. SCLCಯೊಂದಿಗಿನ ರೋಗಿಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಒಟ್ಟಾರೆ ಐದು-ವರ್ಷ ಅವಧಿಯ ಬದುಕುಳಿಯುವಿಕೆಯು ಸುಮಾರು 5%ನಷ್ಟಿರುತ್ತದೆ.[೨] ವ್ಯಾಪಕ-ಹಂತದ SCLCಯೊಂದಿಗಿನ ರೋಗಿಗಳು 1%ಗೂ ಕಡಿಮೆಯಿರುವ ಐದು-ವರ್ಷ ಬದುಕುಳಿಯುವಿಕೆಯ ಒಂದು ಸರಾಸರಿ ಅವಧಿಯನ್ನು ಹೊಂದಿರುತ್ತಾರೆ. ಸೀಮಿತ-ಹಂತದ ಕಾಯಿಲೆಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಬದುಕುಳಿಯುವಿಕೆಯ ಮಧ್ಯಸ್ಥ ಸಮಯವು 20 ತಿಂಗಳುಗಳಷ್ಟಿರುತ್ತದೆ ಹಾಗೂ 20%ನಷ್ಟಿರುವ ಐದು-ವರ್ಷ ಬದುಕುಳಿಯುವಿಕೆಯ ಒಂದು ಅವಧಿಯನ್ನು ಅದು ಹೊಂದಿರುತ್ತದೆ.[೪]
ರಾಷ್ಟ್ರೀಯ ಕ್ಯಾನ್ಸರ್ ಸಂಸ್ಥೆಯ ವತಿಯಿಂದ ಒದಗಿಸಲ್ಪಟ್ಟ ದತ್ತಾಂಶದ ಅನುಸಾರ, ಅಮೆರಿಕಾ ಸಂಯುಕ್ತ ಸಂಸ್ಥಾನಗಳಲ್ಲಿ ಕಂಡುಬರುವ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಪ್ರಕರಣಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತಿರುವ ಸಾವಿನ ಮಧ್ಯಸ್ಥ ವಯಸ್ಸು 70 ವರ್ಷಗಳಷ್ಟಿದೆ, ಮತ್ತು ಮಧ್ಯಸ್ಥ ವಯಸ್ಸು 71 ವರ್ಷಗಳಷ್ಟಿದೆ.[೧೩೯]
ಸೋಂಕುಶಾಸ್ತ್ರ
[ಬದಲಾಯಿಸಿ]

ವ್ಯಾಪ್ತಿ ಮತ್ತು ಮರಣ-ಪ್ರಮಾಣ ಈ ಎರಡೂ ದೃಷ್ಟಿಯಲ್ಲಿಯೂ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ವಿಶ್ವಾದ್ಯಂತದ ಅತ್ಯಂತ ಸಾಮಾನ್ಯ ಕ್ಯಾನ್ಸರ್ ಎನಿಸಿಕೊಂಡಿದ್ದು (ಪ್ರತಿ ವರ್ಷವೂ 1.35 ದಶಲಕ್ಷ ಹೊಸ ಪ್ರಕರಣಗಳು ಮತ್ತು 1.18 ದಶಲಕ್ಷ ಸಾವುಗಳು), ಯುರೋಪ್ ಮತ್ತು ಉತ್ತರ ಅಮೆರಿಕಾಗಳಲ್ಲಿ ಇದರ ಅತಿಹೆಚ್ಚಿನ ಪ್ರಕರಣಗಳು ಕಂಡುಬರುತ್ತವೆ.[೧೪೧] ಧೂಮಪಾನದ ಒಂದು ಇತಿಹಾಸವನ್ನು ಹೊಂದಿರುವ ಐವತ್ತಕ್ಕೂ ಹೆಚ್ಚಿನ ವಯೋಮಾನದ ಜನಸಂಖ್ಯಾ ವಲಯವು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಈಡಾಗುವ ಸಾಧ್ಯತೆ ಹೆಚ್ಚು. ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್, ಬಹುತೇಕ ಪಾಶ್ಚಾತ್ಯ ದೇಶಗಳಲ್ಲಿ ಸಂಭವಿಸುವ ಕ್ಯಾನ್ಸರ್ನ ಎರಡನೇ ಅತ್ಯಂತ ಸಾಮಾನ್ಯ ಸ್ವರೂಪ ಎನಿಸಿಕೊಂಡಿದೆ, ಮತ್ತು ಇದು ಸಾವನ್ನು ಉಂಟುಮಾಡುವಲ್ಲಿನ ಕ್ಯಾನ್ಸರ್-ಸಂಬಂಧಿತ ಅಗ್ರಗಣ್ಯ ಕಾರಣವಾಗಿದೆ. 20 ವರ್ಷಗಳಿಗೂ ಹೆಚ್ಚಿನ ಅವಧಿಯಿಂದ ಇಳಿಯಲು ಶುರುಮಾಡಿರುವ, ಪುರುಷರಲ್ಲಿ ಕಂಡುಬರುವ ಮರ್ತ್ಯತೆಯ ಪ್ರಮಾಣಕ್ಕೆ ಪ್ರತಿಯಾಗಿ, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಿಂದ ಸಾಯುತ್ತಿರುವ ಮಹಿಳೆಯರ ಪ್ರಮಾಣವು ಕಳೆದ ದಶಕಗಳಿಂದಲೂ ಏರುತ್ತಲೇ ಇದ್ದು, ಕೇವಲ ಇತ್ತೀಚೆಗಷ್ಟೇ ಅದು ಸ್ಥಿರಗೊಳ್ಳಲು ಶುರುವಾಗುತ್ತಿದೆ.[೧೪೨] "ತಂಬಾಕು ಉದ್ಯಮ"ದ ವಿಕಸನವು ಧೂಮಪಾನ ಸಂಸ್ಕೃತಿಯಲ್ಲಿ ಒಂದು ಗಣನೀಯ ಪಾತ್ರವನ್ನು ವಹಿಸುತ್ತದೆ.[೧೪೩] 1970ರ ದಶಕದಿಂದಲೂ, ತಂಬಾಕು ಕಂಪನಿಗಳು ತಮ್ಮ ಉತ್ಪನ್ನವನ್ನು, ಅದರಲ್ಲೂ ವಿಶೇಷವಾಗಿ "ಲಘು" ಮತ್ತು "ಕಡಿಮೆ-ಟಾರಿನ ಅಂಶವುಳ್ಳ" ಸಿಗರೇಟುಗಳನ್ನು, ಮಹಿಳೆಯರು ಮತ್ತು ಹುಡುಗಿಯರ ವಲಯಕ್ಕೆ ಮಾರಾಟ ಮಾಡುವೆಡೆಗೆ ತಮ್ಮ ಪ್ರಯತ್ನಗಳನ್ನು ಕೇಂದ್ರೀಕರಿಸಿಕೊಂಡು ಬಂದಿವೆ.[೧೪೪] ಜೀವನಪರ್ಯಂತ ಧೂಮಪಾನಿಗಳಾಗಿರದಿದ್ದವರ ಪೈಕಿ, ಮಹಿಳೆಯರಿಗೆ ಹೋಲಿಸಿದಾಗ ಪುರುಷರು ಉನ್ನತವಾದ, ವಯೋಮಾನವನ್ನು-ಪ್ರಮಾಣಕವಾಗಿಸಿದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಸಾವಿನ ಪ್ರಕರಣಗಳನ್ನು ಹೊಂದಿದ್ದಾರೆ.
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಎಲ್ಲಾ ಪ್ರಕರಣಗಳು ಧೂಮಪಾನದ ಕಾರಣದಿಂದಾಗಿಯೇ ಹುಟ್ಟಿಕೊಳ್ಳುವುದಿಲ್ಲವಾದರೂ, ನಿಷ್ಕ್ರಿಯ ಧೂಮಪಾನದ ಪಾತ್ರವು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಸಂಬಂಧಿಸಿದಂತಿರುವ ಒಂದು ಅಪಾಯಕಾರಿ ಅಂಶವಾಗಿ ಗುರುತಿಸಲ್ಪಡುತ್ತಿರುವ ಸಂದರ್ಭಗಳು ಹೆಚ್ಚಾಗುತ್ತಲೇ ಇವೆ; ಇತರರ ತಂಬಾಕು ಹೊಗೆಗೆ ಒಡ್ಡಿಕೊಳ್ಳುವುದನ್ನು ಬಯಸದ ಧೂಮಪಾನಿಗಳಲ್ಲದವರ ಹಿತರಕ್ಷಣೆ ಮಾಡಲೆಂದು ಅಥವಾ ಅಂಥದೊಂದು ಸನ್ನಿವೇಶವು ಎದುರಾಗುವುದನ್ನು ತಗ್ಗಿಸಲೆಂದು ಕಾರ್ಯನೀತಿಯ ಮಧ್ಯಸ್ಥಿಕೆಗಳು ಜಾರಿಯಾಗುವುದಕ್ಕೆ ಇವು ಕಾರಣವಾಗಿವೆ ಎನ್ನಬಹುದು. ವಾಹನಗಳು, ಕಾರ್ಖಾನೆಗಳು, ಮತ್ತು ವಿದ್ಯುತ್ ಸ್ಥಾವರಗಳಿಂದ ಹೊರಹೊಮ್ಮುವ ಉತ್ಸರ್ಜನಗಳೂ ಸಹ ಸಮರ್ಥ ಅಪಾಯಗಳನ್ನು ಒಡ್ಡುತ್ತವೆ.[೧೦][೧೨][೧೪೫]
ಪೂರ್ವದ ಯುರೋಪ್ನಲ್ಲಿ, ಪುರುಷರಲ್ಲಿ ಕಂಡುಬರುವ ಅತಿಹೆಚ್ಚಿನ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್-ಸಂಬಂಧಿ ಮರಣ ಪ್ರಮಾಣವು ಕಂಡುಬಂದರೆ, ಉತ್ತರದ ಯುರೋಪ್ ಮತ್ತು U.S.ಗಳಲ್ಲಿ ಮಹಿಳೆಯರ ವಲಯದಲ್ಲಿ ಅತಿಹೆಚ್ಚಿನ ಮರಣ ಪ್ರಮಾಣವು ಕಂಡುಬರುತ್ತದೆ. ಅಭಿವೃದ್ಧಿಶೀಲ ದೇಶಗಳಲ್ಲಿ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ವ್ಯಾಪ್ತಿಯು ಪ್ರಸಕ್ತವಾಗಿ ವಿರಳವಾಗಿದೆ.[೧೪೬] ಅಭಿವೃದ್ಧಿಶೀಲ ದೇಶಗಳಲ್ಲಿ ಧೂಮಪಾನದ ಪ್ರಮಾಣವು ಹೆಚ್ಚಳವಾಗುತ್ತಿರುವುದರಿಂದ, ಮುಂದಿನ ಕೆಲವೇ ವರ್ಷಗಳಲ್ಲಿ ಕ್ಯಾನ್ಸರ್ ವ್ಯಾಪ್ತಿಯು ಹೆಚ್ಚಾಗಬಹುದು, ಅದರಲ್ಲೂ ಗಮನಾರ್ಹವಾಗಿ ಚೀನಾ[೧೪೭] ಮತ್ತು ಭಾರತ ದೇಶಗಳಲ್ಲಿ ಇದರ ಸಾಧ್ಯತೆ ಹೆಚ್ಚು ಎಂದು ನಿರೀಕ್ಷಿಸಲಾಗಿದೆ.[೧೪೮]
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ವ್ಯಾಪ್ತಿಯು (ದೇಶದ ಆಧಾರದಲ್ಲಿ) ಬಿಸಿಲು ಮತ್ತು UVBಗೆ ಒಡ್ಡಿಕೊಳ್ಳುವ ಪ್ರಕ್ರಿಯೆಯೊಂದಿಗೆ ಒಂದು ವಿಲೋಮ ಸ್ವರೂಪದ ಪರಸ್ಪರ ಸಂಬಂಧವನ್ನು ಹೊಂದಿದೆ. D ಜೀವಸತ್ವದ (ಬಿಸಿಲಿಗೆ ಒಡ್ಡಿಕೊಳ್ಳುವುದರಿಂದಾಗಿ ಚರ್ಮದಲ್ಲಿ ಇದು ಉತ್ಪಾದಿಸಲ್ಪಡುತ್ತದೆ) ಒಂದು ನಿರೋಧಕ ಪರಿಣಾಮವು ಒಂದು ಸಂಭಾವ್ಯ ವಿವರಣೆಯಾಗಿದೆ .[೧೪೯]
1950ರ ದಶಕದಿಂದಲೂ, ಶ್ವಾಸಕೋಶದ ಅಡಿನೊಕಾರ್ಸಿನೋಮದ ವ್ಯಾಪ್ತಿಯು, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ಇತರ ಬಗೆಗಳಿಗೆ ತುಲನಾತ್ಮಕವಾಗಿರುವ ರೀತಿಯಲ್ಲಿ ಹೆಚ್ಚಳಗೊಳ್ಳಲು ಪ್ರಾರಂಭಿಸಿತು.[೧೫೦] ಫಿಲ್ಟರ್ ಸಿಗರೇಟುಗಳ ಪರಿಚಯವು ಇದಕ್ಕೆ ಭಾಗಶಃ ಕಾರಣವಾಗಿದೆ. ಫಿಲ್ಟರ್ಗಳ ಬಳಕೆಯು ತಂಬಾಕು ಸೇದುವಿಕೆಯಲ್ಲಿರುವ ದೊಡ್ಡದಾದ ಕಣಗಳನ್ನು ತೆಗೆದುಹಾಕುವುದರಿಂದ, ದೊಡ್ಡದಾದ ವಾಯುಮಾರ್ಗಗಳಲ್ಲಿ ಅವು ಸಂಚಯನಗೊಳ್ಳುವುದನ್ನು ತಗ್ಗಿಸಿದಂತಾಗುತ್ತದೆ. ಆದಾಗ್ಯೂ, ಅದೇ ಪ್ರಮಾಣದ ನಿಕೋಟಿನ್ನ್ನು ಸ್ವೀಕರಿಸುವುದಕ್ಕಾಗಿ ಧೂಮಪಾನಿಯು ಹೆಚ್ಚು ಆಳವಾಗಿ ಹೊಗೆಯನ್ನು ಒಳಗೆಳೆದುಕೊಳ್ಳಬೇಕಾಗುತ್ತದೆಯಾದ್ದರಿಂದ, ಸಣ್ಣ ವಾಯುಮಾರ್ಗಗಳಲ್ಲಿ ಕಣ ಸಂಚಯನದ ಪ್ರಮಾಣವು ಹೆಚ್ಚಾಗಿ ಅಡಿನೊಕಾರ್ಸಿನೋಮವು ಹುಟ್ಟಿಕೊಳ್ಳಲು ಪ್ರಚೋದನೆ ಸಿಕ್ಕಂತಾಗುತ್ತದೆ.[೧೫೧] 1999ರಿಂದಲೂ, U.S.ನಲ್ಲಿನ ಶ್ವಾಸಕೋಶದ ಅಡಿನೊಕಾರ್ಸಿನೋಮದ ವ್ಯಾಪ್ತಿಯು ಕುಸಿದಿದೆ. ಪರಿಸರೀಯ ವಾಯುಮಾಲಿನ್ಯದಲ್ಲಿನ ಕಡಿತವು ಇದಕ್ಕೆ ಕಾರಣವಾಗಿರಬಹುದು.[೧೫೦] ಆದಾಗ್ಯೂ, ಭಾರತದಂಥ ಕೆಲವೊಂದು ಅಭಿವೃದ್ಧಿಶೀಲ ದೇಶಗಳಲ್ಲಿ, ಸೋಂಕುಶಾಸ್ತ್ರದಲ್ಲಿ ಒಂದಷ್ಟು ಬದಲಾವಣೆಯಾಗಿದೆ ಮತ್ತು ಪೊರೆಯುಕ್ತ ಜೀವಕೋಶದ ಕಾರ್ಸಿನೋಮವು ಪ್ರಬಲವಾದ ಊತಕಶಾಸ್ತ್ರೀಯ ಬಗೆಯಾಗಿ ಮುಂದುವರಿಯುತ್ತಿದೆ.[೧೫೨][೧೫೩][೧೫೪] ಜನಸಮುದಾಯದಲ್ಲಿ ತಂಬಾಕು ಸೇದುವಿಕೆಯ ಬಗೆಯಲ್ಲಿ ಬದಲಾವಣೆಯಿಲ್ಲದಿರುವುದು ಅಥವಾ ತಂಬಾಕು ಸೇವನೆಯ ಮಾದರಿಯು ಸಂಭಾವ್ಯ ಕಾರಣಗಳಲ್ಲಿ ಒಂದಾಗಿರಬಹುದು.
ಇತಿಹಾಸ
[ಬದಲಾಯಿಸಿ]ಸಿಗರೇಟು ಸೇದುವಿಕೆಯು ಹುಟ್ಟಿಕೊಳ್ಳುವುದಕ್ಕೂ ಮುಂಚೆ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ವಿರಳವಾಗಿತ್ತು; 1761ರವರೆಗೂ ಇದನ್ನೊಂದು ವಿಶಿಷ್ಟ ಕಾಯಿಲೆಯಾಗಿ ಗುರುತಿಸಿರಲಿಲ್ಲ.[೧೫೫] ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ವಿಭಿನ್ನ ಮಗ್ಗುಲುಗಳನ್ನು ಮುಂದೊಮ್ಮೆ 1810ರಲ್ಲಿ ವಿವರಿಸಲಾಯಿತು.[೧೫೬] 1878ರಲ್ಲಿ ಕೈಗೊಳ್ಳಲಾದ ಶವಪರೀಕ್ಷೆಯ ಸಂದರ್ಭದಲ್ಲಿ, ಎಲ್ಲಾ ಕ್ಯಾನ್ಸರ್ಗಳ ಪೈಕಿ ಶ್ವಾಸಕೋಶದ ಪ್ರಾಣಾಂತಕ ಗೆಡ್ಡೆಗಳ ಪಾಲು ಕೇವಲ 1%ನಷ್ಟಿತ್ತು; ಆದರೆ 1900ರ ದಶಕದ ಆರಂಭದ ಹೊತ್ತಿಗೆ ಈ ಪ್ರಮಾಣವು 10–15%ನಷ್ಟಕ್ಕೆ ಏರಿತ್ತು.[೧೫೭] 1912ರಲ್ಲಿ[೧೫೮] ವಿಶ್ವಾದ್ಯಂತ ವೈದ್ಯಕೀಯ ಸಾಹಿತ್ಯದಲ್ಲಿ ದಾಖಲಿಸಲ್ಪಟ್ಟ ಪ್ರಕರಣದ ವರದಿಗಳು ಕೇವಲ 374ರಷ್ಟು ಇತ್ತಾದರೂ, ಶವಪರೀಕ್ಷೆಗಳ ಒಂದು ಅವಲೋಕನವು ತೋರಿಸಿದ ಅನುಸಾರ, 1852ರಲ್ಲಿ 0.3%ನಷ್ಟಿದ್ದ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ವ್ಯಾಪ್ತಿಯು 1952ರ ವೇಳೆಗೆ 5.66%ಗೆ ಏರಿತ್ತು.[೧೫೯] 1929ರಲ್ಲಿ ಜರ್ಮನಿಯಲ್ಲಿ, ಫ್ರಿಟ್ಜ್ ಲಿಕಿಂಟ್ ಎಂಬ ವೈದ್ಯನು ಧೂಮಪಾನ ಮತ್ತು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್[೧೫೭] ನಡುವಿನ ಕೊಂಡಿಯನ್ನು ಗುರುತಿಸಿದ; ಇದು ಒಂದು ಆಕ್ರಮಣಶೀಲವಾದ ಧೂಮಪಾನ ವಿರೋಧಿ ಪ್ರಚಾರಾಂದೋಲನಕ್ಕೆ ಕಾರಣವಾಯಿತು.[೧೬೦] 1950ರ ದಶಕದಲ್ಲಿ ಪ್ರಕಟಿಸಲ್ಪಟ್ಟ ಬ್ರಿಟಿಷ್ ಡಾಕ್ಟರ್ಸ್ ಸ್ಟಡಿ ಎಂಬ ಕೃತಿಯು, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಮತ್ತು ಧೂಮಪಾನದ ನಡುವಿನ ಕೊಂಡಿಯ ಕುರಿತು ವಿವರಿಸುವ ಸೋಂಕುಶಾಸ್ತ್ರದ ಮೊದಲ ಬಲವಾದ ಪುರಾವೆಯಾಗಿತ್ತು.[೧೬೧] ಇದರ ಪರಿಣಾಮವಾಗಿ, 1964ರಲ್ಲಿ ಅಮೆರಿಕಾ ಸಂಯುಕ್ತ ಸಂಸ್ಥಾನಗಳ ಪ್ರಧಾನ ವೈದ್ಯಾಧಿಕಾರಿಯು, ಧೂಮಪಾನಿಗಳು ಧೂಮಪಾನವನ್ನು ನಿಲ್ಲಿಸತಕ್ಕದ್ದು ಎಂಬುದಾಗಿ ಶಿಫಾರಸು ಮಾಡಿದ.[೧೬೨]
ರೇಡಾನ್ ಅನಿಲದ ಜೊತೆಗಿನ ಸಂಬಂಧವನ್ನು ಸ್ಯಾಕ್ಸನಿಯ ಸ್ಕ್ನೀಬರ್ಗ್ ಸಮೀಪದಲ್ಲಿರುವ ಅದಿರು ಪರ್ವತಗಳಲ್ಲಿ ಕೆಲಸಮಾಡುವ ಗಣಿಗಾರರಲ್ಲಿ ಮೊದಲ ಗುರುತಿಸಲಾಯಿತು. 1470ರಿಂದಲೂ ಅಲ್ಲಿ ಬೆಳ್ಳಿಯನ್ನು ಗಣಿಗಾರಿಕೆ ಮಾಡಿ ತೆಗೆಯಲಾಗುತ್ತಿತ್ತು. ಈ ಗಣಿಗಳು ಯುರೇನಿಯಂನ್ನು ಸಮೃದ್ಧವಾಗಿ ಹೊಂದಿವೆ; ಅದರ ಜೊತೆಗೂಡಿಕೊಂಡಿರುವ ರೇಡಿಯಂ ಹಾಗೂ ರೇಡಾನ್ ಅನಿಲವು ಇದಕ್ಕೆ ಕಾರಣ. ಇಲ್ಲಿನ ಗಣಿಗಾರರಲ್ಲಿ ಒಂದು ವಿಷಮ ಪ್ರಮಾಣದ ಮೊತ್ತದ ಶ್ವಾಸಕೋಶ ಕಾಯಿಲೆಯು ಕಂಡುಬಂದಿತು; ಅಂತಿಮವಾಗಿ ಇದು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಎಂಬುದಾಗಿ 1870ರ ದಶಕದಲ್ಲಿ ಗುರುತಿಸಲ್ಪಟ್ಟಿತು. ಒಂದು ಅಂದಾಜಿನ ಪ್ರಕಾರ ಹಿಂದಿನ ಗಣಿಗಾರರ ಪೈಕಿ 75%ನಷ್ಟು ಮಂದಿ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನಿಂದ ಸತ್ತರು.[೧೬೩] ಈ ಪತ್ತೆಹಚ್ಚುವಿಕೆಯ ಹೊರತಾಗಿಯೂ, ಯುರೇನಿಯಂಗಾಗಿ USSR ವತಿಯಿಂದ ಬಂದ ಬೇಡಿಕೆಯ ಕಾರಣದಿಂದಾಗಿ 1950ರ ದಶಕದವರೆಗೂ ಗಣಿಗಾರಿಕೆಯು ಮುಂದುವರಿಯಿತು.[೧೬೪]
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ಗೆ ಸಂಬಂಧಿಸಿದ ಮೊದಲ ಯಶಸ್ವೀ ಶ್ವಾಸಕೋಶ ಛೇದನೆಯನ್ನು 1933ರಲ್ಲಿ ನಿರ್ವಹಿಸಲಾಯಿತು.[೧೬೫] ಉಪಶಾಮಕವಾಗಿರುವ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯನ್ನು 1940ರ ದಶಕದಿಂದಲೂ ಬಳಸಿಕೊಂಡು ಬರಲಾಗಿದೆ.[೧೬೬] ಆರಂಭದಲ್ಲಿ, 1950ರ ದಶಕದಲ್ಲಿ ಬಳಸಲಾದ ರೋಗಮೂಲಹಾರಿ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯು, ದೊಡ್ಡದಾದ ವಿಕಿರಣ ಚಿಕಿತ್ಸಾ ಪ್ರಮಾಣಗಳನ್ನು ಬಳಸುವಲ್ಲಿನ ಒಂದು ಪ್ರಯತ್ನವಾಗಿತ್ತು; ತುಲನಾತ್ಮಕವಾಗಿ ಆರಂಭಿಕ ಹಂತದಲ್ಲಿರುವ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ಹೊಂದಿದ್ದರೂ, ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಅನ್ಯಥಾ ಸಮರ್ಥರಲ್ಲದ ರೋಗಿಗಳಲ್ಲಿ ಈ ಚಿಕಿತ್ಸೆಯನ್ನು ಬಳಸಲಾಗುತ್ತಿತ್ತು.[೧೬೭] 1997ರಲ್ಲಿ, ನಿರಂತರವಾದ ಅಧಿಕವಾಗಿ-ಅಂಶೀಕರಿಸಲ್ಪಟ್ಟ ತ್ವರಿತಗೊಳಿಸಿದ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಯು (ಕಂಟಿನ್ಯುಯಸ್ ಹೈಪರ್ಫ್ರಾಕ್ಷನೇಟೆಡ್ ಆಕ್ಸಿಲರೇಟೆಡ್ ರೇಡಿಯೋಥೆರಪಿ-CHART), ಸಾಂಪ್ರದಾಯಿಕ ರೋಗಮೂಲಹಾರಿ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಗಿಂತ ಉತ್ತಮವಾದ ಒಂದು ಸುಧಾರಿತ ಚಿಕಿತ್ಸೆಯಾಗಿ ಕಂಡುಬಂದಿತು.[೧೧೩]
ಸಣ್ಣ ಜೀವಕೋಶದ ಶ್ವಾಸಕೋಶದ ಕಾರ್ಸಿನೋಮವು ಕಾಣಿಸಿಕೊಳ್ಳುವುದರೊಂದಿಗೆ, ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯ ಅಂಶಛೇದನ[೧೬೮] ಮತ್ತು ರೋಗಮೂಲಹಾರಿ ವಿಕಿರಣ ಚಿಕಿತ್ಸೆಗೆ[೧೬೯] ಸಂಬಂಧಿಸಿದಂತೆ 1960ರ ದಶಕದಲ್ಲಿ ಕಂಡುಬಂದ ಆರಂಭಿಕ ಪ್ರಯತ್ನಗಳು ವಿಫಲಗೊಂಡಿದ್ದವು. 1970ರ ದಶಕದಲ್ಲಿ, ಯಶಸ್ವೀ ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆಯ ಕಟ್ಟುಪಾಡುಗಳು ಅಭಿವೃದ್ಧಿ ಹೊಂದಿದ್ದವು.[೧೭೦]
ಚಿತ್ರಸಂಪುಟ
[ಬದಲಾಯಿಸಿ]-
ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ್ನು ತೋರಿಸುತ್ತಿರುವ ಎದೆಯ ರೇಡಿಯೋಗ್ರಾಫ್.
ಇವನ್ನೂ ಗಮನಿಸಿ
[ಬದಲಾಯಿಸಿ]- ಶ್ವಾಸನಾಳದ ಸೂಕ್ಷ್ಮಕವಲಿನ ಕಿರುಗುಳಿಯ ಕಾರ್ಸಿನೋಮ
- ಶ್ವಾಸಕೋಶದ ಕಾಲುವೆಯ ಗೆಡ್ಡೆ
- ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ನ ನಿರ್ದೇಶಿತ ಚಿಕಿತ್ಸೆ
ಉಲ್ಲೇಖಗಳು
[ಬದಲಾಯಿಸಿ]- ↑ WHO (2006). "Cancer". World Health Organization. Retrieved 2007-06-25.
{{cite web}}: Unknown parameter|month=ignored (help) - ↑ ೨.೦ ೨.೧ ೨.೨ ೨.೩ ೨.೪ ೨.೫ Minna, JD (2008). Harrison's Principles of Internal Medicine (17th ed.). McGraw-Hill. pp. 551–562. ISBN 0-07-146633-9.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ ೩.೦ ೩.೧ ೩.೨ ೩.೩ ೩.೪ ೩.೫ Vaporciyan, AA (2000). Cancer Medicine. B C Decker. pp. 1227–1292. ISBN 1-55009-113-1.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ ೪.೦ ೪.೧ ೪.೨ "Lung Carcinoma: Tumors of the Lungs". Merck Manual Professional Edition, Online edition. Retrieved 2007-08-15.
- ↑ Thun, MJ (2008). "Lung Cancer Occurrence in Never-Smokers: An Analysis of 13 Cohorts and 22 Cancer Registry Studies". PLoS Medicine. 5 (9): e185. doi:10.1371/journal.pmed.0050185. PMC 2531137. PMID 18788891.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help)CS1 maint: unflagged free DOI (link) - ↑ Gorlova, OY (2007). "Aggregation of cancer among relatives of never-smoking lung cancer patients". International Journal of Cancer. 121 (1): 111–118. doi:10.1002/ijc.22615. PMID 17304511.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Hackshaw, AK (1997-10-18). "The accumulated evidence on lung cancer and environmental tobacco smoke". British Medical Journal. 315 (7114): 980–988. PMC 2127653. PMID 9365295.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ ೮.೦ ೮.೧ Catelinois O, Rogel A, Laurier D; et al. (2006). "Lung cancer attributable to indoor radon exposure in france: impact of the risk models and uncertainty analysis". Environ. Health Perspect. 114 (9): 1361–6. doi:10.1289/ehp.9070. PMC 1570096. PMID 16966089. Archived from the original on 2009-01-20. Retrieved 2010-11-23.
{{cite journal}}: Explicit use of et al. in:|author=(help); Unknown parameter|doi_brokendate=ignored (help); Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - ↑ ೯.೦ ೯.೧ O'Reilly, KM (2007). "Asbestos-related lung disease". American Family Physician. 75 (5): 683–688. PMID 17375514. Archived from the original on 2007-09-29. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ೧೦.೦ ೧೦.೧ Kabir, Z (2007). "Lung cancer and urban air-pollution in dublin: a temporal association?". Irish Medical Journal. 100 (2): 367–369. PMID 17432813.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Coyle, YM (2006). "An ecological study of the association of metal air pollutants with lung cancer incidence in Texas". Journal of Thoracic Oncology. 1 (7): 654–661. doi:10.1097/01243894-200609000-00009. PMID 17409932.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ೧೨.೦ ೧೨.೧ Chiu, HF (2006). "Outdoor air pollution and female lung cancer in Taiwan". Inhalation Toxicology. 18 (13): 1025–1031. doi:10.1080/08958370600904561. PMID 16966302.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Carmona, RH (2006-06-27). "The Health Consequences of Involuntary Exposure to Tobacco Smoke: A Report of the Surgeon General". U.S. Department of Health and Human Services.
Secondhand smoke exposure causes disease and premature death in children and adults who do not smoke.
- ↑ "Tobacco Smoke and Involuntary Smoking" (PDF). IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. WHO International Agency for Research on Cancer. 83. 2002.
There is sufficient evidence that involuntary smoking (exposure to secondhand or 'environmental' tobacco smoke) causes lung cancer in humans. [...] Involuntary smoking (exposure to secondhand or 'environmental' tobacco smoke) is carcinogenic to humans (Group 1).
- ↑ ೧೫.೦ ೧೫.೧ Travis, WD (1995). "Lung cancer". Cancer. 75 (Suppl. 1): 191–202. doi:10.1002/1097-0142(19950101)75:1+<191::AID-CNCR2820751307>3.0.CO;2-Y. PMID 8000996.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Morandi, U (2006). "Bronchial typical carcinoid tumors". Seminars in Thoracic and Cardiovascular Surgery. 18 (3): 191–198. doi:10.1053/j.semtcvs.2006.08.005. PMID 17185178.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ Etienne-Mastroianni, B (2002). "Primary sarcomas of the lung: a clinicopathologic study of 12 cases". Lung Cancer. 38 (3): 283–289. doi:10.1016/S0169-5002(02)00303-3. PMID 12445750.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Bryant, A (2007). "Differences in epidemiology, histology, and survival between cigarette smokers and never-smokers who develop non-small cell lung cancer". Chest. 132 (1): 198–192. doi:10.1378/chest.07-0442. PMID 17573517. Archived from the original on 2008-12-06. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ೧೯.೦ ೧೯.೧ ಟ್ರಾವಿಸ್ WD. ಪೆಥಾಲಜಿ ಆಫ್ ಲಂಗ್ ಕ್ಯಾನ್ಸರ್. ಕ್ಲಿನ್ ಚೆಸ್ಟ್ ಮೆಡ್ 2002;23:65-81
- ↑ Subramanian, J (2007). "Lung cancer in never smokers: a review". Journal of Clinical Oncology. American Society of Clinical Oncology. 25 (5): 561–570. doi:10.1200/JCO.2006.06.8015. PMID 17290066.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ೨೧.೦ ೨೧.೧ Raz, DJ (2006). "Bronchioloalveolar carcinoma: a review". Clinical Lung Cancer. 7 (5): 313–322. doi:10.3816/CLC.2006.n.012. PMID 16640802.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ - ಸ್ಮಾಲ್ ಸೆಲ್ ಮೆಡ್ಲೈನ್ ಪ್ಲಸ್. 2010ರ ಫೆಬ್ರುವರಿ 5ರಂದು ಮರುಸಂಪಾದಿಸಲಾಯಿತು
- ↑ ೨೩.೦ ೨೩.೧ Collins, LG (2007). "Lung cancer: diagnosis and management". American Family Physician. American Academy of Family Physicians. 75 (1): 56–63. PMID 17225705. Archived from the original on 2007-09-29. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Rosti, G (2006). "Small cell lung cancer". Annals of Oncology. 17 (Suppl. 2): 5–10. doi:10.1093/annonc/mdj910. PMID 16608983.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Barbone, F (1997). "Cigarette smoking and histologic type of lung cancer in men" (PDF). Chest. American College of Chest Physicians. 112 (6): 1474–1479. doi:10.1378/chest.112.6.1474. PMID 9404741.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ರೊಗ್ಲಿ VL, ವೋಲ್ಮರ್ RT, ಗ್ರೀನ್ಬರ್ಗ್ SD, ಮೆಕ್ಗಾವ್ರಾನ್ MH, ಸ್ಪುಟ್ HJ, ಯೆಸ್ನರ್ R. ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ ಹೆಟೆರೋಜೀನಿಯಿಟಿ: ಎ ಬ್ಲೈಂಡೆಡ್ ಅಂಡ್ ರ್ಯಾಂಡಮೈಸ್ಡ್ ಸ್ಟಡಿ ಆಫ್ 100 ಕಾನ್ಸಿಕ್ಯುಟಿವ್ ಕೇಸಸ್. ಹಮ್ ಪ್ಯಾಥಾಲ್ 1985; 16: 569-79.
- ↑ ೨೭.೦ ೨೭.೧ Dishop MK, Kuruvilla S (2008). "Primary and metastatic lung tumors in the pediatric population: a review and 25-year experience at a large children's hospital". Arch. Pathol. Lab. Med. 132 (7): 1079–103. PMID 18605764.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Seo, JB (1 March 2001). "Atypical pulmonary metastases: spectrum of radiologic findings". Radiographics. 21 (2): 403–417. PMID 11259704.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Mountain, CF (2003). A Handbook for Staging, Imaging, and Lymph Node Classification. Charles P Young. Retrieved 2007-09-01.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ Hamilton, W (2005). "What are the clinical features of lung cancer before the diagnosis is made? A population based case-control study". Thorax. BMJ Publishing Group. 60 (12): 1059–1065. doi:10.1136/thx.2005.045880. PMC 1747254. PMID 16227326.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Honnorat, J (2007). "Paraneoplastic neurological syndromes". Orphanet Journal of Rare Diseases. BioMed Central. 2: 22. doi:10.1186/1750-1172-2-22. PMC 1868710. PMID 17480225.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help)CS1 maint: unflagged free DOI (link) - ↑ Jones, DR (1998). "Pancoast tumors of the lung". Current Opinion in Pulmonary Medicine. 4 (4): 191–197. doi:10.1097/00063198-199807000-00001. PMID 10813231.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Greene, Frederick L. (2002). AJCC cancer staging manual. Berlin: Springer-Verlag. ISBN 0-387-95271-3.
- ↑ Biesalski, HK (1998). "European Consensus Statement on Lung Cancer: risk factors and prevention. Lung Cancer Panel". CA Cancer J Clin. Smoking is the major risk factor, accounting for about 90% of lung cancer incidence. 48 (3): 167–176, discussion 164–166. doi:10.3322/canjclin.48.3.167. PMID 9594919.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help)CS1 maint: location (link)[ಶಾಶ್ವತವಾಗಿ ಮಡಿದ ಕೊಂಡಿ] - ↑ Hecht, S (2003). "Tobacco carcinogens, their biomarkers and tobacco-induced cancer". Nature Reviews. Cancer. Nature Publishing Group. 3 (10): 733–744. doi:10.1038/nrc1190. PMID 14570033.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Sopori, M (2002). "Effects of cigarette smoke on the immune system". Nature Reviews. Immunology. 2 (5): 372–7. doi:10.1038/nri803. PMID 12033743.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Peto, R (2006). Mortality from smoking in developed countries 1950–2000: Indirect estimates from National Vital Statistics. Oxford University Press. ISBN 0-19-262535-7.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ Samet, JM (1988). "Cigarette smoking and lung cancer in New Mexico". American Review of Respiratory Disease. 137 (5): 1110–1113. PMID 3264122.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Villeneuve, PJ (1994). "Lifetime probability of developing lung cancer, by smoking status, Canada". Canadian Journal of Public Health. 85 (6): 385–388. PMID 7895211.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Chlebowski RT; et al. (2009). "Non-small cell lung cancer and estrogen plus progestin use in postmenopausal women in the Women's Health Initiative randomized clinical trial". Journal of Clinical Oncology. 27 (155): CRA1500.
{{cite journal}}: Explicit use of et al. in:|author=(help) - ↑ US Department of Health and Human Services (1990-09-30). "The Health Benefits of Smoking Cessation: a Report of the Surgeon General" (PDF). Centers for Disease Control (CDC), Office on Smoking and Health. pp. vi, 130, 148, 152, 155, 164, 166. Retrieved 2007-11-18.
- ↑ Nordquist, LT (2004). "Improved survival in never-smokers vs current smokers with primary adenocarcinoma of the lung". Chest. American College of Chest Physicians. 126 (2): 347–351. doi:10.1378/chest.126.2.347. PMID 15302716. Archived from the original on 2008-12-06. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Tammemagi, CM (2004). "Smoking and lung cancer survival: the role of comorbidity and treatment". Chest. American College of Chest Physicians. 125 (1): 27–37. doi:10.1378/chest.125.1.27. PMID 14718417. Archived from the original on 2008-12-06. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Centers for Disease Control (CDC) (1986). "1986 Surgeon General's report: the health consequences of involuntary smoking". MMWR. Morbidity and mortality weekly report. CDC. 35 (50): 769–70. PMID 3097495. Retrieved 2007-08-10.
{{cite journal}}: Unknown parameter|month=ignored (help)
[62].
* EPA (1992). "Respiratory health effects of passive smoking: lung cancer and other disorders". EPA. Archived from the original on 2010-06-30. Retrieved 2007-08-10.{{cite journal}}: Cite journal requires|journal=(help)
* California Environmental Protection Agency (1997). "Health effects of exposure to environmental tobacco smoke". Tobacco Control. 6 (4): 346–353. doi:10.1136/tc.6.4.346. PMC 1759599. PMID 9583639.
* CDC (2001). "State-specific prevalence of current cigarette smoking among adults, and policies and attitudes about secondhand smoke—United States, 2000". Morbidity and Mortality Weekly Report. Atlanta, Georgia: CDC. 50 (49): 1101–1106. PMID 11794619.{{cite journal}}: More than one of|author1=and|last=specified (help); Unknown parameter|month=ignored (help)
* Alberg, AJ (2003). "Epidemiology of lung cancer". Chest. American College of Chest Physicians. 123 (S1): 21S–49S. doi:10.1378/chest.123.1_suppl.21S. PMID 12527563. Archived from the original on 2008-05-09. Retrieved 2010-11-23.{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Boffetta, P (1998). "Multicenter case-control study of exposure to environmental tobacco smoke and lung cancer in Europe" ([ಮಡಿದ ಕೊಂಡಿ]). Journal of the National Cancer Institute. Oxford University Press. 90 (19): 1440–1450. doi:10.1093/jnci/90.19.1440. PMID 9776409.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ "Report of the Scientific Committee on Tobacco and Health". Department of Health. 1998. Retrieved 2007-07-09.
{{cite web}}: Unknown parameter|month=ignored (help)
* Hackshaw, AK (1998). "Lung cancer and passive smoking". Statistical Methods in Medical Research. 7 (2): 119–136. doi:10.1191/096228098675091404. PMID 9654638.{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ National Health and Medical Research Council (April 1994). "The health effects and regulation of passive smoking". Australian Government Publishing Service. Archived from the original on September 29, 2007. Retrieved 2007-08-10.
{{cite journal}}: Cite journal requires|journal=(help); Unknown parameter|deadurl=ignored (help) - ↑ Schick, S (2005). "Philip Morris toxicological experiments with fresh sidestream smoke: more toxic than mainstream smoke". Tobacco Control. 14 (6): 396–404. doi:10.1136/tc.2005.011288. PMC 1748121. PMID 16319363.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Thun, M.J., S.J. Henley, D Burns, et al., Lung cancer death rates in lifelong nonsmokers. J. Natl Cancer Inst, 2006. 98: p.691.
- ↑ Sun, S., J.H. Schiller and A.F. Gazdar, Lung cancer in never-smokers: A different disease. Nat Rev Cancer, 2007. 7: p.778-90.
- ↑ Schmid K, Kuwert T, Drexler H (2010). "Radon in indoor spaces: an underestimated risk factor for lung cancer in environmental medicine". Dtsch Arztebl Int. 107 (11): 181–6. doi:10.3238/arztebl.2010.0181. PMC 2853156. PMID 20386676.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - ↑ EPA (2006). "Radiation information: radon". EPA. Retrieved 2007-08-11.
{{cite web}}: Unknown parameter|month=ignored (help) - ↑ Field, RW (1 June 2000). "Residential radon gas exposure and lung cancer: the Iowa Radon Lung Cancer Study". American Journal of Epidemiology. Oxford Journals. 151 (11): 1091–1102. PMID 10873134.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ EPA (2000). "Iowa Radon Lung Cancer Study". EPA. Archived from the original on 2008-12-25. Retrieved 2007-08-11.
{{cite web}}: Unknown parameter|month=ignored (help) - ↑ Darnton, AJ (2006). "Estimating the number of asbestos-related lung cancer deaths in Great Britain from 1980 to 2000". Annals of Occupational Hygiene. 50 (1): 29–38. doi:10.1093/annhyg/mei038. PMID 16126764.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Leroux, C (March–April 2007). "Jaagsiekte Sheep Retrovirus (JSRV): from virus to lung cancer in sheep". Veterinary Research. 38 (2): 211–228. doi:10.1051/vetres:2006060. PMID 17257570.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help)CS1 maint: date format (link) - ↑ Palmarini, M (2001). "Retrovirus-induced ovine pulmonary adenocarcinoma, an animal model for lung cancer". Journal of the National Cancer Institute. Oxford University Press. 93 (21): 1603–1614. doi:10.1093/jnci/93.21.1603. PMID 11698564.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Cheng, YW (1 April 2001). "The association of human papillomavirus 16/18 infection with lung cancer among nonsmoking Taiwanese women". Cancer Research. American Association for Cancer Research. 61 (7): 2799–2803. PMID 11306446.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Zheng, H (2007). "Oncogenic role of JC virus in lung cancer". Journal of Pathology. 212 (3): 306–315. doi:10.1002/path.2188. PMID 17534844.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Giuliani, L (2007). "Detection of oncogenic viruses (SV40, BKV, JCV, HCMV, HPV) and p53 codon 72 polymorphism in lung carcinoma". Lung Cancer. 57 (3): 273–281. doi:10.1016/j.lungcan.2007.02.019. PMID 17400331.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Pope, CA 3rd (2002). "Lung cancer, cardiopulmonary mortality, and long-term exposure to fine particulate air pollution". Journal of the American Medical Association. 287 (9): 1132–1141. doi:10.1001/jama.287.9.1132. PMID 11879110.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help)CS1 maint: numeric names: authors list (link) - ↑ Krewski D, Burnett R, Jerrett M, Pope CA, Rainham D, Calle E, Thurston G, Thun M (2005 Jul 9-23). "Mortality and long-term exposure to ambient air pollution: ongoing analyses based on the American Cancer Society cohort". J Toxicol Environ Health A. 68 (13–14): 1093–109. doi:10.1080/15287390590935941. PMID 16024490.
{{cite journal}}: Check date values in:|date=(help)CS1 maint: multiple names: authors list (link) - ↑ Valavanidis A, Fiotakis K, Vlachogianni T (2008 Oct-Dec). "Airborne particulate matter and human health: toxicological assessment and importance of size and composition of particles for oxidative damage and carcinogenic mechanisms". J Environ Sci Health C Environ Carcinog Ecotoxicol Rev. 26 (4): 339–62. doi:10.1080/10590500802494538. PMID 19034792.
{{cite journal}}: Check date values in:|date=(help)CS1 maint: multiple names: authors list (link) - ↑ Fong, KM (2003). "Lung cancer. 9: Molecular biology of lung cancer: clinical implications". Thorax. BMJ Publishing Group Ltd. 58 (10): 892–900. doi:10.1136/thorax.58.10.892. PMC 1746489. PMID 14514947.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Salgia, R (1998). "Molecular abnormalities in lung cancer". Journal of Clinical Oncology. 16 (3): 1207–1217. PMID 9508209.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ೬೬.೦ ೬೬.೧ ೬೬.೨ ೬೬.೩ Herbst, RS (2008). "Molecular origins of cancer: lung cancer". N Engl J Med. 359 (13): 1367–1380. doi:10.1056/NEJMra0802714. PMID 18815398. Archived from the original on 2008-09-28. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Aviel-Ronen, S (2006). "K-ras mutations in non-small-cell lung carcinoma: a review". Clinical Lung Cancer. Cancer Information Group. 8 (1): 30–38. doi:10.3816/CLC.2006.n.030. PMID 16870043.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Devereux, TR (1996). "Molecular mechanisms of lung cancer. Interaction of environmental and genetic factors". Chest. American College of Chest Physicians. 109 (Suppl 3): 14S–19S. doi:10.1378/chest.109.3_Supplement.14S. PMID 8598134.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Engels, EA (2007). "Systematic evaluation of genetic variants in the inflammation pathway and risk of lung cancer". Cancer Research. American Association for Cancer Research. 67 (13): 6520–6527. doi:10.1158/0008-5472.CAN-07-0370. PMID 17596594.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Wenzlaff, AS (2005). "CYP1A1 and CYP1B1 polymorphisms and risk of lung cancer among never smokers: a population-based study". Carcinogenesis. Oxford University Press. 26 (12): 2207–2212. doi:10.1093/carcin/bgi191. PMID 16051642.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Son, JW (2006). "Polymorphisms in the caspase-8 gene and the risk of lung cancer". Cancer Genetics and Cytogenetics. 169 (2): 121–127. doi:10.1016/j.cancergencyto.2006.04.001. PMID 16938569.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Yin, J (2007). "The DNA repair gene XRCC1 and genetic susceptibility of lung cancer in a northeastern Chinese population". Lung Cancer. 56 (2): 153–160. doi:10.1016/j.lungcan.2006.12.012. PMID 17316890.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Tomoda K, Ohkoshi T, Hirota K; et al. (2009). "Preparation and properties of inhalable nanocomposite particles for treatment of lung cancer". Colloids Surf B Biointerfaces. 71 (2): 177. doi:10.1016/j.colsurfb.2009.02.001. PMID 19264458.
{{cite journal}}: Explicit use of et al. in:|author=(help); Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - ↑ Fan, YG (2009). "Association between sputum atypia and lung cancer risk in an occupational cohort in yunnan, china". Chest. 135 (3): 778–85. doi:10.1378/chest.08-1469. PMID 19265088.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Vineis, P (2007). "Lung cancers attributable to environmental tobacco smoke and air pollution in non-smokers in different European countries: a prospective study". Environmental Health. BioMed Central. 6: 7. doi:10.1186/1476-069X-6-7. PMC 1803768. PMID 17302981.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help)CS1 maint: unflagged free DOI (link) - ↑ ೭೬.೦ ೭೬.೧ "A Decade of Broken Promises: The 1998 State Tobacco Settlement Ten Years Later" (PDF). Campaign for Tobacco-Free Kids. Retrieved 2008-12-03.
- ↑ Pandey, G (2005). "Bhutan's smokers face public ban". BBC. Retrieved 2007-09-07.
{{cite news}}: Unknown parameter|month=ignored (help) - ↑ Gray, N (2003). "A global approach to tobacco policy". Lung Cancer. BioMed Central. 39 (2): 113–117. doi:10.1016/S0169-5002(02)00456-7. PMID 12581561.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Slatore, CG (2008). "Long-term use of supplemental multivitamins, vitamin C, vitamin E, and folate does not reduce the risk of lung cancer". American Journal of Respiratory and Critical Care Medicine. 177 (5): 524–30. doi:10.1164/rccm.200709-1398OC. PMC 2258445. PMID 17989343.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ "UN health agency calls for total ban on tobacco advertising to protect young" (Press release). United Nations News service. 30 May 2008.
- ↑ van Klaveren RJ, Oudkerk M, Prokop M; et al. (2009). "Management of lung nodules detected by volume CT scanning". N. Engl. J. Med. 361 (23): 2221–9. doi:10.1056/NEJMoa0906085. PMID 19955524.
{{cite journal}}: Explicit use of et al. in:|author=(help); Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - ↑ Gohagan, JK (2005). "Final results of the Lung Screening Study, a randomized feasibility study of spiral CT versus chest X-ray screening for lung cancer". Lung Cancer. 47 (1): 9–15. doi:10.1016/j.lungcan.2004.06.007. PMID 15603850.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Schiller JH, Vidaver RM, Novello S, Brahmer J, Monroe L (2007). "Living with a Diagnosis of Lung Cancer". [National Lung Cancer Partnership]. Archived from the original on 2009-09-23. Retrieved 2008-12-01.
{{cite web}}: CS1 maint: multiple names: authors list (link) - ↑ Strand, TE (2007). "Risk factors for 30-day mortality after resection of lung cancer and prediction of their magnitude". Thorax. BMJ Publishing Group. 62 (11): 991. doi:10.1136/thx.2007.079145. PMC 2117132. PMID 17573442.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ El-Sherif, A (2006). "Outcomes of sublobar resection versus lobectomy for stage I non-small cell lung cancer: a 13-year analysis". Annals of Thoracic Surgery. 82 (2): 408–415. doi:10.1016/j.athoracsur.2006.02.029. PMID 16863738.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Fernando, HC (2005). "Lobar and sublobar resection with and without brachytherapy for small stage IA non-small cell lung cancer". Journal of Thoracic and Cardiovascular Surgery. 129 (2): 261–267. doi:10.1016/j.jtcvs.2004.09.025. PMID 15678034.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Casali G, Walker WS (2009). "Video-assisted thoracic surgery lobectomy: can we afford it?". Eur J Cardiothorac Surg. 35 (3): 423–8. doi:10.1016/j.ejcts.2008.11.008. PMID 19136272.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Hann CL, Rudin CM (2008 Nov 30). "Management of small-cell lung cancer: incremental changes but hope for the future". Oncology (Williston Park). 22 (13): 1486–92.
{{cite journal}}: Check date values in:|date=(help) - ↑ Murray, N (2006). "A review of first-line treatment for small-cell lung cancer". Journal of Thoracic Oncology. 1 (3): 270–278. PMID 17409868.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Azim, HA (2007). "Treatment options for relapsed small-cell lung cancer". Anticancer drugs. 18 (3): 255–261. doi:10.1097/CAD.0b013e328011a547. PMID 17264756.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ MacCallum, C (2006). "Second-line treatment of small-cell lung cancer". Current Oncology Reports. 8 (4): 258–264. doi:10.1007/s11912-006-0030-8. PMID 17254525.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Araujo AM, Mendez JC, Coelho AL; et al. (2009). "Phase II Study of Celecoxib with Cisplatin Plus Etoposide in Extensive-Stage Small Cell Lung Cancer". Cancer Invest. 27 (4): 1. doi:10.1080/07357900802232756. PMID 19266367.
{{cite journal}}: Explicit use of et al. in:|author=(help); Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - ↑ Clegg, A (2002). "Clinical and cost effectiveness of paclitaxel, docetaxel, gemcitabine, and vinorelbine in non-small cell lung cancer: a systematic review". Thorax. BMJ Publishing Group. 57 (1): 20–28. doi:10.1136/thorax.57.1.20. PMC 1746188. PMID 11809985.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Sandler A, Gray R, Perry MC; et al. (2006). "Paclitaxel-carboplatin alone or with bevacizumab for non-small-cell lung cancer". N Engl J Med. 355 (24): 2542–50. doi:10.1056/NEJMoa061884. PMID 17167137.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ↑ West HL, Franklin WA, McCoy J; et al. (2006). "Gefitinib therapy in advanced brochoalveolar carcinoma. Southwest Oncology Group study S0126". J Clin Oncol. 24 (12): 1807–13. doi:10.1200/JCO.2005.04.9890. PMID 16622257.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ↑ Miller VA, Riely GJ, Zakowski MF; et al. (2008). "Molecular characteristics of bronchoalveolar carcinoma and adenocarcinoma, brochoalveolar carcinoma subtype, predict response to erlotinib". J Clin Oncol. 26 (9): 1472–8. doi:10.1200/JCO.2007.13.0062. PMID 18349398.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ↑ Aggarwal C; et al. (2010). "Biomarkers with predictive and prognostic function in non-small cell lung cancer: ready for prime time?". J Natl Compr Canc Netw. 8: 822–32.
{{cite journal}}: Explicit use of et al. in:|author=(help) - ↑ Rosell, R; Moran, T; Queralt, C; Porta, R; Cardenal, F; Camps, C; Majem, M; Lopez-Vivanco, G; Isla, D (2009). "Screening for epidermal growth factor receptor mutations in lung cancer". N Engl J Med. 361 (10): 958–67. doi:10.1056/NEJMoa0904554. PMID 19692684.
- ↑ Mok TS; et al. (2009). "Gefitinib or carboplatin-paclitaxel in pulmonary adenocarcinoma". N Engl J Med. 361 (10): 947–57. doi:10.1056/NEJMoa0810699. PMID 19692680.
{{cite journal}}: Explicit use of et al. in:|author=(help) - ↑ Eaton KD, Martins RG (2010 Jul). "Maintenance chemotherapy in non-small cell lung cancer". J Natl Compr Canc Netw. 8 (7): 815–21. PMID 20679540.
{{cite journal}}: Check date values in:|date=(help) - ↑ Ciuleanu T, Brodowicz T, Zielinski C; et al. (2009). "Maintenance pemetrexed plus best supportive care versus placebo plus best supportive care for non-small-cell lung cancer: a randomised, double-blind, phase 3 study". Lancet. 374: 1432–40. doi:10.1016/S0140-6736(09)61497-5.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ↑ Cappuzzo F, Ciuleanu T, Stelmakh L; et al. (2010). "Erlotinib as maintenance treatment in advanced non-small-cell lung cancer: a multicentre, randomised, placebo-controlled phase 3 study". Lancet Oncol. 11: 521–9. doi:10.1016/S1470-2045(10)70112-1.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ↑ Fidias PM, Dakhil SR, Lyss AP; et al. (2009). "Phase III study of immediate compared with delayed docetaxel after front-line therapy with gemcitabine plus carboplatin in advanced non-small-cell lung cancer". J Clin Oncol. 27 (4): 591–8. doi:10.1200/JCO.2008.17.1405. PMID 19075278.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ↑ Rossi A, Ricciardi S, Maione P, de Marinis F, Gridelli C (2009). "Pemetrexed in the treatment of advanced non-squamous lung cancer". Lung Cancer. 66 (2): 141–9. doi:10.1016/j.lungcan.2009.06.006. PMID 19577816.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ↑ Winton, T (2005). "Vinorelbine plus cisplatin vs. observation in resected non-small-cell lung cancer". New England Journal of Medicine. Massachusetts Medical Society. 352 (25): 2589–2597. doi:10.1056/NEJMoa043623. PMID 15972865.
Adjuvant vinorelbine plus cisplatin has an acceptable level of toxicity and prolongs disease-free and overall survival among patients with completely resected early-stage non-small-cell lung cancer.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Douillard, JY (2006). "Adjuvant vinorelbine plus cisplatin versus observation in patients with completely resected stage IB-IIIA non-small-cell lung cancer (Adjuvant Navelbine International Trialist Association [ANITA]): a randomised controlled trial". Lancet Oncology. Elsevier. 7 (9): 719–727. doi:10.1016/S1470-2045(06)70804-X. PMID 16945766.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Tsuboi, M (2007). "The present status of postoperative adjuvant chemotherapy for completely resected non-small cell lung cancer" (PDF). Annals of Thoracic and Cardiovascular Surgery. 13 (2): 73–77. PMID 17505412.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ಒಲೌಸ್ಸೆನ್ KA, ಡ್ಯೂನಾಂಟ್ A, ಫೌರೆಟ್ P, ಮತ್ತು ಇತರರು: DNA ರಿಪೇರ್ ಬೈ ERCC1 ಇನ್ ನಾನ್-ಸ್ಮಾಲ್-ಸೆಲ್ ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ ಅಂಡ್ ಸಿಸ್ಪ್ಲಾಟಿನ್-ಬೇಸ್ಡ್ ಅಡ್ಜುವೆಂಟ್ ಕೀಮೋಥೆರಪಿ. N ಎಂಗ್ಲ್ J ಮೆಡ್ 2006;355:983-991
- ↑ Horn, L (2007). "The rationale for adjuvant chemotherapy in stage I non-small cell lung cancer". Journal of Thoracic Oncology. 2 (5): 377–383. doi:10.1097/01.JTO.0000268669.64625.bb. PMID 17473651.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Wakelee, HA (2006). "Current status of adjuvant chemotherapy for stage IB non-small-cell lung cancer: implications for the New Intergroup Trial". Clinical Lung Cancer. Cancer Information Group. 8 (1): 18–21. doi:10.3816/CLC.2006.n.028. PMID 16870041.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ BMJ (2005). Clinical evidence concise : the international resource of the best available evidence for effective health care. London: BMJ Publishing Group. pp. 486–488. ISBN 1-905545-00-2. ISSN 1475-9225.
{{cite book}}: Unknown parameter|month=ignored (help) - ↑ Arriagada, R (2002). Oxford Textbook of Oncology (2nd ed.). Oxford University Press. p. 2094. ISBN 0-19-262926-3.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ ೧೧೩.೦ ೧೧೩.೧ Saunders, M (1997). "Continuous hyperfractionated accelerated radiotherapy (CHART) versus conventional radiotherapy in non-small-cell lung cancer: a randomised multicentre trial". Lancet. Elsevier. 350 (9072): 161–165. doi:10.1016/S0140-6736(97)06305-8. PMID 9250182.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Wagner, H (1998). "Radiation therapy in the management of limited small cell lung cancer: when, where, and how much?". Chest. American College of Chest Physicians. 113 (Suppl. 1): 92S–100S. doi:10.1378/chest.113.1_Supplement.92S. PMID 9438697. Archived from the original ([ಮಡಿದ ಕೊಂಡಿ]) on 2007-11-09. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ PORT Meta-analysis Trialists Group (2005). "Postoperative radiotherapy for non-small cell lung cancer". Cochrane database of systematic reviews (Online) (2): CD002142. doi:10.1002/14651858.CD002142.pub2. PMID 15846628.
- ↑ Lally, BE (2006). "Postoperative Radiotherapy for Stage II or III Non–Small-Cell Lung Cancer Using the Surveillance, Epidemiology, and End Results Database". Journal of Clinical Oncology. John Wiley & Sons. 24 (19): 2998–3006. doi:10.1200/JCO.2005.04.6110. PMID 16769986.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Raben, A (1997). "Brachytherapy for non-small cell lung cancer and selected neoplasms of the chest". Chest. American College of Chest Physicians. 112 (Suppl. 4): 276S–286S. doi:10.1378/chest.112.4_Supplement.276S. PMID 9337304. Archived from the original on 2008-12-08. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Celebioglu, B (2002). "High dose rate endobronchial brachytherapy effectively palliates symptoms due to inoperable lung cancer". Japanese Journal of Clinical Oncology. Oxford University Press. 32 (11): 443–448. doi:10.1093/jjco/hyf102. PMID 12499415.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Ng, M (2007). "Tolerability of accelerated chest irradiation and impact on survival of prophylactic cranial irradiation in patients with limited-stage small cell lung cancer: review of a single institution's experience". Journal of Thoracic Oncology. International Association for the Study of Lung Cancer. 2 (6): 506–513. doi:10.1097/JTO.0b013e318060095b. PMID 17545845.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Slotman, B (2007). "Prophylactic cranial irradiation in extensive small-cell lung cancer". New England Journal of Medicine. 357 (7): 664–672. doi:10.1056/NEJMoa071780. PMID 17699816. Archived from the original on 2010-03-01. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Hof, H (2007). "Stereotactic single-dose radiotherapy (radiosurgery) of early stage nonsmall-cell lung cancer (NSCLC)". Cancer. Wiley InterScience. 110 (1): 148–155. doi:10.1002/cncr.22763. PMID 17516437.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help)[ಶಾಶ್ವತವಾಗಿ ಮಡಿದ ಕೊಂಡಿ] - ↑ Simon, CJ (2007). "Pulmonary radiofrequency ablation: long-term safety and efficacy in 153 patients". Radiology. 243 (1): 268–275. doi:10.1148/radiol.2431060088. PMID 17392258.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ೧೨೩.೦ ೧೨೩.೧ Bencardino, K (2007). "Epidermal growth factor receptor tyrosine kinase inhibitors for the treatment of non-small-cell lung cancer: results and open issues". Internal and Emergency Medicine. 2 (1): 3–12. doi:10.1007/s11739-007-0002-5. PMC 2780603. PMID 17551677.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Feld, R (2006). "Use of the epidermal growth factor receptor inhibitors gefitinib and erlotinib in the treatment of non-small cell lung cancer: a systematic review". Journal of Thoracic Oncology. International Association for the Study of Lung Cancer. 1 (4): 367–376. doi:10.1097/01243894-200605000-00018. PMID 17409886.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Sandler, A (2006). "Paclitaxel–carboplatin alone or with bevacizumab for non–small cell lung cancer". New England Journal of Medicine. Massachusetts Medical Society. 355 (24): 2542–2550. doi:10.1056/NEJMoa061884. PMID 17167137.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Edelman, MJ (2006). "Novel cytotoxic agents for non-small cell lung cancer". Journal of Thoracic Oncology. 1 (7): 752–755. doi:10.1097/01243894-200609000-00032. PMID 17409954.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Danesi, R (2007). "The role of pharmacogenetics in adjuvant treatment of non-small cell lung cancer". Journal of Thoracic Oncology. 2 (5 Suppl.): S27–S30. doi:10.1097/01.JTO.0000268638.10332.07. PMID 17457227.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Blackhall, FH (2007). "Small cell lung cancer and targeted therapies". Current Opinion in Oncology. 19 (2): 103–108. doi:10.1097/CCO.0b013e328011bec3. PMID 17272981.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Lee, JM (2007). "Significance of cyclooxygenase-2 in prognosis, targeted therapy and chemoprevention of NSCLC". Future Oncology. 2 (2): 149–153. doi:10.2217/14796694.3.2.149. PMID 17381414.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Whitehead, CM (1 May 2003). "Exisulind-induced Apoptosis in a Non-Small Cell Lung Cancer Orthotopic Lung Tumor Model Augments Docetaxel Treatment and Contributes to Increased Survival". Molecular Cancer Therapeutics. 2 (5): 479–488. PMID 12748310.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Scagliotti, G (2006). "Proteasome inhibitors in lung cancer". Critical Reviews in Oncology/Haematology. 58 (3): 177–189. doi:10.1016/j.critrevonc.2005.12.001. PMID 16427303.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Dragnev, KH (2007). "A proof-of-principle clinical trial of bexarotene in patients with non-small cell lung cancer". Clinical Cancer Research. American Association for Cancer Research. 13 (6): 1794–1800. doi:10.1158/1078-0432.CCR-06-1836. PMID 17363535.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Reade, CA (2009). "EGFR targeted therapy in non-small cell lung cancer: potential role of cetuximab". Biologics. 3: 215–224. PMC 2726075. PMID 19707410.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Albright, C (2007). "Vaccine therapy in non-small cell lung cancer". Current Oncology Reports. 9 (4): 241–246. doi:10.1007/s11912-007-0029-9. PMID 17588347.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Sun, S (2007). "New molecularly targeted therapies for lung cancer". Journal of Clinical Investigation. American Society for Clinical Investigation. 117 (10): 2740–2750. doi:10.1172/JCI31809. PMC 1994616. PMID 17909619.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ "Non-Small Cell Lung Cancer Treatment". PDQ for Health Professionals. National Cancer Institute. Retrieved 2008-11-22.
- ↑ "-Small Cell Lung Cancer Treatment". PDQ for Health Professionals. National Cancer Institute. Retrieved 2008-11-22.
- ↑ Mountain, CF (1997). "Revisions in the international system for staging lung cancer". Chest. American College of Chest Physicians. 111 (6): 1710–1717. doi:10.1378/chest.111.6.1710. PMID 9187198. Archived from the original (PDF) on 2008-12-06. Retrieved 2010-11-23.
- ↑ "Cancer Statistics Review 1975-2002 - Search". Surveillance Epidemiology and End Results (SEER). Archived from the original on July 06, 2007. Retrieved 2007-11-18.
{{cite web}}: Check date values in:|archivedate=(help); Unknown parameter|deadurl=ignored (help) - ↑ "WHO Disease and injury country estimates". World Health Organization. 2009. Retrieved November 11, 2009.
- ↑ "Commonly diagnosed cancers worldwide". Cancer Research UK. 2005. Archived from the original on 2008-01-10. Retrieved 2008-01-11.
{{cite web}}: Unknown parameter|month=ignored (help) - ↑ Jemal, A., R.C. Tiwari, T. Murray, A. Ghafoor, A. Samuels, El. Ward, E.J. Feuer, and M.J. Thun, Cancer statistics, 2004. CA Cancer J Clin, 2004. 54(1): p.8-29.
- ↑ Lum, KL (2008). "Signed, sealed and delivered: "big tobacco" in Hollywood, 1927-1951". Tobacco Control. 17 (5): 313–323. doi:10.1136/tc.2008.025445. PMC 2602591. PMID 18818225.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ "Deadly in Pink". Tobaccofreekids.org. Retrieved 2010-09-26.
- ↑ Parent, ME (2007). "Exposure to diesel and gasoline engine emissions and the risk of lung cancer". American Journal of Epidemiology. 165 (1): 53–62. doi:10.1093/aje/kwj343. PMID 17062632.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ "Gender in lung cancer and smoking research" (PDF). World Health Organization. 2004. Retrieved 2007-05-26.
- ↑ Liu, BQ (1998-11-21). "Emerging tobacco hazards in China: 1. Retrospective proportional mortality study of one million deaths". British Medical Journal. 317 (7170): 1411–1422. PMC 28719. PMID 9822393.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ Behera, D (2004). "Lung cancer in India" (PDF). Indian Journal of Chest Diseases and Allied Sciences. 46 (4): 269–281. PMID 15515828. Archived from the original (PDF) on 2008-12-17. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ Mohr, SB (2008). "Could ultraviolet B irradiance and vitamin D be associated with lower incidence rates of lung cancer?". Journal of Epidemiology and Community Health. 62 (1): 69–74. doi:10.1136/jech.2006.052571. PMID 18079336.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ ೧೫೦.೦ ೧೫೦.೧ Chen, F (2007). "Declining incidence rate of lung adenocarcinoma in the United States". Chest. 131 (4): 1000–1005. doi:10.1378/chest.06-1695. PMID 17426202. Archived from the original on 2008-12-06. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Charloux, A (1997). "The increasing incidence of lung adenocarcinoma: reality or artefact? A review of the epidemiology of lung adenocarcinoma". International Journal of Epidemiology. 26 (1): 14–23. doi:10.1093/ije/26.1.14. PMID 9126499.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ ಸಿಂಗ್ N, ಅಗರ್ವಾಲ್ AN, ಗುಪ್ತಾ D, ಮತ್ತು ಇತರರು. ಅನ್ಚೇಂಜಿಂಗ್ ಕ್ಲಿನಿಕೊ-ಎಪಿಡೆಮಿಯೋಲಾಜಿಕಲ್ ಪ್ರೊಫೈಲ್ ಆಫ್ ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ ಇನ್ ನಾರ್ತ್ ಇಂಡಿಯಾ ಓವರ್ ಥ್ರೀ ಡಿಕೇಡ್ಸ್. ಕ್ಯಾನ್ಸರ್ ಎಪಿಡೆಮಿಯೋಲ್ 2010; 34(1): 101-104
- ↑ ರಾವತ್ J, ಸಿಂಧ್ವಾನಿ G, ಗೌರ್ D, ಮತ್ತು ಇತರರು. ಕ್ಲಿನಿಕೊ-ಪೆಥಲಾಜಿಕಲ್ ಪ್ರೊಫೈಲ್ ಆಫ್ ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ ಇನ್ ಉತ್ತರಾಖಾಂಡ್. ಲಂಗ್ ಇಂಡಿಯಾ. 2009 ಜುಲೈ;26(3):74-6.
- ↑ ಖಾನ್ NA, ಆಫ್ರೋಜ್ F, ಲೋನ್ MM, ಮತ್ತು ಇತರರು. ಪ್ರೊಫೈಲ್ ಆಫ್ ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಇನ್ ಕಾಶ್ಮೀರ್, ಇಂಡಿಯಾ: ಎ ಫೈವ್-ಇಯರ್ ಸ್ಟಡಿ.ಇಂಡಿಯನ್ J ಚೆಸ್ಟ್ ಡಿಸ್ ಅಲೈಡ್ ಸೈನ್ಸ್ 2006 ಜುಲೈ-ಸೆಪ್ಟೆಂಬರ್;48(3):187-90.
- ↑ Morgagni, Giovanni Battista (1761). De sedibus et causis morborum per anatomen indagatis.
- ↑ Bayle, Gaspard-Laurent (1810). Recherches sur la phtisie pulmonaire (in French). Paris.
{{cite book}}: CS1 maint: unrecognized language (link) - ↑ ೧೫೭.೦ ೧೫೭.೧ Witschi, H (2001). "A short history of lung cancer". Toxicological Sciences. 64 (1): 4–6. doi:10.1093/toxsci/64.1.4. PMID 11606795.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Adler, I (1912). Primary Malignant Growths of the Lungs and Bronchi. New York: Longmans, Green, and Company. OCLC 14783544., cited in Spiro SG, Silvestri GA (2005). "One hundred years of lung cancer". American Journal of Respiratory and Critical Care Medicine. 172 (5): 523–529. doi:10.1164/rccm.200504-531OE. PMID 15961694.
- ↑ Grannis, FW. "History of cigarette smoking and lung cancer". smokinglungs.com. Archived from the original on July 18, 2007. Retrieved 2007-08-06.
- ↑ Proctor, R (2000). The Nazi War on Cancer. Princeton University Press. pp. 173–246. ISBN 0-691-00196-0.
- ↑ Doll, R (1956). "Lung cancer and other causes of death in relation to smoking; a second report on the mortality of British doctors". British Medical Journal. 2 (5001): 1071–1081. doi:10.1136/bmj.2.5001.1071. PMC 2035864. PMID 13364389.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ US Department of Health Education and Welfare (1964). "Smoking and health: report of the advisory committee to the Surgeon General of the Public Health Service" (PDF). Washington, DC: US Government Printing Office.
- ↑ Pirozynski, M (2006). "100 years of Lung Cancer". Respiratory Medicine. 100 (12): 2073–2084. doi:10.1016/j.rmed.2006.09.002. PMID 17056245.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Greaves, M (2000). Cancer: the Evolutionary Legacy. Oxford University Press. pp. 196–197. ISBN 0-19-262835-6.
- ↑ Horn, L (2008). "Evarts A. Graham and the first pneumonectomy for lung cancer". Journal of Clinical Oncology. 26 (19): 3268–3275. doi:10.1200/JCO.2008.16.8260. PMID 18591561. Archived from the original on 2020-03-17. Retrieved 2010-11-23.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Edwards, AT (1946). "Carcinoma of the bronchus". Thorax. 1 (1): 1–25. doi:10.1136/thx.1.1.1. PMC 1018207.
- ↑ Kabela, M (1956). "[Experience with radical irradiation of bronchial cancer]". Ceskoslovenská Onkológia (in German). 3 (2): 109–115. PMID 13383622.
{{cite journal}}: CS1 maint: unrecognized language (link) - ↑ Lennox, SC (1968). "Results of resection for oat-cell carcinoma of the lung". Lancet. Elsevier. 2 (7575): 925–927. doi:10.1016/S0140-6736(68)91163-X. PMID 4176258.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Miller, AB (1969). "Five-year follow-up of the Medical Research Council comparative trial of surgery and radiotherapy for the primary treatment of small-celled or oat-celled carcinoma of the bronchus". Lancet. Elsevier. 2 (7619): 501–505. doi:10.1016/S0140-6736(69)90212-8. PMID 4184834.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - ↑ Cohen, M (1977). "Intensive chemotherapy of small cell bronchogenic carcinoma". Cancer Treatment Reports. 61 (3): 349–354. PMID 194691.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help)
ಬಾಹ್ಯ ಕೊಂಡಿಗಳು
[ಬದಲಾಯಿಸಿ]- ಡೀಟೇಲ್ಡ್ ಗೈಡ್: ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ - ಸ್ಮಾಲ್ ಸೆಲ್ Archived 2009-11-02 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ. ಅಮೆರಿಕನ್ ಕ್ಯಾನ್ಸರ್ ಸೊಸೈಟಿ
- ಡೀಟೇಲ್ಡ್ ಗೈಡ್: ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ - ನಾನ್-ಸ್ಮಾಲ್ ಸೆಲ್ Archived 2010-06-27 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ. ಅಮೆರಿಕನ್ ಕ್ಯಾನ್ಸರ್ ಸೊಸೈಟಿ
- 1957 ಫಿಲ್ಮ್ ಆನ್ ಲಿಂಕ್ ಬಿಟ್ವೀನ್ ಸ್ಮೋಕಿಂಗ್ ಅಂಡ್ ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ Archived 2011-06-11 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ. ಧೂಮಪಾನ ಮತ್ತು ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಕುರಿತಾದ ಆರಂಭಿಕ ದೃಶ್ಯಭಾಗ
- ಲಂಗ್ ಕ್ಯಾನ್ಸರ್ ಟ್ಯುಟೋರಿಯಲ್ Archived 2007-12-17 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ. ಎದೆವಿಕಿರಣಶೀಲತೆಯ ಶಾಸ್ತ್ರ.net
- ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಓಪನ್ ಡೈರೆಕ್ಟರಿ ಪ್ರಾಜೆಕ್ಟ್
- LungCancer.org — ಉಚಿತ ಆಕರಗಳು ಮತ್ತು ಬೆಂಬಲದ ಸೇವೆಗಳು
- ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ರಾಷ್ಟ್ರೀಯ ಕ್ಯಾನ್ಸರ್ ಸಂಸ್ಥೆ
- ತಂಬಾಕು ಹೊಗೆ ಮತ್ತು ಅನೈಚ್ಛಿಕ ಧೂಮಪಾನ, ವರದಿಮಾಡಲಾದ ದತ್ತಾಂಶ ಮತ್ತು ಮೌಲ್ಯಮಾಪನದ ಸಾರಾಂಶ (2004) IARC
- ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್ ಲೇಖನಗಳು & ಮಾಹಿತಿ- ರಾಷ್ಟ್ರೀಯ ಆರೋಗ್ಯ ಸಂಸ್ಥೆಗಳಲ್ಲಿರುವ ಧೂಮಪಾನ ನಿಲ್ಲಿಸುವುದರ ಕುರಿತಾದ ಲೇಖನಗಳು ಮತ್ತು ಮಾಹಿತಿ
- PMID 19254045 (PubMed)
Citation will be completed automatically in a few minutes.
- CS1 errors: unsupported parameter
- CS1 maint: unflagged free DOI
- CS1 errors: explicit use of et al.
- CS1 maint: multiple names: authors list
- CS1 maint: location
- ಮಡಿದ ಬಾಹ್ಯ ಕೊಂಡಿಗಳನ್ನು ಹೊಂದಿರುವ ಎಲ್ಲಾ ಲೇಖನಗಳು
- ಮಡಿದ ಬಾಹ್ಯ ಕೊಂಡಿಗಳನ್ನು ಹೊಂದಿರುವ ಲೇಖನಗಳು from ಸೆಪ್ಟೆಂಬರ್ 2021
- Articles with invalid date parameter in template
- ಶಾಶ್ವತವಾಗಿ ಮಡಿದ ಬಾಹ್ಯ ಕೊಂಡಿಗಳನ್ನು ಹೊಂದಿರುವ ಎಲ್ಲಾ ಲೇಖನಗಳು
- CS1 errors: missing periodical
- CS1 errors: redundant parameter
- ಮಡಿದ ಬಾಹ್ಯ ಕೊಂಡಿಗಳನ್ನು ಹೊಂದಿರುವ ಲೇಖನಗಳು from July 2010
- CS1 maint: date format
- CS1 maint: numeric names: authors list
- CS1 errors: dates
- ಮಡಿದ ಬಾಹ್ಯ ಕೊಂಡಿಗಳನ್ನು ಹೊಂದಿರುವ ಲೇಖನಗಳು from May 2009
- CS1 maint: unrecognized language
- Articles with hatnote templates targeting a nonexistent page
- Commons link is locally defined
- Commons category with local link different than on Wikidata
- ವೆಬ್ ಆರ್ಕೈವ್ ಟೆಂಪ್ಲೇಟಿನ ವೇಬ್ಯಾಕ್ ಕೊಂಡಿಗಳು
- Articles with Open Directory Project links
- Pages with incomplete PMID references
- ಶ್ವಾಸಸಂಬಂಧಿ ಕಾಯಿಲೆಗಳ ಶಾಸ್ತ್ರ
- ಕ್ಯಾನ್ಸರ್ನ ಬಗೆಗಳು
- ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್
- Pages using PMID magic links