ಪರಮಾಣು ಸಂಖ್ಯೆ
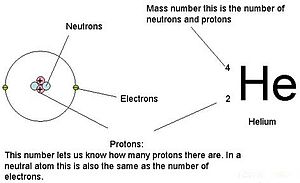
ರಸಾಯನಶಾಸ್ತ್ರ ಮತ್ತು ಭೌತಶಾಸ್ತ್ರದಲ್ಲಿ, ಪರಮಾಣು ಸಂಖ್ಯೆಯು (ಧನವಿದ್ಯುತ್ಕಣ ಸಂಖ್ಯೆ ಎಂದೂ ಪರಿಚಿತವಾಗಿರುವ) ಒಂದು ಪರಮಾಣುವಿನ ಪರಮಾಣು ಬೀಜದಲ್ಲಿ ಕಾಣಲಾದ ಧನವಿದ್ಯುತ್ಕಣಗಳ ಸಂಖ್ಯೆ ಮತ್ತು ಹಾಗಾಗಿ ಅದು ಪರಮಾಣು ಬೀಜದ ವಿದ್ಯುದಾವೇಶ ಸಂಖ್ಯೆಗೆ ತದ್ರೂಪವಾಗಿದೆ. ಇದನ್ನು ಸಾಂಪ್ರದಾಯಿಕವಾಗಿ Z ಸಂಕೇತದಿಂದ ಚಿತ್ರಿಸಲಾಗುತ್ತದೆ. ಪರಮಾಣು ಸಂಖ್ಯೆಯು ಒಂದು ಮೂಲಧಾತುವನ್ನು ಅದ್ವಿತೀಯವಾಗಿ ಗುರುತಿಸುತ್ತದೆ.
ಪರಮಾಣು ಸಂಖ್ಯೆ[೧] ಹಾಗೂ ಸಾಕ್ಷೇಪಿಕ ದ್ರವ್ಯರಾಶಿಯ ಸಂಖ್ಯೆಯ ನಡುವೆ ಗೊಂದಲವಿರಬಾರದು. ಪರಮಾಣು ತೂಕಕ್ಕೆ ಕೆಲವೊಮ್ಮೆ ಸಾಕ್ಷೇಪಿಕ ದ್ರವ್ಯರಾಶಿ ಎಂದು ಸಹ ಹೇಳಲಾಗುತ್ತದೆ. ದ್ರವ್ಯರಾಶಿ ಸಂಖ್ಯೆಯನ್ನು A ಎಂದು ಗುರುತಿಸಲಾಗುತ್ತದೆ. ಪರಮಾಣು ಸಂಖ್ಯೆ ಮತ್ತು ಪ್ರೋಟಾನ್ಗಳ ಸಂಖ್ಯೆ ಒಂದೇ. ಆದರೆ ಪರಮಾಣುವಿನ ಬೀಜಕಣ ಅಥವಾ ನ್ಯೂಕ್ಲಿಯಸ್ನಲ್ಲಿ ನ್ಯೂಟ್ರಾನ್ಗಳೂ ಇರುತ್ತವೆ (ಜಲಜನಕ ಪರಮಾಣುವಿನಲ್ಲಿ ಒಂದು ಪ್ರೋಟಾನ್ ಇರುತ್ತದೆ). ಬೀಜಕಣದಲ್ಲಿರುವ ನ್ಯೂಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯನ್ನು N ಎಂದು ಗುರುತಿಸಲಾಗುತ್ತದೆ. ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ತೂಕ ಮತ್ತು ದ್ರವ್ಯರಾಶಿಯ ದೋಷ[೨] ತೀರ ಕಡಿಮೆ ಇದ್ದು ಇವುಗಳನ್ನು ಕಡೆಗೆಣಿಸಬಹುದು. ಹೀಗಾಗಿ ದ್ರವ್ಯರಾಶಿಯ ಸಂಖ್ಯೆ A ಯನ್ನು ಪ್ರೋಟಾನ್ ಮತ್ತು ನ್ಯೂಟ್ರಾನ್ ಸಂಖ್ಯೆಗಳ ಮೂಲಕ ವ್ಯಕ್ತಪಡಿಸಬಹುದು. ಪ್ರೋಟಾನ್ ಮತ್ತು ನ್ಯೂಟ್ರಾನ್ ತೂಕಗಳಲ್ಲಿಯೂ ಗಣನೀಯ ವ್ಯತ್ಯಾಸವಿರುವುದಿಲ್ಲ.
ಮೇಲೆ ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿ ಸಂಖ್ಯೆಯ ವ್ಯಾಖ್ಯಾನ ನೋಡಿದಿರಿ. ಇಲ್ಲಿಯ ಇನ್ನೊಂದು ಅಂಶವೆಂದರೆ ಹಲವು ಮೂಲಧಾತುಗಳಲ್ಲಿನ ನ್ಯೂಟ್ರಾನ್ ಸಂಖ್ಯೆ ಒಂದೇ ಇರುವುದಿಲ್ಲ. ಒಂದು ಪರಮಾಣುವಿನಲ್ಲಿ ನ್ಯೂಟ್ರಾನ್ ಸಂಖ್ಯೆ ಭಿನ್ನವಾಗಿದ್ದರೆ ಅಂತಹ ಪರಾಮಾಣುಗಳನ್ನು ಸಮಸ್ಥಾನಿಗಳು (ಐಸೊಟೋಪ್) ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ನೂರಕ್ಕೆ ಎಪ್ಪತೈದಕ್ಕೂ ಹೆಚ್ಚು ಮೂಲಧಾತುಗಳಿಗೆ ನಿಸರ್ಗದಲ್ಲಿ ಸಮಸ್ಥಾನಿಗಳಿವೆ. ಹೀಗಾಗಿ ಪರಮಾಣು ತೂಕ ಅಥವಾ ಸಾಕ್ಷೇಪಿಕ ದ್ರವ್ಯರಾಶಿ ಸಂಖ್ಯೆಯು ಮಾದರಿಯಿಂದ ಮಾದರಿಗೆ ತುಸು ಭಿನ್ನವಾಗಬಹುದು. ಒಂದು ಧಾತುವಿನ ಸರಾಸರಿ ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿಯ (ನಿರ್ದಿಷ್ಟ ಮಾದರಿ ಅಥವಾ ಮೂಲದ) ಇಂಗಾಲ-12 ದ್ರವ್ಯರಾಶಿಯ 1⁄12ಕ್ಕೆ ಇರುವ ಅನುಪಾತವನ್ನು ಸಾಕ್ಷೇಪಿಕ ದ್ರವ್ಯರಾಶಿ ಸಂಖ್ಯೆ ಎಂದು ವ್ಯಾಖ್ಯಾನಿಸಲಾಗುತ್ತದೆ. ಐತಿಹಾಸಿಕವಾಗಿ ಹತ್ತೊಂಬತ್ತನೆಯ ಶತಮಾನದಲ್ಲಿ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞರು ಪರಮಾಣುತೂಕಗಳನ್ನು ಮಾತ್ರ (ಜಲಜನಕಕ್ಕೆ ಹೋಲಿಸಿ) ಅಳೆಯಬಲ್ಲವರಾಗಿದ್ದರು.
ಪರಮಾಣು ಸಂಖ್ಯೆಯು ಜರ್ಮನ್ ಪದದಿಂದ ಬಂದಿದ್ದು ಅದರ ಸಂವಾದಿ ಇಂಗ್ಲಿಷ್ ಪದ ಆಟಾಮಿಕ್ ನಂಬರ್ ಅಥವಾ ಸಂಖ್ಯೆಯು ಸಾಮಾನ್ಯವಾಗಿ (ಯಾವಾಗಲೂ ಅಲ್ಲ) ಆವರ್ತ ಕೋಷ್ಟಕದ ಅದು ಇರುವ ಸ್ಥಾನವನ್ನು ಸೂಚಿಸುತ್ತಿತ್ತು. 1915ರ ನಂತರ Z ಸಂಖ್ಯೆಯು ಬೀಜಕಣದ ಆವೇಶ (ಚಾರ್ಜ್) ಮತ್ತು ಅದು ಪರಮಾಣುವಿನ ಭೌತಿಕ ಗುಣ ಎಂಬ ಸೂಚನೆ ಮತ್ತು ಪುರಾವೆಗಳ ನಂತರವೇ ಅದಕ್ಕೊಂದು ಪ್ರಾಮುಖ್ಯತೆ ಲಭಿಸತೊಡಗಿತು.
ಇತಿಹಾಸ
[ಬದಲಾಯಿಸಿ]ದಿಮಿತ್ರಿ ಮೆಂಡಲೀವ್ 1869ರಲ್ಲಿ[೩] ಮೊದಲು ಸಾರ್ವತ್ರಿಕವಾಗಿ ಗುರುತಿಸಿದ ಆವರ್ತ ಕೋಷ್ಟಕವನ್ನು ಪ್ರಕಟಿಸಿದ. ಮೆಂಡಲೀವ್ ಪರಮಾಣು ತೂಕದ ಆಧಾರದ ಮೇಲೆ ಮೂಲಧಾತುಗಳನ್ನು ಅನುಕ್ರಮವನ್ನು ಸೂಚಿಸಿದ್ದೇನೆಂದು ಹೇಳಿದ. ಆದರೆ ಅವನು ಈ ಅನುಕ್ರಮವನ್ನು ಟೆಲ್ಲುರಿಯಮ್ (ಪರಮಾಣುತೂಕ 127.6) ಮತ್ತು ಅಯೊಡಿನ್ (ಪರಮಾಣುತೂಕ 126.9) ವಿಷಯದಲ್ಲಿ ತುಸು ಬದಲಾಯಿಸಿ ಟೆಲ್ಲುರಿಯಮ್ನ್ನು ಮೊದಲು ಇರಿಸಿದ. ಇದಕ್ಕೆ ಅವನು ಆ ಮೂಲಧಾತುಗಳ ರಾಸಾಯನಿಕ ಗುಣಗಳನ್ನು ಬಳಸಿದ್ದೇ ಕಾರಣವಾಗಿತ್ತು. ಪರಮಾಣು ಸಂಖ್ಯೆ ಇರುವಿಕೆಯ ಬಗೆಗೆ ಅಂದು ಏನೇನೂ ತಿಳಿದಿರಲಿಲ್ಲವಾದರೂ ಈ ಅನುಕ್ರಮ ಪರಮಾಣು ಸಂಖ್ಯೆಯ ಆಧಾರಕ್ಕೆ ಅನುಗುಣವಾಗಿದೆ.
ಆದರೆ ಕೇವಲ ಆವರ್ತಕ ಕೋಷ್ಟಕದಲ್ಲಿನ ಸಂಖ್ಯೆಯ ಮೇಲೆಯೇ ಧಾತುಗಳಿಗೆ ಕ್ರಮಸಂಖ್ಯೆ ನೀಡವುದು ಸಮರ್ಪಕವೆನ್ನಿಸುತ್ತಿರಲಿಲ್ಲ, ಹೀಗಾಗಿ ಹಲವು ಧಾತುಗಳ ಆವರ್ತ ಕೋಷ್ಟಕದ ಸ್ಥಾನವನ್ನು ಪರಮಾಣು ತೂಕದ ಬದಲು ರಾಸಾಯನಿಕ ಗುಣಗಳನ್ನು ಆಧಾರವಾಗಿಸಿ ಕೊಳ್ಳಬೇಕಾಯಿತು. ನಿಧಾನವಾಗಿ ಒಂದೇ ರೀತಿಯ ರಾಸಾಯನಿಕ ಗುಣಗಳನ್ನು ಹೊಂದಿರುವ ಹೆಚ್ಚು ಲ್ಯಾಂಥನೈಡ್ ಧಾತುಗಳನ್ನು ಕಂಡುಹಿಡಿದಂತೆ ಆವರ್ತ ಕೋಷ್ಟಕದಲ್ಲಿ ಅವುಗಳ ಸ್ಥಾನದ ಬಗೆಗೆ ಸಮಸ್ಯೆ ಉಂಟಾಯಿತು.
ಅಣು ಮಾದರಿ ಮತ್ತು ಮೊಸ್ಲೆ ಪ್ರಯೋಗಗಳು
[ಬದಲಾಯಿಸಿ]1911ರಲ್ಲಿ ರುದರ್ಫೋರ್ಡ್ ಪರಮಾಣು ಮಾದರಿಯೊಂದನ್ನು ಸೂಚಿಸಿದ. ಈ ಮಾದರಿಯಲ್ಲಿ ಬಹುತೇಕ ಪರಮಾಣು ದ್ರವ್ಯವು ಕೇಂದ್ರದಲ್ಲಿ ಇತ್ತು ಮತ್ತು ಅದು ಧನಾತ್ಮಕ ಆವೇಶವನ್ನು ಹೊಂದಿತ್ತು. ಈ ಧನಾತ್ಮಕ ಆವೇಶವು ಜಲಜನಕ ಪರಮಾಣುಗಳಲ್ಲಿ ಹೇಳಿದ ಪರಮಾಣು ತೂಕದ ಸರಿಸುಮಾರು ಅರ್ಧದಷ್ಟಿತ್ತು. ರುದರ್ಫೋರ್ಡ್ ಊಹಿಸಿದ ಒಂದೇ ಪರಮಾಣುವಾದ ಬಂಗಾರದಲ್ಲಿ ಇದು 100 ಆಗಿತ್ತು (ವಾಸ್ತವದ ಆವರ್ತ ಕೋಷ್ಟಕದಲ್ಲಿ ಬಂಗಾರದ ಸಂಖ್ಯೆ 79 ಆಗಿತ್ತು). ರುದರ್ಫೋರ್ಡ್ನ ಈ ಬಗೆಗಿನ ಪ್ರಬಂಧದ ಒಂದು ತಿಂಗಳ ನಂತರ ಆಂಟೋನಿಯಸ್ ವ್ಯಾನ್ ಡೆನ್ ಬ್ರೊಯೆಕ್ ವಿಧ್ಯುಕ್ತವಾಗಿ ಕೇಂದ್ರದ ಆವೇಶ ಮತ್ತು ಪರಮಾಣುವಿನಲ್ಲಿನ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆ ಆವರ್ತ ಕೋಷ್ಟಕದ ಕ್ರಮ ಸಂಖ್ಯೆಗೆ ಸಮವಾಗಿರುತ್ತದೆ ಎಂದು ಸೂಚಿಸಿದ. ವಾಸ್ತವದಲ್ಲಿ ಈ ಊಹೆ ನಿಜವಾಯಿತು.
ಆದರೆ ಪ್ರಾಯೋಗಿಕ ಪುರಾವೆಗಳು 1913 ರ ಹೆನ್ರಿ ಮೊಸ್ಲೆ ಪ್ರಯೋಗಗಳ ನಂತರ ದೊರೆಯತೊಡಗಿದವು. ಮೊಸ್ಲೆ ಅದೇ ಪ್ರಯೋಗಶಾಲೆಯಲ್ಲಿದ್ದ ಬೋರ್ನೊಂದಿಗೆ ಚರ್ಚಿಸಿದ ನಂತರ ಬ್ರೆಯೆಕ್ ಸೂಚನೆ ಮತ್ತು ಬೋರ್ ಊಹನ ಅಥವಾ ಹೈಪೊತೀಸಿಸ್[೪] ಪರೀಕ್ಷಿಸಲು ನಿರ್ದರಿಸಿದ. ಇದಕ್ಕೂ ತುಸು ಮುಂಚೆ 1909ರಲ್ಲಿ ಚಾರ್ಲ್ಸ್ ಜಿ. ಬಾರ್ಕ್ಲ ಹಲವು ಧಾತುಗಳು ವಿಶಿಷ್ಟ ಎಕ್ಸ್ ರೇಗಳನ್ನು ಹೊರಸೂಸುತ್ತವೆಯೆಂದು ಪತ್ತೆ ಮಾಡಿದರು ಮತ್ತು ಅಂದು ಇನ್ನೂ ಅವುಗಳ ಅಲೆಯುದ್ದವನ್ನು ಅಳೆಯುವ ತಂತ್ರವಿರಲಿಲ್ಲ ವಾದ್ದರಿಂದ ಎಷ್ಟರ ಮಟ್ಟಿಗೆ ಈ ಎಕ್ಸ್ ರೇಗಳು ಹಿಂಗಿಸಲ್ಪಡುತ್ತವೆ ಎಂಬುದನ್ನು ಅಳೆದರು.[೫] ಹೆನ್ರಿ ಮೊಸ್ಲೆ, ತುಸು ಹಿಂದೆಯಷ್ಟೆ ವಿಲಿಯಂ ಲಾರೆನ್ಸ್ ಬ್ರಾಗ್ (ಮತ್ತು ಅವರ ತಂದೆ ವಿಲಿಯಂ ಹೆನ್ರಿ ಬ್ರಾಗ್ ಜೊತೆಗೂಡಿ) ಹೊಸದಾಗಿ ಕಂಡುಹಿಡಿದ ತಂತ್ರಗಳನ್ನು ಬಳಸಿ, ಅಲ್ಯೂಮಿನಿಯಮ್ ನಿಂದ ಬಂಗಾರದವರೆಗೆ ಅಂದು ತಿಳಿದ ಎಲ್ಲ ಧಾತುಗಳು ಹೂರಸೂಸುವ ಎಕ್ಸ್ ರೇಗಳ ಆವರ್ತನ (ಫ್ರೀಕ್ವೆನ್ಸಿ) ಕಂಡುಹಿಡಿಯಲು ನಿರ್ಣಯಿಸಿದ.[೬] ಮೊಸ್ಲೆ ಅದಕ್ಕೊಂದು ಪ್ರಯೋಗವನ್ನು ರೂಪಿಸಿದ ಮತ್ತು ಎಕ್ಸ್ ರೆ ಕಿರಣಗಳ ರೋಹಿತ ಸಾಲುಗಳ ಆವರ್ತನಗಳನ್ನು ಅಳೆದ.[೭] ಈ ಪ್ರಯೋಗವು ಆವರ್ತನಗಳ ವರ್ಗ ಮೂಲ (ಸ್ಕ್ವಯೆರ್ ರೂಟ್) ಮತ್ತು ಆವರ್ತ ಕೋಷ್ಟಕದಲ್ಲಿನ ಅದರ ಕ್ರಮಸಂಖ್ಯೆಗೂ ಸಂಬಂಧವಿದೆ ಎಂದು ತೋರಿಸಿಕೊಟ್ಟಿತು. ಆವರ್ತ ಕೋಷ್ಟಕದಲ್ಲಿನ ಧಾತುವಿನ ಸಂಖ್ಯೆ ಹೆಚ್ಚಾದಂತೆ ಆವರ್ತನಗಳ ವರ್ಗ ಮೂಲವೂ ಹೆಚ್ಚಾಗುತ್ತಿತ್ತು. ಮೊದಲ ಸಲ ಆವರ್ತ ಕೋಷ್ಟಕದಲ್ಲಿನ ಸಂಖ್ಯೆಗಳಿಗೆ ಪ್ರಾಯೋಗಿಕ ಆಧಾರವೊಂದು ಒದಗಿ ಬಂತು.
ಪ್ರೋಟಾನ್ ಮತ್ತು ಬೀಜಕಣ ಎಲೆಕ್ಟ್ರಾನ್
[ಬದಲಾಯಿಸಿ]ಪರಮಾಣು ಸಂಖ್ಯೆ Z ಎಂಬ ಚಿಂತನೆ ಪ್ರಾಮುಖ್ಯತೆಗೆ ಬಂದಿತಾದರೂ ಇದರ ಮಹತ್ವ ಏನು ಎಂದು ತಿಳಿದಿರಲಿಲ್ಲ. ಹಿಂದೆ ಹತ್ತೊಂಬತ್ತನೆಯ ಶತಮಾನದಲ್ಲಿ ಬ್ರಿಟಿಶ್ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞ ವಿಲಿಯಂ ಪ್ರೌಟ್ ಎಲ್ಲಾ ಧಾತುಗಳು ಹಲವು ಜಲಜನಕ ಪರಮಾಣುವನ್ನು ಹೊಂದಿರುತ್ತವೆ ಎಂಬ ಊಹನವೊಂದನ್ನು ಮಂಡಿಸಿದ್ದ ಮತ್ತು ಅವುಗಳನ್ನು ಪ್ರೊಲೈಟ್ ಎಂದು ಕರೆದಿದ್ದ. ಆದರೆ 1907 ರಷ್ಟು ಹಿಂದೆ ರುದರ್ಫೋರ್ಡ್ ಮತ್ತು ಥಾಮಸ್ ರಾಯ್ಡ್ಸ್ ಎರಡು ಧನಾವೇಶ (ಪಾಸಿಟಿವ್ ಚಾರ್ಜ್) ಇರುವ ಆಲ್ಫಾ ಕಣಗಳು ಹೀಲಿಯಮ್ ಬೀಜಕಣ ಎಂತಲೂ ಅವು ಜಲಜನಕ ಪರಮಾಣವಿನ ನಾಲ್ಕರಷ್ಟು ತೂಗುತ್ತವೆ ಎಂದೂ ತೋರಿಸಿಕೊಟ್ಟಿದ್ದರು. ಪ್ರೌಟ್ನ ಊಹನ ನಿಜವೇ ಆಗಿದ್ದಲ್ಲಿ ಆಲ್ಫಾ ಕಣಗಳ ತೂಕ ಜಲಜನಕ ಪರಮಾಣುವಿನ ಎರಡರಷ್ಟಾಗಿರ ಬೇಕಿತ್ತು. ಬೇರೆ ಮಾತುಗಳಲ್ಲಿ ಹೇಳಬೇಕೆಂದರೆ ಬೀಜಕಣದಲ್ಲಿ ಹೆಚ್ಚುವರಿಯಾಗಿರುವ "ಪ್ರೊಲೈಟ್" ಅಥವಾ ಜಲಜನಕ ಪರಮಾಣುವಿನ ಈ ಹೆಚ್ಚುವರಿ ಧನಾವೇಶವನ್ನು ತಟಸ್ಥವಾಗುವುದು ಹೇಗೆ ಎಂಬ ಪ್ರಶ್ನೆಯೊಂದು ಮೂಡಿತು.
1919ರಲ್ಲಿ ರುದರ್ಫೋರ್ಡ್ ಆಲ್ಫಾ ಕಣಗಳನ್ನು[೮] ಸಾರಜನಕದ ಮೇಲೆ ಹಾಯಿಸಿ ಆಮ್ಲಜನಕ ಮತ್ತು ಜಲಜನಕ ಬೀಜಕಣಗಳನ್ನು ಪಡೆದ. ಈ ಪ್ರಯೋಗ ಪಲಿತಾಂಶವು ರುದರ್ಫೋರ್ಡ್ಗೆ ಪ್ರೌಟ್ ಊಹನಕ್ಕೆ ಪ್ರಾಯೋಗಿಕ ಬೆಂಬಲವಾಗಿ ತೋರಿತು. ಆಮ್ಲಜನಕದೊಂದಿಗೆ ಹುಟ್ಟಿದ ಹೊಸ ಕಣವನ್ನು ರುದರ್ಫೋರ್ಡ್ ಪ್ರೋಟಾನ್ (ಬದಲಿ ಹೆಸರುಗಳು ಪ್ರೌಟಾನ್ ಅಥವಾ ಪ್ರೊಲೈಟ್) ಎಂದು ಕರೆದ. ಆದರೆ ಮೊಸ್ಲೆ ಪ್ರಯೋಗವು ಭಾರ ಧಾತುಗಳ ಪರಮಾಣು ಜಲಜನಕ ಪರಮಾಣುವಿನಿಂದಾದುದು ಎಂದು ಭಾವಿಸಲು ಇರುವ ತೊಂದರೆ ಎಂದರೆ ಹಾಗೆ ಭಾವಿಸಿದಲ್ಲಿನ ಪರಮಾಣುತೂಕಕ್ಕಿಂತ ವಾಸ್ತವದ ಪರಮಾಣು ತೂಕವು ಸುಮಾರು ಎರಡರಷ್ಟಾಗುತ್ತದೆ ಎಂದು ಹೇಳುತ್ತದೆ. ಉದಾಹರಣೆಗೆ ಹೀಲಿಯಮ್ ಬೀಜಕಣದ ಧನಾವೇಶ 2 ಆದರೆ ಅದರ ಪರಮಾಣು ತೂಕ 4 (ಜಲಜಲಕ ಬೀಜಕಣ). ಇದನ್ನು ವಿವರಿಸಲು ಬೀಜಕಣದಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಇರುವಿಕೆಯ ಬಗೆಗಿನ ಊಹನ ಮಂಡಿಸಲಾಯಿತು. ಇದರ ಪ್ರಕಾರ ಪರಮಾಣು ತೂಕ ಎಷ್ಟು ಹೆಚ್ಚುವರಿಯಾಗಿರುತ್ತದೆಯೋ ಅಷ್ಟು ಪ್ರೋಟಾನ್ಗಳು ಬೀಜಕಣದಲ್ಲಿರುತ್ತವೆ ಮತ್ತು ಅವನ್ನು ತಟಸ್ಥ ಮಾಡಲು ಅಷ್ಟೇ ಸಂಖ್ಯೆಯ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಬೀಜಕಣದಲ್ಲಿರುತ್ತವೆ ಎಂದು ಊಹಿಸಲಾಯಿತು. ಈ ಪ್ರಕಾರ ಹೀಲಿಯಮ್ ಪರಮಾಣು ಬೀಜಕಣದಲ್ಲಿ 4 ಪ್ರೋಟಾನುಗಳು ಮತ್ತು 2 ಬೀಜಕಣ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಇರುತ್ತವೆ. ಹಾಗೆಯೇ ಆವರ್ತ ಕೋಷ್ಟಕದ ಇನ್ನೊಂದು ತುದಿಯಲ್ಲಿದ್ದ ಬಂಗಾರ ಅಥವಾ ಚಿನ್ನದ ಪರಮಾಣು ತೂಕ ಜಲಜನಕದ 197 ರಷ್ಟು ಮತ್ತು ಅದರ ಆವರ್ತ ಕೋಷ್ಟಕದ ಸ್ಥಾನ 79. ಇದನ್ನು ವಿವರಿಸಲು ಚಿನ್ನದ ಪರಮಾಣು ಬೀಜಕಣದಲ್ಲಿ 197 ಪ್ರೋಟಾನುಗಳು ಮತ್ತು 118 ಬೀಜಕಣ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಇರುತ್ತವೆ ಎಂದು ಭಾವಿಸಲಾಗಿತ್ತು.
ನ್ಯೂಟ್ರಾನ್ಗಳ ಕಂಡುಹಿಡಿಯುವಿಕೆ
[ಬದಲಾಯಿಸಿ]1931ರಲ್ಲಿ ಜರ್ಮನಿಯ ವಾಲ್ಟರ್ ಬೋತೆ ಮತ್ತು ಹರ್ಬಟ್ ಬೆಕರ್ ಪೋಲೊನಿಯಮ್ನಿಂದ ಉತ್ಪನ್ನವಾದ ಆಲ್ಫಾ ಕಣಗಳನ್ನು [೮] ಬೆರಿಲಿಯಮ್, ಬೋರಾನ್ ಅಥವಾ ಲಿಥಿಯಮ್ನಂತಹ ಕೆಲವು ಹಗುರ ಧಾತುಗಳ ಮೇಲೆ ಬಿದ್ದಾಗ ಕೆಲವು ವಿಕಿರಣಗಳು ಉತ್ಪನ್ನವಾಗುತ್ತವೆ ಎಂಬುದನ್ನು ಗಮನಿಸಿದರು. ಅವುಗಳಿಗೆ ಯಾವುದೇ ಆವೇಶ (ಚಾರ್ಜ್) ಇರುವುದಿಲ್ಲವಾದ್ದರಿಂದ ಅವುಗಳನ್ನು ಗಾಮ ಕಿರಣಗಳು (ಶಕ್ತಿಯುತ ವಿದ್ಯುತ್ಕಾಂತೀಯ ವಿಕಿರಣಗಳು) ಎಂದು ಭಾವಿಸಿದರು. ನಂತರದ ವರುಷದಲ್ಲಿ ಪ್ಯಾರಿಸ್ನಲ್ಲಿ ಇರ್ನೆ ಜೋಲಿಯಟ್-ಕ್ಯೂರಿ ಮತ್ತು ಫೆಡ್ರಿಕ್ ಜೋಲಿಯಟ್ ಈ ಹೊಸ ಕಿರಣಗಳು ಮೇಣ (ಪ್ಯಾರಫಿನ್) ಅಥವಾ ಇತರ ಜಲಜನಕ ಸಂಯುಕ್ತಗಳ ಮೇಲೆ ಬಿದ್ದಾಗ ಹೆಚ್ಚು ಶಕ್ತಿಯುತ ಪ್ರೋಟಾನುಗಳನ್ನು ಹೊರಸೂಸುವಂತೆ ಮಾಡುತ್ತವೆ ಎಂದು ತೋರಿಸಿಕೊಟ್ಟರು. ಆದರೆ ಪ್ರಯೋಗದ ಹಲವು ಪಲಿತಾಂಶಗಳನ್ನು ವಿವರಿಸುವುದು ಕಷ್ಟಕರವಾಗಿತ್ತು. ಈ ಹೊಸ ಕಿರಣಗಳು ಪ್ರೋಟಾನುಗಳೊಂದಿಗೆ ಪರಸ್ಪರಕ್ರಿಯೆ ನಡೆಸುವ ರೀತಿಯು ಹೊಸ ತಟಸ್ಥ ಕಣದ ಅಗತ್ಯವನ್ನು ಸೂಚಿಸುತ್ತದೆ ಎಂದು ರೋಮ್ನ ಭೌತಶಾಸ್ತ್ರಜ್ಞ ಎಟ್ಟೊರೆನೆ ಮಜೊರನ ಸೂಚಿಸಿದರು.[೯]
ಈ ಹೊಸ ಕಿರಣಗಳು ಗಾಮ ಕಿರಣಗಳೆಂಬ ವಿವರಣೆಯ ಬಗೆಗೆ ಅಸಮಾಧಾನ ಹೊಂದಿದ್ದ ಜೇಮ್ಸ್ ಚಾಡ್ವಿಕ್ ಪ್ರಯೋಗಗಳ ಮೂಲಕ 1932ರಲ್ಲಿ ಈ ಹೊಸ ಕಿರಣಗಳು ಗಾಮ ಕಿರಣಗಳಲ್ಲ ಬದಲಾಗಿ ಪ್ರೋಟಾನಿನಷ್ಟೇ ದ್ರವ್ಯರಾಶಿ ಇರುವ ತಟಸ್ಥ ಕಣಗಳು ಎಂದು ತೋರಿಸಿಕೊಟ್ಟರು. ಹೀಗೆ ಪರಮಾಣು ಬೀಜಕಣದಲ್ಲಿರುವ ಹೆಚ್ಚುವರಿ ಪ್ರೋಟಾನು ಮತ್ತು ಅದನ್ನು ತಟಸ್ಥಗೊಳಿಸಲು ಇದೆ ಎಂದು ಭಾವಿಸಲಾದ ಎಲೆಕ್ಟ್ರಾನ್ ಇರುತ್ತವೆ ಎಂಬ ಚಿಂತನೆ ಬಿದ್ದು ಹೋಯಿತು. ಆ ಸ್ಥಾನವನ್ನು ಹೊಸದಾಗಿ ಕಂಡುಹಿಡಿದ ನ್ಯೂಟ್ರಾನ್ ಆಕ್ರಮಿಸಿತು.[೯]
ಪರಮಾಣು ಸಂಖ್ಯೆ ಮತ್ತು ಆಧುನಿಕ ಪರಮಾಣು ಮಾದರಿ
[ಬದಲಾಯಿಸಿ]ಇದರೊಂದಿಗೆ ಧಾತುವೊಂದರ ಪರಮಾಣುವಿನ ಬೀಜಕಣದಲ್ಲಿರುವ ಪ್ರೋಟಾನು ಸಂಖ್ಯೆಯು ಅದರ Z ಆಯಿತು ಮತ್ತು ಅದು ಪರಮಾಣುವೊಂದರ ಧನಾವೇಶವಾಯಿತು. 1915 ಕ್ಕೂ ಮುಂಚೆ ಅದೊಂದು ಆವರ್ತ ಕೋಷ್ಟಕದಲ್ಲಿ ಮೂಲಧಾತುವೊಂದರ ಕ್ರಮಸಂಖ್ಯೆ ಮಾತ್ರವಾಗಿತ್ತು. ತಟಸ್ಥ ಪರಮಾಣುವೊಂದರಲ್ಲಿ ಅದರ ಬೀಜಕಣ ಅಥವಾ ನ್ಯೂಕ್ಲಿಯಸ್ನಲ್ಲಿ ಎಷ್ಟು ಪ್ರೋಟಾನುಗಳಿರುತ್ತವೆಯೋ ಅಷ್ಟೇ ಸಂಖ್ಯೆಯ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿರುತ್ತವೆ. ಪರಮಾಣು ತೂಕಕ್ಕೆ ಧನಾವೇಶವಿರುವ ಪ್ರೋಟಾನುಗಳಲ್ಲದೆ ಬಹುತೇಕ ಅದೇ ದ್ರವ್ಯರಾಶಿಯಿರುವ ತಟಸ್ಥ ಆವೇಶದ ನ್ಯೂಟ್ರಾನ್ಗಳು ಸಹ ಕಾರಣವಾಗುತ್ತವೆ. ಈ ಎರಡೂ ಕಣಗಳು ಪರಮಾಣುವಿನ ಬೀಜಕಣದಲ್ಲಿರುತ್ತವೆ ಮತ್ತು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಅದರ ಸುತ್ತ ಕಕ್ಷೆಗಳಲ್ಲಿ ಸುತ್ತತ್ತವೆ. ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಬೀಜಕಣದ ಸುತ್ತ ಹೇಗೆ ಸುತ್ತುತ್ತವೆ ಎಂದು ಎಲೆಕ್ಟ್ರಾನ್ ವಿನ್ಯಾಸ ವಿವರಿಸುತ್ತದೆ. ಇದು ಹೊಸ ಪರಮಾಣು ಮಾದರಿಯ ರೂಪರೇಖೆ.
ಉಲ್ಲೇಖಗಳು ಮತ್ತು ಟಿಪ್ಪಣಿ
[ಬದಲಾಯಿಸಿ]- ↑ Wikipedia en:Atomic number ಆಧಾರ. ಇದರ ಉಲ್ಲೇಖಗಳನ್ನು ಪ್ರತ್ಯೇಕವಾಗಿ ತೋರಿಸಿಲ್ಲ
- ↑ ದ್ಯವ್ಯರಾಶಿಯ ತೂಕವು ಬೀಜಕಣಗಳು ಒಳಗೊಂಡ ಪ್ರೋಟಾನ್ ಮತ್ತು ನ್ಯೂಟ್ರಾನ್ ಕಣಗಳ ತೂಕಕ್ಕಿಂತ ಕಡಿಮೆ ಇರುತ್ತದೆ. ಬೀಜಕಣ ರೂಪಗೊಳ್ಳುವಾಗ ಶಕ್ತಿಯು ಬಿಡುಗಡೆಯಾಗುವ ಇದಕ್ಕೆ ಕಾರಣ ಎನ್ನಲಾಗಿದೆ
- ↑ Wikipedia en: Periodic table access date 2016-10-10
- ↑ ಬೋರ್ ಪರಮಾಣುಗಳು ಸೂಸುವ ಕಿರಣಗಳ ರೋಹಿತ ಸಾಲುಗಳು ಅಥವಾ ಸ್ಪೆಕ್ಟ್ರಲ್ ಲೈನ್ಗಳ ಆವರ್ತನ (ಫ್ರೀಕ್ವೆನ್ಸಿ) Z ಸಂಖ್ಯೆಯ ವರ್ಗ ಅಥವಾ ಸ್ಕ್ವಯರ್ನ ಅನುಪಾತದಲ್ಲಿರುತ್ತವೆ ಎಂದು ಸಿದ್ಧಾಂತೀಕರಿಸಿದ್ದ
- ↑ "Leading up to Moseley: X-Ray Spectra" access date 2016-10-10
- ↑ "Moseley's Discovery - The Modern Concept of Atomic Number" access date 2016-10-10
- ↑ "The story of Moseley and X-rays" Archived 2016-11-08 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., Department of Physics, University of Oxford, access date 2016-10-10
- ↑ ೮.೦ ೮.೧ ಎರಡು ಪ್ರೋಟಾನು ಮತ್ತು ಎರಡು ನ್ಯೂಟ್ರಾನುಗಳಿರುವ ಹೀಲಿಯಮ್ ಬೀಜಕಣ
- ↑ ೯.೦ ೯.೧ Wikipedia en:Discovery of the neutron access date 2016-10-10
