ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ

ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರವು ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಮತ್ತು ಅವುಗಳ ರೂಪಾಂತರಗಳ ರಚನೆ, ಲಕ್ಷಣಗಳು, ಸಂಯೋಜನೆ, ಕ್ರಿಯೆ ಹಾಗೂ ಸಿದ್ಧತೆ (ಸಂಯೋಗ ಅಥವಾ ಇತರ ರೀತಿಯಾಗಿ) ಮುಂತಾದುವುಗಳ ವೈಜ್ಞಾನಿಕ ಅಧ್ಯಯನವನ್ನೊಳಗೊಂಡ ರಸಾಯನಶಾಸ್ತ್ರದೊಳಗಿನ ಪ್ರತ್ಯೇಕ ಶಾಖೆ. ಇಂಗಾಲ ಮತ್ತು ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಅಭ್ಯಾಸ ಮಾಡುವ ವಿಭಾಗ. ಈ ಸಂಯುಕ್ತಗಳು ಜಲಜನಕ, ಸಾರಜನಕ, ಆಮ್ಲಜನಕ, ಹಾಲೋಜನ್ಗಳು ಹಾಗೂ ರಂಜಕ, ಸಿಲಿಕಾನ್ ಮತ್ತು ಗಂಧಕಗಳೂ ಸೇರಿದಂತೆ ಯಾವುದೇ ಸಂಖ್ಯೆಯ ಇತರ ಅಂಶಗಳನ್ನು ಹೊಂದಿರಬಹುದು.[೧][೨][೩] ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ವೈವಿಧ್ಯಮಯ ರಚನೆಯನ್ನು ಹೊಂದಿದ್ದು, ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳಿಂದ ಪಡೆಯಬಹುದಾದ ಅನುಕೂಲಗಳ ವ್ಯಾಪ್ತಿ ಅಗಾಧ. ಅನೇಕ ಉತ್ಪನ್ನಗಳು ಮೂಲಾಧಾರ ಅಥವಾ ಪ್ರಮುಖ ಅಂಶಗಳಾಗಿರುವುದಲ್ಲದೇ (ಹೆಸರಿಸಬಹುದಾದ ಕೆಲವೆಂದರೆ ಬಣ್ಣಗಳು, ಪ್ಲಾಸ್ಟಿಕ್, ಆಹಾರ, ಸ್ಫೋಟಕಗಳು, ಔಷಧಸಾಮಗ್ರಿಗಳು, ಪೆಟ್ರೋಲಿಯಂ ರಾಸಾಯನಿಕಗಳು) ಕೆಲ ಅಪವಾದಗಳನ್ನು ಬಿಟ್ಟರೆ ಬಹುತೇಕ ಭೂಮಿಯ ಎಲ್ಲಾ ಜೀವ ಪ್ರಕ್ರಿಯೆಗಳಿಗೆ ಮೂಲಾಧಾರವಾಗಿವೆ. ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರವು ಕೂಡಾ, ವಿಜ್ಞಾನದ ಇತರ ಶಾಖೆಗಳಂತೆಯೇ ನಿರ್ದಿಷ್ಟ ನಾವೀನ್ಯತೆಯ ಅಲೆಗಳೊಂದಿಗೆ ವಿಕಾಸಗೊಂಡಿದೆ. ಈ ನಾವೀನ್ಯತೆಗಳಿಗೆ ಪ್ರಾಯೋಗಿಕ ಪರಿಗಣನೆಗಳು ಹಾಗೂ ಸೈದ್ಧಾಂತಿಕ ನಾವೀನ್ಯತೆಗಳು ಪ್ರಚೋದನೆ ನೀಡಿವೆ. ಆದಾಗ್ಯೂ ಈ ಕ್ಷೇತ್ರವು ಪಾಲಿಮರ್ ವಿಜ್ಞಾನ, ಔಷಧೀಯ ರಸಾಯನಶಾಸ್ತ್ರ, ಹಾಗೂ ಕೃಷಿರಾಸಾಯನಿಕಗಳ ಉದ್ಯಮಗಳಲ್ಲಿನ ಬೃಹತ್ ಅನ್ವಯಗಳಿಂದಾಗಿ ಆರ್ಥಿಕ ಬಲವನ್ನು ಹೊಂದಿದೆ.
ಪದ ವ್ಯುತ್ಪತ್ತಿ
[ಬದಲಾಯಿಸಿ]ಜೀವಜನ್ಯ, ಎಂದರೆ ಸಸ್ಯ ಮತ್ತು ಪ್ರಾಣಿಜನ್ಯ ಸಂಯುಕ್ತಗಳ ಅಭ್ಯಾಸ ಮಾಡುವ ರಸಾಯನಶಾಸ್ತ್ರ ವಿಭಾಗವನ್ನು ಮೊದಲು ಸಾವಯವ (ಆರ್ಗ್ಯಾನಿಕ್) ರಸಾಯನಶಾಸ್ತ್ರವೆಂದು ಕರೆಯುತ್ತಿದ್ದರು. ಅಂದಿನ ವಿಜ್ಞಾನಿಗಳು ಜೀವದ ನೆರವಿಲ್ಲದೆ ಈ ಬಗೆಯ ಸಂಯುಕ್ತಗಳ ತಯಾರಿಕೆ ಸಾಧ್ಯವೇ ಇಲ್ಲವೆಂದು ನಂಬಿದ್ದುದರಿಂದ ಈ ಹೆಸರು ಬಂತು.
ಇತಿಹಾಸ
[ಬದಲಾಯಿಸಿ]
ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳನ್ನು ಅವುಗಳ ಆಕರಗಳಿಂದ ಬೇರ್ಪಡಿಸಿ ಪರೀಕ್ಷಿಸುವುದು, ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಪರಿವರ್ತನೆಗಳ ಅಭ್ಯಾಸ ಇವು ಬಲು ಹಿಂದಿನಿಂದಲೂ ಪ್ರಚಲಿತವಿದ್ದುವು. ಉದಾಹರಣೆಗೆ ಕೆಲವೊಂದು ಮದ್ಯಸಾರಗಳ ತಯಾರಿಕೆಯನ್ನು ಸಾಧಾರಣವಾಗಿ ೯ನೆಯ ಶತಮಾನದವರೆಗೂ ಗುರುತಿಸಲಾಗಿದೆ.
ಪ್ರಕೃತಿಯಲ್ಲಿ ದೊರೆಯುವ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಕ್ರಮಬದ್ಧ ತಯಾರಿಕೆ ಮತ್ತು ಅಧ್ಯಯನಗಳು ಆರಂಭವಾದದ್ದು ೧೮ನೆಯ ಶತಮಾನದಲ್ಲಿ. ಶೀಲೆ ಎಂಬ ವಿಜ್ಞಾನಿ ಟಾರ್ಟಾನಿಕ್, ಆಕ್ಸಾಲಿಕ್, ಸಿಟ್ರಿಕ್, ಮ್ಯಾಲಿಕ್, ಮ್ಯೂಸಿಕ್ ಮತ್ತು ಲ್ಯಾಕ್ಟಿಕ್ ಆಮ್ಲಗಳನ್ನು ಬೇರ್ಪಡಿಸಿ ಅವುಗಳ ಗುಣ ಲಕ್ಷಣಗಳನ್ನು ಪರೀಕ್ಷಿಸಿದ (೧೭೬೯-೧೭೮೫); ಪ್ರಾಣಿಮೂತ್ರದಲ್ಲಿರುವ ಯೂರಿಯವನ್ನು ಬೇರ್ಪಡಿಸಿದ (೧೭೭೩). ಈ ಬಗೆಯ ಹಲವಾರು ಸಂಯುಕ್ತಗಳು ದೊರೆತ ಅನಂತರ ಇವುಗಳ ಗುಣ ಲಕ್ಷಣಗಳು ಖನಿಜಜನ್ಯ ಸಂಯುಕ್ತಗಳ ಗುಣ ಲಕ್ಷಣಗಳಿಗಿಂತ ಭಿನ್ನವಾದುವುಗಳೆಂದು ಕಂಡುಕೊಂಡ ವಿಜ್ಞಾನಿಗಳು ಈ ಸಂಯುಕ್ತಗಳ ರಸಾಯನಶಾಸ್ತ್ರವನ್ನು ಪ್ರತ್ಯೇಕವಾಗಿ ಅಭ್ಯಸಿಸತೊಡಗಿದರು.
೧೯ನೆಯ ಶತಮಾನದ ಆದಿಭಾಗದಲ್ಲಿ ಬರ್ಜ಼ೀಲಿಯಸ್ ಈ ವಿಭಾಗವನ್ನು ಸಾವಯವ ರಸಾಯನಶಾಸ್ತ್ರವೆಂದು ಕರೆದ. ಮುಖ್ಯವಾಗಿ ಕೇವಲ ನಾಲ್ಕು ಧಾತುಗಳಿಂದ-ಎಂದರೆ ಇಂಗಾಲ (ಕಾರ್ಬನ್), ಜಲಜನಕ (ಹೈಡ್ರೊಜನ್), ಆಮ್ಲಜನಕ (ಆಕ್ಸಿಜನ್) ಮತ್ತು ಸಾರಜನಕಗಳಿಂದ (ನೈಟ್ರೊಜನ್) ಬಲುಮಟ್ಟಿನ ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ತಯಾರಾಗಿವೆಯೆಂದು ಲವಾಸ್ಯೆ ಈ ಸಂಯುಕ್ತಗಳ ವಿಶ್ಲೇಷಣದಿಂದ ತೋರಿಸಿದ. ಅದುವರೆಗೆ ನಿರವಯವ ಲವಣಗಳನ್ನು (ಇನಾರ್ಗ್ಯಾನಿಕ್ ಸಾಲ್ಟ್ಸ್) ತಯಾರಿಸಲು ಉಪಯೋಗಿಸುತ್ತಿದ್ದ ಯಾವ ಕ್ರಿಯೆ, ವಿಧಾನಗಳಿಂದಲೂ ಈ ಸಂಯುಕ್ತಗಳನ್ನು ತಯಾರಿಸಲು ಸಾಧ್ಯವಾಗುತ್ತಿರಲಿಲ್ಲ. ಆದ್ದರಿಂದ ಜೈವಿಕ ಸಸ್ಯ ಮತ್ತು ಪ್ರಾಣಿಗಳಲ್ಲಿರುವ ಜೀವಶಕ್ತಿಯ ನೆರವಿಲ್ಲದೆ ಇಂಥವನ್ನು ತಯಾರಿಸುವುದು ಅಸಾಧ್ಯವೆಂದು ಭಾವಿಸಲಾಯಿತು.
ಹತ್ತೊಂಬತ್ತನೇ ಶತಮಾನದ ಆರಂಭದಲ್ಲಿ, ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞರು ಸಾಧಾರಣವಾಗಿ ಜೀವಿಗಳಿಂದ ಪಡೆಯುವ ಸಂಯುಕ್ತಗಳನ್ನು ಕೃತಕವಾಗಿ ಪಡೆಯಲು ಕಷ್ಟಸಾಧ್ಯವಾಗುವಷ್ಟು ವಿಪರೀತ ಸಂಕೀರ್ಣತೆಯನ್ನು ಹೊಂದಿವೆ ಎಂಬ ಆಲೋಚನೆ ಹೊಂದಿದ್ದರು. ಜೀವತತ್ವವಾದದ ಪ್ರಕಾರ, ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ವಸ್ತುಗಳು "ಜೀವಶಕ್ತಿ"ಯನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಅವರು ಈ ಸಂಯುಕ್ತಗಳನ್ನು "ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ" ಎಂದು ಕರೆದು ಅಧ್ಯಯನಕ್ಕೆ ಸುಲಭವಾಗುವಂತಹ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ವಸ್ತುಗಳ ಮೇಲೆ ಕೇಂದ್ರೀಕೃತವಾಗಿ ತಮ್ಮ ಪರಿಶೋಧನೆಗಳನ್ನು ಆರಂಭಿಸಿದರು.
ಹತ್ತೊಂಬತ್ತನೇ ಶತಮಾನದ ಪ್ರಥಮಾರ್ಧ ಅವಧಿಯಲ್ಲಿ, ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳನ್ನು ವಾಸ್ತವಿಕವಾಗಿ ಪ್ರಯೋಗಶಾಲೆಯಲ್ಲಿ ಕೃತಕವಾಗಿ ಸೃಷ್ಟಿಸಬಹುದೆಂಬುದು ಸ್ಪಷ್ಟವಾಯಿತು. ೧೮೧೬ರ ವೇಳೆಗೆ ಮೈಕೆಲ್ ಚೆವ್ರೆಲ್ ಅನೇಕ ವಿಧದ ಕೊಬ್ಬಿನಂಶಗಳು ಹಾಗೂ ಕ್ಷಾರವಸ್ತುಗಳಿಂದ ಮಾಡಿದ ಸಾಬೂನುಗಳ ಅಧ್ಯಯನವನ್ನು ಆರಂಭಿಸಿದ್ದರು. ಅವರು ಕ್ಷಾರದೊಂದಿಗೆ ಸೇರಿಸಿದಾಗ ಸಾಬೂನು ಉತ್ಪಾದನೆಯಾಗುವಂತಹ ಬೇರೆ ಬೇರೆ ಆಮ್ಲಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಿದರು. ಇವೆಲ್ಲವೂ ಪ್ರತ್ಯೇಕ ಸಂಯುಕ್ತಗಳಾದ ಕಾರಣ, (ರೂಢಿಗತವಾಗಿ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಮೂಲಗಳಿಂದ ಸಿಗುವ) ಅನೇಕ ಕೊಬ್ಬಿನಂಶದ ವಸ್ತುಗಳಲ್ಲಿ ರಾಸಾಯನಿಕ ಬದಲಾವಣೆ ಮಾಡಿ "ಜೀವಶಕ್ತಿ"ಯಿಲ್ಲದ ನವೀನ ಸಂಯುಕ್ತಗಳನ್ನು ಪಡೆಯಲು ಸಾಧ್ಯ ಎಂದು ನಿದರ್ಶನದ ಮೂಲಕ ತೋರಿಸಿದರು. ಫ್ರೆಡ್ರಿಕ್ ವೊಹ್ಲರ್ ಸಯನೋಜೆನ್ನಿನಿಂದ (C2N2) ಆಕ್ಸಾಲಿಕ್ ಆಮ್ಲವನ್ನೂ (COOH)2 (೧೮೨೪), ೧೮೨೮ರಲ್ಲಿ ಮೂತ್ರದ ಅಂಶವಾದ ಯೂರಿಯಾ ಎಂಬ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ರಾಸಾಯನಿಕ (ಕಾರ್ಬಮೈಡ್)ವನ್ನು, ಅಜೈವಿಕ/ಅಸಾವಯವ ಅಮೋನಿಯಮ್ ಸೈನೇಟ್ನಿಂದ NH4OCN, ಉತ್ಪಾದಿಸಿದರು. ಈ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಈಗ ವೊಹ್ಲರ್ ಸಂಶ್ಲೇಷಣೆಯೆಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಇದೇ ಅವಧಿಯಲ್ಲಿ ಹಾಗೂ ನಂತರ ಕೂಡಾ ವೊಹ್ಲರ್ರು, ಜೀವ ಶಕ್ತಿ ಸಿದ್ಧಾಂತವನ್ನು ಅಸಿಂಧು ಎಂದು ಸಾಧಿಸಿದೆನೆಂದು ಹೇಳುವ ಎಚ್ಚರ ತೋರಿದರೂ, ಇತಿಹಾಸಕಾರರು ಇದನ್ನೊಂದು ನಿರ್ಣಾಯಕ ಘಟ್ಟವೆಂಬಂತೆ ಪರಿಗಣಿಸಿದರು.
೧೮೪೮ರ ವೇಳೆಗೆ ಅನೇಕ ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ವಿಶ್ಲೇಷಣೆ, ಸಂಶ್ಲೇಷಣೆಗಳು ನಡೆದಿದ್ದು ಇಂಗಾಲ ಎಲ್ಲ ಸಾವಯವ ಸಂಯುಕ್ತಗಳಲ್ಲಿನ ಆವಶ್ಯಕ ಧಾತುವೆಂದು ತಿಳಿದುಬಂತು. ಇಂದು ಈ ವಿಭಾಗದಲ್ಲಿ ಜೀವಜನ್ಯ ಸಂಯುಕ್ತಗಳು ಮಾತ್ರವಲ್ಲದೆ ಅನೇಕ ಕೃತಕವಾಗಿ ತಯಾರಿಸಿದ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಸಂಶ್ಲೇಷಣೆ, ಅಧ್ಯಯನಗಳು ಸೇರಿವೆ. ಆದರೆ ಮೊದಲೇ ತಿಳಿಸಿದಂತೆ ಈ ವಿಭಾಗದಲ್ಲಿ ಇಂಗಾಲಸಂಯುಕ್ತಗಳೆಲ್ಲವೂ ಸೇರುವುದಿಲ್ಲ. ಸರಳ ಮತ್ತು ಖನಿಜ ಸಂಬಂಧವಾದ ಸಂಯುಕ್ತಗಳಾದ ಇಂಗಾಲದ ಆಕ್ಸೈಡುಗಳು, ಕಾರ್ಬಾನಿಕ್ ಆಮ್ಲ ಮತ್ತು ಅದರ ಲವಣಗಳು, ಹೈಡ್ರೊಸಯನಿಕ್ ಆಮ್ಲ ಮತ್ತು ಅದರ ಲವಣಗಳು, ಸಯನೇಟುಗಳೇ ಮೊದಲಾದುವುಗಳು ನಿರವಯವ (ಇನಾರ್ಗ್ಯಾನಿಕ್) ರಸಾಯನ ಶಾಸ್ತ್ರದ ಗುಂಪಿಗೆ ಸೇರುತ್ತವೆ. ಇಂಗಾಲ ಸಂಯುಕ್ತ ರಸಾಯನಶಾಸ್ತ್ರ ವಿಭಾಗದಲ್ಲಿ ಸೇರಿರುವ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಸಾಮಾನ್ಯವಾಗಿ ಎಲ್ಲದರಲ್ಲಿಯೂ ಇಂಗಾಲದೊಡನೆ ಜಲಜನಕವೂ ಇದ್ದೇ ಇರುತ್ತದೆ.
೧೮೫೬ರಲ್ಲಿ ವಿಲಿಯಂ ಹೆನ್ರಿ ಪರ್ಕಿನ್, ಕ್ವಿನೈನ್ ಅನ್ನು ಉತ್ಪಾದಿಸಲು ಪ್ರಯತ್ನಿಸಿದಾಗ, ಆಕಸ್ಮಿಕವಾಗಿ ಪರ್ಕಿನ್ರ ಕೆನ್ನೀಲಿ ವರ್ಣ ಎಂದೇ ಈಗ ಪರಿಚಿತವಾಗಿರುವ, ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ವರ್ಣದ್ರವ್ಯವನ್ನು ಉತ್ಪಾದಿಸಿದಾಗ, ಅದರಿಂದ ಹರಿದ ಹಣದ ಹೊಳೆ ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಆಸಕ್ತಿಯನ್ನು ಹೆಚ್ಚಿಸಿದ್ದು ಮತ್ತೊಂದು ಪ್ರಮುಖ ಮೈಲಿಗಲ್ಲಾಗಿತ್ತು.
ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಾದ ನಿರ್ಣಾಯಕ ಪ್ರಗತಿಯೆಂದರೆ ೧೮೫೮ರಲ್ಲಿ ಫ್ರೆಡ್ರಿಕ್ ಆಗಸ್ಟ್ ಕೆಕುಲೆ ಹಾಗೂ ಆರ್ಚಿಬಾಲ್ಡ್ ಸ್ಕಾಟ್ ಕೂಪರ್ ಇಬ್ಬರೂ ಪ್ರತ್ಯೇಕವಾಗಿ ಏಕಕಾಲದಲ್ಲಿ ಸಿದ್ಧಪಡಿಸಿದ ರಾಸಾಯನಿಕ ಸಂರಚನೆಯ ಕಲ್ಪನೆ. ಇಬ್ಬರೂ ಸಂಯೋಗ ಸಾಮರ್ಥ್ಯ ನಾಲ್ಕನ್ನು ಹೊಂದಿರುವ ಇಂಗಾಲದ ಅಣುಗಳು ಪರಸ್ಪರ ಸಂಪರ್ಕಿಸಿಕೊಂಡು ಇಂಗಾಲದ ಜಾಲಕವನ್ನು ರೂಪಿಸಬಲ್ಲವು ಹಾಗೂ ಅಣುಗಳ ಬಂಧಕಶಕ್ತಿಯ ವಿವರಣಾತ್ಮಕ ವಿನ್ಯಾಸಗಳನ್ನು ಸಮರ್ಪಕ ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳ ಪರಿಣತ ಗ್ರಹಿಕೆಗಳ ಮೂಲಕ ಗ್ರಹಿಸಲು ಸಾಧ್ಯ ಎಂಬ ಅಭಿಪ್ರಾಯ ವ್ಯಕ್ತಪಡಿಸಿದ್ದರು.
ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಇತಿಹಾಸವು ಪೆಟ್ರೋಲಿಯಂನ ಆವಿಷ್ಕಾರ ಹಾಗೂ ಕುದಿಯುವ ಬಿಂದುವಿನ ವ್ಯಾಪ್ತಿಯ ಪ್ರಕಾರ ಭಿನ್ನಾಂಕಗಳಾಗಿ ಪ್ರತ್ಯೇಕಿಸುವುದರೊಂದಿಗೆ ಮುಂದುವರೆಯಿತು. ವಿವಿಧ ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳ ಮೂಲಕ ವಿವಿಧ ಸಂಯುಕ್ತ ನಮೂನೆಗಳು ಅಥವಾ ವಿಶಿಷ್ಟ ಸಂಯುಕ್ತಗಳ ಪರಿವರ್ತನೆಯ ಸಾಧ್ಯತೆಯು ಪೆಟ್ರೋಲಿಯಂ ರಸಾಯನಶಾಸ್ತ್ರವೆಂಬ ಶಾಖೆಯನ್ನು ರಚಿಸಿ ಅದರಿಂದಾಗಿ ಪೆಟ್ರೋಲಿಯಂ ರಾಸಾಯನಿಕ ಉದ್ಯಮದ ಹುಟ್ಟಿಗೆ ಕಾರಣವಾಯಿತು. ಈ ಉದ್ಯಮವು ಕೃತಕ ರಬ್ಬರ್ಗಳು, ವಿವಿಧ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಗೋಂದುಗಳು, ಲಕ್ಷಣಗಳನ್ನು ಬದಲಿಸಬಲ್ಲ ಪೆಟ್ರೋಲಿಯಂ ಸಂಯೋಜಕಗಳನ್ನು ಹಾಗೂ ಪ್ಲಾಸ್ಟಿಕ್ಅನ್ನು ಯಶಸ್ವಿಯಾಗಿ ಉತ್ಪಾದಿಸಿತು.
ಔಷಧ ಉದ್ಯಮವು ೧೯ನೇ ಶತಮಾನದ ಕೊನೆಯ ದಶಕದಲ್ಲಿ (ಆಸ್ಪಿರಿನ್ ಎಂದು ಜನಪ್ರಿಯವಾಗಿರುವ) ಅಸಿಟೈಲ್ಸಲಿಸೈಕ್ಲಿಕ್ ಆಮ್ಲದ ಉತ್ಪಾದನೆಯನ್ನು ಬೇಯರ್ ಸಂಸ್ಥೆಯು ಜರ್ಮನಿಯಲ್ಲಿ ಆರಂಭಿಸಿದಾಗ ಆರಂಭವಾಯಿತು. ಪ್ರಥಮ ಬಾರಿಗೆ ಆರ್ಸೆಫೆನಾಮೈನ್ (ಸಾಲ್ವರ್ಸನ್)ನೊಂದಿಗೆ ಔಷಧಿಯೊಂದನ್ನು ವ್ಯವಸ್ಥಿತವಾಗಿ ಸುಧಾರಿಸಲಾಯಿತು. ಅಟಾಕ್ಸಿಲ್ನ ಅಪಾಯಕಾರಿ ವಿಷದ ಅನೇಕ ರೂಪಾಂತರಗಳನ್ನು ಪೌಲ್ ಎಹ್ರ್ಲಿಚ್ ಹಾಗೂ ಆತನ ತಂಡವು ಪರೀಕ್ಷಿಸಿ ಅತ್ಯುತ್ತಮ ಪ್ರಭಾವೀ ಹಾಗೂ ವಿಷಲಕ್ಷಣಗಳುಳ್ಳ ಸಂಯುಕ್ತವನ್ನು ಉತ್ಪಾದನೆಗೆ ಆಯ್ಕೆ ಮಾಡಿತು.
ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಕ್ರಿಯೆಗಳು ಹಾಗೂ ಅನ್ವಯಗಳ ಮುಂಚಿನ ಅವಕಾಶಗಳು ಬಹುಮಟ್ಟಿಗೆ ಅದೃಷ್ಟದವಾಗಿದ್ದರೂ, ೧೯ನೇ ಶತಮಾನದ ಉತ್ತರಾರ್ಧದಲ್ಲಿ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ವ್ಯವಸ್ಥಿತ ಅಧ್ಯಯನಗಳು ನಡೆದವು. ೨೦ನೇ ಶತಮಾನದ ಆರಂಭದಲ್ಲಿ, ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಪ್ರಗತಿಯು ವಿಪರೀತ ಸಂಕೀರ್ಣತೆಯ ಅಣುಗಳ ಸಮನ್ವಯವನ್ನು ಬಹುಹಂತದ ಕ್ರಿಯೆಗಳ ಮೂಲಕ ಸಾಧಿಸಲು ಅನುವು ಮಾಡಿಕೊಟ್ಟಿತು. ಸಮಕಾಲಿಕವಾಗಿ, ಪಾಲಿಮರ್ಗಳು ಹಾಗೂ ಕಿಣ್ವಗಳು ಅತಿದೊಡ್ಡ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಅಣುಗಳು ಹಾಗೂ ಪೆಟ್ರೋಲಿಯಂ ಜೈವಿಕ ಮೂಲದ್ದು ಎಂಬುದು ಪತ್ತೆಯಾದವು. ಯಾವುದೇ ಸಂಯುಕ್ತಕ್ಕೆ ಹೊಸದಾದ ಸಮನ್ವಯದ ಹಾದಿಗಳನ್ನು ಹುಡುಕುವ ಪ್ರಕ್ರಿಯೆಗೆ ಸಂಪೂರ್ಣ ಸಮನ್ವಯ ಎನ್ನಲಾಯಿತು. ಸಂಕೀರ್ಣ ನೈಸರ್ಗಿಕ ಸಂಯುಕ್ತಗಳ ಸಂಪೂರ್ಣ ಸಮನ್ವಯವು ಯೂರಿಯಾದ ಮೂಲಕ ಆರಂಭವಾಗಿ ಹೆಚ್ಚಿನ ಸಂಕೀರ್ಣತೆಯ ಗ್ಲೂಕೋಸ್ ಹಾಗೂ ಟರ್ಪಿನಾಲ್ಗಳೊಂದಿಗೆ ಮುಂದುವರೆಯಿತು. ೧೯೦೭ರಲ್ಲಿ, ಸಂಪೂರ್ಣ ಸಮನ್ವಯವು ಗುಸ್ತಾಫ್ ಕೊಂಪ್ಪಾರು ಕರ್ಪೂರದೊಂದಿಗೆ ಸಂಪೂರ್ಣ ಸಮನ್ವಯದ ವಾಣಿಜ್ಯೀಕರಣ ಮಾಡಿದರು. ಔಷಧೀಯ ಅನುಕೂಲಗಳು ಗಮನಾರ್ಹ ಪ್ರಮಾಣದಲ್ಲಿದ್ದವು, ಉದಾಹರಣೆಗೆ ಕೊಲೆಸ್ಟರಾಲ್-ಸಂಬಂಧಿ ಸಂಯುಕ್ತಗಳು ಸಂಕೀರ್ಣ ಮಾನವ ಹಾರ್ಮೋನ್ಗಳು ಹಾಗೂ ಅವುಗಳ ರೂಪಾಂತರಗಳ ಸಮನ್ವಯಕ್ಕೆ ಮಾರ್ಗ ತೆರೆದಿವೆ. ೨೦ನೇ ಶತಮಾನದ ಆರಂಭದಿಂದ, ಲೈಸರ್ಜಿಕ್ ಆಮ್ಲ ಹಾಗೂ B12 ಜೀವಸತ್ವದಂತಹ ಸಂಪೂರ್ಣ ಸಮನ್ವಯಗಳ ಸಂಕೀರ್ಣತೆಯು ಹೆಚ್ಚುತ್ತಿದೆ. ಇಂದಿನ ಗುರಿಗಳು ಅಸಮ್ಮಿತಿಯ ಸಮನ್ವಯಗಳೊಂದಿಗೆ ಸೂಕ್ತವಾಗಿ ಸಮನ್ವಯಗೊಳಿಸಲೇಬೇಕಾದ ಹತ್ತಾರು ಸ್ಟೀರಿಯೋಜೆನಿಕ್ ಕೇಂದ್ರಗಳನ್ನು ಹೊಂದಿವೆ.
ಜೀವಿಗಳ ರಚನೆ ಹಾಗೂ, ವಿಟ್ರೋದಲ್ಲಿನ ಪರಸ್ಪರ ವರ್ತನೆ ಹಾಗೂ ಜೀವಿಗಳ ಆಂತರಿಕ ವ್ಯವಸ್ಥೆಗಳ ರಸಾಯನಶಾಸ್ತ್ರವಾದ ಜೈವಿಕರಸಾಯನಶಾಸ್ತ್ರವು ಕೇವಲ ೨೦ನೇ ಶತಮಾನದಲ್ಲಷ್ಟೇ ಆರಂಭವಾಗಿದೆ, ಹೆಚ್ಚಿನ ವ್ಯಾಪ್ತಿಯ ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಹೊಸದೊಂದು ಅಧ್ಯಾಯವನ್ನೇ ತೆರೆದಿದೆ. ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದಂತೆಯೇ, ಜೈವಿಕರಸಾಯನಶಾಸ್ತ್ರವು ಕೂಡಾ ಇಂಗಾಲವನ್ನು ಹೊಂದಿರುವ ಸಂಯುಕ್ತಗಳ ಮೇಲೆ ಕೇಂದ್ರೀಕೃತವಾಗಿದೆ.
ಅಸಂಖ್ಯಾತ ಇಂಗಾಲದ ಸಂಯುಕ್ತಗಳಿಗೆ ಕಾರಣ
[ಬದಲಾಯಿಸಿ]ಇಂಗಾಲದ ಸಂಯುಕ್ತಗಳು ಅಸಂಖ್ಯಾತ ಸಂಖ್ಯೆಯಲ್ಲಿರಲು ಕಾರಣವನ್ನು ವಿವೇಚಿಸುವಾಗ ಅದರ ಸಂಯೋಗದ ಬಗೆ ಇತರ ಧಾತುಗಳ ಸಂಯೋಗದ ಬಗೆಗಿಂತಲೂ ಭಿನ್ನವಾದುದೆಂದು ತಿಳಿದುಬರುತ್ತದೆ. ನಾಲ್ಕು ವೇಲೆನ್ಸಿ ಎಲೆಕ್ಟ್ರಾನುಗಳನ್ನು ಪಡೆದಿರುವ ಇಂಗಾಲ ಸ್ಥಿರ ಅಯಾನ್ (ಸ್ಟೇಬಲ್ ಅಯಾನ್) ಆಗಲು ನಾಲ್ಕು ವಿದ್ಯುತ್ಕಣಗಳನ್ನು ಕಳೆದುಕೊಳ್ಳಬೇಕು, ಇಲ್ಲವೇ ನಾಲ್ಕನ್ನು ಗಳಿಸಬೇಕು. ಅಯಾನ್ ಸೃಷ್ಟಿಯಾಗಲು ಅಧಿಕಶಕ್ತಿಬೇಕು. ಆದ್ದರಿಂದಲೇ ಇಂಗಾಲಸಂಯುಕ್ತಗಳಲ್ಲಿ ಇಂಗಾಲ ಅಯಾನ್ ರೂಪದಲ್ಲಿರುವುದಿಲ್ಲ; ಮತ್ತು ಇಂಗಾಲಸಂಯುಕ್ತಗಳಲ್ಲಿ ಬಂಧಗೊಂಡಿರುವ ಪರಮಾಣುಗಳ ನಡುವೆ ವಿದ್ಯುದಂಶದ ಬೇರ್ಪಡೆಯೂ (ಚಾರ್ಜ್ ಸೆಪರೇಷನ್) ಅಧಿಕವಾಗಿರುವುದಿಲ್ಲ. ಬಂಧವೊಂದರ ನಿರ್ಮಾಣಕ್ಕಾಗಿ ಅವಶ್ಯಕವಾಗಿರುವ ವಿದ್ಯುತ್ಕಣಗಳ ವಿದ್ಯುದಂಶಗಳು ಬಂಧಗೊಂಡಿರುವ ಎರಡು ಪರಮಾಣುಗಳ ನಡುವೆ ಹೆಚ್ಚುಕಡಿಮೆ ಸರಿಸಮವಾಗಿ ಹಂಚಿ ಹೋಗಿರುತ್ತವೆ. ಇಂಥ ಬಂಧನಗಳಲ್ಲಿ ಅಸಮಾಂಗತ್ವ (ಅಸಿಮೆಟ್ರಿ) ಅತ್ಯಲ್ಪವಾದುದರಿಂದ ಇವುಗಳ ಬಂಧ ಅಧಿಕ. ಈ ಕಾರಣದಿಂದಲೇ ಇಂಗಾಲಸಂಯುಕ್ತಗಳ ಸ್ಥಿರತೆಯೂ ಹೆಚ್ಚು. ಈ ತರಹದ ಸರಿಸಮ ವಿದ್ಯುದಂಶ ಅಥವಾ ವಿದ್ಯುತ್ಕಣಗಳ ಹಂಚಿಕೆಯಿಂದ ಪರಮಾಣುಗಳ ನಡುವೆ ಏರ್ಪಡುವ ಬಂಧದ ಹೆಸರು ಸಹ ಸಂಯೋಗಬಂಧ (ಕೋವೇಲೆಂಟ್ ಬಾಂಡ್). ಇಂಥ ಬಂಧಶಕ್ತಿಯನ್ನು ಪಡೆದಿರುವುದರಿಂದಲೇ ಇಂಗಾಲದ ಪರಮಾಣುಗಳ ನಡುವೆ ಪರಸ್ಪರ ಸ್ಥಿರಬಂಧ ಸಾಧ್ಯ. ಈ ಬಗೆಯ ಅಧಿಕಬಂಧಶಕ್ತಿಯುಳ್ಳ ಇಂಗಾಲ ಪರಮಾಣುಗಳ ಸ್ಥಿರವಾದ ಸರಣಿ (ಚೈನ್) ವೃತ್ತ (ರಿಂಗ್) ಮತ್ತು ವಿವಿಧಾಕಾರದ ಜಾಲ (ನೆಟ್ವರ್ಕ್) ರಚನೆಗಳು ಸಾಧ್ಯ. ಇಂಗಾಲದ ಪರಮಾಣುಗಳು ಇತರ ಇಂಗಾಲದ ಪರಮಾಣುಗಳೊಡನೆ ಮಾತ್ರವಲ್ಲದೆ ಇತರ ಧಾತುಗಳ ಪರಮಾಣುಗಳೊಡನೆಯೂ ಸ್ಥಿರರೀತಿಯಲ್ಲಿ ಬಂಧಗೊಳ್ಳಬಲ್ಲುವು. ಇಂಗಾಲ-ಇಂಗಾಲ ಬಂಧವಲ್ಲದೆ ಇಂಗಾಲಸಂಯುಕ್ತಗಳಲ್ಲಿನ ಮತ್ತೊಂದು ಮುಖ್ಯ ಬಂಧವಾದ ಇಂಗಾಲ-ಜಲಜನಕ ಬಂಧದಲ್ಲಿಯೂ ವಿದ್ಯುದಂಶ ತಕ್ಕಮಟ್ಟಿಗೆ ಸರಿಸಮನಾಗಿಯೇ ಹಂಚಿಕೆಯಾಗಿರುವುದರಿಂದ ಆ ಬಗೆಯ ಬಂಧವೂ ಬಹು ಸ್ಥಿರವಾದುದು.
ಏಕಬಂಧ, ದ್ವಿಬಂಧ ಮತ್ತು ತ್ರಿಬಂಧ
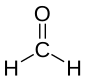
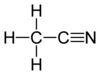
[ಬದಲಾಯಿಸಿ]ಇಂಗಾಲಸಂಯುಕ್ತಗಳಲ್ಲಿ ಪರಮಾಣುಗಳ ನಡುವಣ ಸಾಮಾನ್ಯ ಮತ್ತು ಸರಳ ಬಂಧ ಏಕಬಂಧ. ಈ ಬಗೆಯ ಬಂಧದಲ್ಲಿ ಎರಡು ಪರಮಾಣುಗಳ ನಡುವೆ ಎರಡು ವಿದ್ಯುತ್ಕಣಗಳು ಸರಿಸಮನಾಗಿ ಹಂಚಿಕೆಯಾಗಿರುತ್ತವೆ. ಇಂಗಾಲ ಮತ್ತು ಇನ್ನೊಂದು ಇಂಗಾಲ ಅಥವಾ ಇತರ ಪರಮಾಣುಗಳ ನಡುವೆ ಸಂಯೋಗಶಕ್ತಿಯ ನಿಯಮಗಳಿಗೆ ಅನುಗುಣವಾಗಿ ದ್ವಿಬಂಧ, ತ್ರಿಬಂಧಗಳೂ ಸಾಧ್ಯ. ದ್ವಿಬಂಧದಿಂದ ಕೂಡಿರುವ ಎರಡು ಪರಮಾಣುಗಳ ನಡುವೆ ನಾಲ್ಕು ವಿದ್ಯುತ್ಕಣಗಳೂ ತ್ರಿಬಂಧದಿಂದ ಕೂಡಿರುವ ಎರಡು ಪರಮಾಣುಗಳ ಮಧ್ಯೆ ಆರು ವಿದ್ಯುತ್ಕಣಗಳೂ ಹಂಚಿಕೆಯಾಗಿರುತ್ತವೆ. ಕೆಳಗೆ ತೋರಿಸಿರುವ ಮೀಥೇನ್ ಮತ್ತು ಈಥೇನ್ ಅಣುಗಳಲ್ಲಿರುವ ಎಲ್ಲ ಬಂಧಗಳೂ ಎರಡು ವಿದ್ಯುತ್ಕಣಗಳಿಂದಾದ ಏಕಬಂಧಗಳು. ಎಥಿಲೀನ್ ಮತ್ತು ಫಾರ್ಮಾಲ್ಡಿಹೈಡುಗಳು ದ್ವಿಬಂಧವನ್ನುಳ್ಳ ಸಂಯುಕ್ತಗಳು. ಅಸಿಟಲೀನ್ ಮತ್ತು ಅಸಿಟೋನೈಟ್ರಿಲ್ಲುಗಳು ತ್ರಿಬಂಧವುಳ್ಳ ಸಂಯುಕ್ತಗಳು. ರಚನೆಗಳನ್ನು ತೋರಿಸುವಾಗ ಚುಕ್ಕೆಗಳಾಗಿ ವಿದ್ಯುತ್ಕಣಗಳನ್ನಾಗಲೀ ಬಂಧಗಳನ್ನು ಸೂಚಿಸುವ ಗೆರೆಗಳನ್ನಾಗಲೀ ಉಪಯೋಗಿಸಬಹುದು. ಏಕಬಂಧನವನ್ನು ನಿರ್ದೇಶಿಸಲು ಒಂದು ಗೆರೆಯನ್ನೂ ದ್ವಿಬಂಧಕ್ಕೆ ಎರಡು ಗೆರೆಗಳನ್ನೂ ತ್ರಿಬಂಧಕ್ಕೆ ಮೂರು ಗೆರೆಗಳನ್ನೂ ಉಪಯೋಗಿಸಲಾಗುತ್ತದೆ.
- ವಿವಿಧ ಸಂಖ್ಯೆಯ ಬಂಧಗಳ ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳು
-
ಮೀಥೇನ್ ಇಂಗಾಲ-ಇಂಗಾಲ ಏಕಬಂಧ
-
ಈಥೇನ್ ಇಂಗಾಲ-ಇಂಗಾಲ ಏಕಬಂಧ
-
ಎಥಿಲೀನ್ ಇಂಗಾಲ-ಇಂಗಾಲ ದ್ವಿಬಂಧ
-
ಫಾರ್ಮಾಲ್ಡಿಹೈಡ್ ಇಂಗಾಲ-ಇಂಗಾಲ ದ್ವಿಬಂಧ
-
ಅಸಿಟಿಲೀನ್ ಇಂಗಾಲ-ಇಂಗಾಲ ತ್ರಿಬಂಧ
-
ಅಸಿಟೋನೈಟ್ರಿಲ್ ಇಂಗಾಲ-ಇಂಗಾಲ ತ್ರಿಬಂಧ
ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಏಕಬಂಧ, ದ್ವಿಬಂಧ, ತ್ರಿಬಂಧಗಳು ಯಾವುದೇ ಇರಲಿ ಪ್ರತಿ ಪರಮಾಣುವೂ ತನ್ನ ವೇಲೆನ್ಸಿ ನಿಯಮಗಳನ್ನು ಅನುಸರಿಸಲೇಬೇಕು-ಎಂದರೆ ಇಂಗಾಲದ ಪರಮಾಣುವಿನ ಬಂಧಗಳು ನಾಲ್ಕು. ಆಮ್ಲಜನಕದ ಪರಮಾಣುವಿನ ಬಂಧಗಳು ಎರಡು, ಸಾರಜನಕದ ಪರಮಾಣುವಿನ ಬಂಧಗಳು ಮೂರು-ಇವೇ ಮೊದಲಾದ ನಿಯಮಗಳ ಉಲ್ಲಂಘನೆ ಆಗುವಂತಿಲ್ಲ.
ಸಮಘಟಕತ್ವ (ಐಸೋಮೆರಿಸಂ)
[ಬದಲಾಯಿಸಿ]ಇತರ ಧಾತುಗಳ ಸಂಯುಕ್ತಗಳನ್ನು ನಿರ್ದೇಶಿಸುವಾಗ ಸಾಮಾನ್ಯವಾಗಿ ರಚನಾಸೂತ್ರಗಳನ್ನು ಬರೆಯುವುದಿಲ್ಲ; ಕೇವಲ ಅಣುಸೂತ್ರಗಳೇ ಸಾಕು. ಆದರೆ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳನ್ನು (ಕೆಲವು ಅತಿ ಸರಳವಾದುವುಗಳನ್ನು ಬಿಟ್ಟರೆ) ನಿರ್ದೇಶಿಸಲು ಅಣುಸೂತ್ರಗಳು ಸಾಲವು. ಅಣುಸೂತ್ರ ಒಂದೇ ಆಗಿದ್ದರೂ ರಚನೆಯಲ್ಲಿ ಭಿನ್ನವಾಗಿರುವ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳು ಅನೇಕವಿವೆ. ಇಂಥ ಸಂಯುಕ್ತಗಳನ್ನು ಪರಸ್ಪರ ಸಮಘಟಕಗಳೆಂದೂ (ಐಸೋಮರ್ಸ್) ಈ ವಿಶಿಷ್ಟ ಲಕ್ಷಣವನ್ನು ಸಮಘಟಕತ್ವವೆಂದೂ (ಐಸೋಮೆರಿಸಂ) ಕರೆಯಲಾಗುತ್ತದೆ.
ಹೈಡ್ರೊಕಾರ್ಬನ್ (ಜಲಜನಕೇಂಗಾಲ) ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಬ್ಯೂಟೇನ್ ಮತ್ತು ಅದಕ್ಕಿಂತ ಹಿರಿಯಗಾತ್ರದ ಅಣುಗಳಲ್ಲಿ ಸಮಘಟಕತ್ವವನ್ನು ಕಾಣಬಹುದು.
ಮೇಲೆ ಬರೆದಿರುವ ಎರಡು ಅಣುಗಳ ಅಣುಸೂತ್ರ ಒಂದೇ ಆದರೂ ಅವು ಒಂದೇ ಬಗೆಯವಲ್ಲ. ಎರಡರಲ್ಲೂ ನಾಲ್ಕು ಇಂಗಾಲಗಳಿದ್ದರೂ ಮೊದಲನೆಯದರಲ್ಲಿ ನಾಲ್ಕು ಇಂಗಾಲದ ಪರಮಾಣುಗಳೂ ಒಂದು ನೇರ ಸರಣಿಯಲ್ಲಿವೆ. ಇದು ನಾರ್ಮಲ್ ಬ್ಯೂಟೇನ್. ಎರಡನೆಯದರಲ್ಲಿ ಮೂರು ಮಾತ್ರ ಒಂದು ನೇರ ಸರಣಿಯಲ್ಲಿದ್ದು ನಾಲ್ಕನೆಯದು ಎರಡನೆಯ ಇಂಗಾಲದ ಪರಮಾಣುವಿನಿಂದ ಕವಲಾಗಿ ಸೇರಿಕೊಂಡಿದೆ. ಇದು ಐಸೋಬ್ಯೂಟೇನ್. ನಾರ್ಮಲ್ ಮತ್ತು ಐಸೋಬ್ಯೂಟೇನುಗಳೆರಡರ ಅಣುಸೂತ್ರವೂ C4H10. ಆದರೂ ಅವುಗಳ ರಚನೆಗಳು ಭಿನ್ನವಾಗಿರುವುದರಿಂದ, ಭೌತಲಕ್ಷಣಗಳಲ್ಲಿ ಮತ್ತು ರಾಸಾಯನಿಕ ಪಟುತ್ವಗಳಲ್ಲಿ ಬಹಳ ವ್ಯತ್ಯಾಸ ಕಂಡುಬರುತ್ತದೆ. ಆದ್ದರಿಂದ ಅವು ಭಿನ್ನ ಸಂಯುಕ್ತಗಳೇ ಹೊರತು ಒಂದೇ ಸಂಯುಕ್ತದ ಭಿನ್ನರೂಪಗಳಲ್ಲ. ಪುಂಜವೊಂದರ (ಮೇಲ್ಕಂಡ ಬ್ಯೂಟೇನುಗಳಲ್ಲಿ ಮೀಥೈಲ್ ಪುಂಜದ) ಸ್ಥಾನಪಲ್ಲಟನ ಈ ಬಗೆಯ ಸಮಘಟಕಗಳಲ್ಲಿರುವ ಪರಸ್ಪರ ವ್ಯತ್ಯಾಸ-ಆದ್ದರಿಂದ ಇವುಗಳ ಹೆಸರು ಸ್ಥಾನೀಯ (ಪೊಜ಼ಿಷನಲ್) ಸಮಘಟಕಗಳು. ಸ್ಥಾನೀಯ ಸಮಘಟಕತ್ವವೆಂದು ಈ ಸಮಘಟಕತ್ವದ ಹೆಸರು.
ಇನ್ನೊಂದು ರೀತಿಯ ಸಾಮಾನ್ಯ ಸಮಘಟಕತ್ವ ಕ್ರಿಯಾತ್ಮಕ ಸಮಘಟಕತ್ವ. ಎರಡು ಕ್ರಿಯಾತ್ಮಕ ಸಮಘಟಕತ್ವಗಳ ಅಣುಸೂತ್ರ ಒಂದೇ ಆಗಿದ್ದು ರಚನಾಸೂತ್ರದಲ್ಲಿ ಭಿನ್ನತೆಯಿರುವುದು ಮಾತ್ರವಲ್ಲದೆ ಇವುಗಳ ಗುಣಲಕ್ಷಣಗಳನ್ನು ನಿರ್ಣಯಿಸುವ ಕ್ರಿಯಾಪುಂಜಗಳಲ್ಲಿಯೇ (ಫಂಕ್ಷನಲ್ ಗ್ರೂಪ್) ವ್ಯತ್ಯಾಸವಿರುತ್ತದೆ. ಉದಾಹರಣೆಗೆ C2H6O ಎಂಬ ಅಣುಸೂತ್ರವಿರುವ ಎರಡು ಸಂಯುಕ್ತಗಳಿವೆ. ಇವುಗಳಲ್ಲಿ ಮೊದಲನೆಯದು OH ಅಥವಾ ಹೈಡ್ರಾಕ್ಸಿಲ್ ಕ್ರಿಯಾಪುಂಜವನ್ನುಳ್ಳ ಈಥೈಲ್ ಆಲ್ಕೊಹಾಲ್. ಎರಡನೆಯದು ಡೈಮೀಥೈಲ್ ಈಥರ್. ಇವೆರಡಕ್ಕೂ ಭೌತ ಮತ್ತು ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳಲ್ಲಿ ಬಹಳ ವ್ಯತ್ಯಾಸವಿದೆ. ಎರಡೂ ಬೇರೆ ಬೇರೆ ರಾಸಾಯನಿಕ ವರ್ಗಗಳಿಗೆ ಸೇರಿದ ಸಂಯುಕ್ತಗಳು.
ಇಂಗಾಲ ಪರಮಾಣುವಿನ ರಚನೆ ಮತ್ತು ಇಂಗಾಲಸಂಯುಕ್ತಗಳ ಆಕಾರ
[ಬದಲಾಯಿಸಿ]ಎಲ್ಲ ಪರಮಾಣುಗಳಿಗೂ ಮಧ್ಯೆ ಪರಮಾಣುಕೇಂದ್ರ ಅಥವಾ ಬೀಜ (ನ್ಯೂಕ್ಲಿಯಸ್) ಇದೆ. ಬೀಜದ ಸುತ್ತಲೂ ಋಣ ವಿದ್ಯುತ್ಕಣಗಳು ಮುಖ್ಯ ಶಕಲಕಕ್ಷೆಗಳ (ಮೇನ್ ಕ್ವಾಂಟೈಜ್ಡ್ ಆರ್ಬಿಟ್ಸ್) ಮಿತಿಯಲ್ಲಿ ನಿರ್ದಿಷ್ಟ ಕಕ್ಷೆಗಳಲ್ಲಿ ಬಲು ವೇಗವಾಗಿ ಸಂಚರಿಸುತ್ತಿರುತ್ತವೆ. ಬೀಜದ ಸುತ್ತಲಿನ ಪ್ರದೇಶದಲ್ಲಿ ಯಾವ ಎಡೆಯಲ್ಲಿ ಬೇಕಾದರೂ ವಿದ್ಯುತ್ಕಣವೊಂದು ಇರಬಹುದಾದ ಸಂಭಾವ್ಯತೆಯನ್ನು (ಪ್ರಾಬೆಬಿಲಿಟಿ) ಷ್ರೋಡಿಂಗರ್ ಸಮೀಕರಣವನ್ನು ಉಪಯೋಗಿಸಿ ತಿಳಿಯಬಹುದು. ಆವರಣವೊಂದರಲ್ಲಿ ಹೀಗೆ ಕಂಡುಹಿಡಿದ ಸಂಭಾವ್ಯತೆಯನ್ನು ಪರೀಕ್ಷಿಸಿದಾಗ ಯಾವೊಂದು ಎಡೆ ಅಥವಾ ವರ್ತುಲದಲ್ಲಿಯೂ ಪೂರ್ಣ ಸಂಭಾವ್ಯತೆ (ಎಂದರೆ ಸಂಭಾವ್ಯತೆ ೧) ಇಲ್ಲದೆ ಹೋದರೂ ಹಲವೆಡೆಗಳಲ್ಲಿ ಅದು ಹೆಚ್ಚಾಗಿದ್ದು ಅಕ್ಕಪಕ್ಕಗಳಲ್ಲಿ ಕ್ರಮೇಣ ಕಡಿಮೆಯಾಗುವುದು ತಿಳಿದುಬರುತ್ತದೆ. ವಿದ್ಯುತ್ಕಣವನ್ನು ಋಣ ವಿದ್ಯುತ್ತಿನ ಚದರಿ ಹರಡಿದ ಮೋಡದಂತೆ (ಡಿಫ್ಯೂಸ್ಡ್ ಕ್ಲೌಡ್ ಆಫ್ ಎಲೆಕ್ಟ್ರಿಸಿಟಿ) ಚಿತ್ರಿಸಿದರೆ ಸಂಭಾವ್ಯತೆ ಹೆಚ್ಚಿರುವ ಕಡೆಗಳಲ್ಲಿ ದಟ್ಟವಾಗಿಯೂ ಕಡಿಮೆಯಿರುವ ಕಡೆಗಳಲ್ಲಿ ತೆಳುವಾಗಿಯೂ ಇರುತ್ತದೆ. ಸಂಭಾವ್ಯತೆಯನ್ನು ನಿರ್ದೇಶಿಸುವ ನಕ್ಷೆಯಲ್ಲಿ ದಟ್ಟ ಮೋಡದ ನಕ್ಷೆ ಒಂದು ನಿರ್ದಿಷ್ಟ ಆಕೃತಿಯನ್ನು ತಾಳಿರುವುದು ಕಂಡುಬರುತ್ತದೆ. ಈ ನಿರ್ದಿಷ್ಟ ಆಕೃತಿಗಳು ಆಯಾ ವಿದ್ಯುತ್ಕಣಗಳ ಶಕ್ತಿ ಪ್ರತೀಕಗಳು. ಇವನ್ನು ಪರಮಾಣು ಕಕ್ಷೇಯಗಳೆಂದು (ಅಟಾಮಿಕ್ ಆರ್ಬಿಟಲ್) ಕರೆಯಲಾಗುತ್ತದೆ.[೪] ನಿರ್ದಿಷ್ಟ ಆಕೃತಿ ಪಡೆದಿರುವ ಈ ಕಕ್ಷೇಯಗಳನ್ನು ಅವುಗಳ ಆಕೃತಿ, ಶಕ್ತಮಟ್ಟಗಳಿಗೆ ಅನುಗುಣವಾಗಿ ಹೆಸರಿಸಲಾಗಿದೆ. ಇಂಗಾಲದ ಪರಮಾಣುಸ್ವರೂಪ ಮತ್ತು ಇಂಗಾಲಸಂಯುಕ್ತಗಳ ಆಕಾರವನ್ನು ಅರಿಯಲು ಪ್ರಮುಖ ಆವರಣದ (ಮೇನ್ ಶೆಲ್) ಮಿತಿಯಲ್ಲಿನ s ಮತ್ತು p ಎಂಬ ಪರಮಾಣು ಕಕ್ಷೇಯಗಳ ಆಕೃತಿಗಳನ್ನು ತಿಳಿದುಕೊಂಡರೆ ಸಾಕು. s ಕಕ್ಷೇಯ ಬೀಜದ ಸುತ್ತಲೂ ಸಮನಾಗಿ ಹರಡಿಕೊಂಡು ಪೊಳ್ಳು ಗೋಳಾಕೃತಿಯನ್ನು ಪಡೆದಿರುತ್ತದೆ.

ಮೊದಲ ಮುಖ್ಯ ವಲಯದಲ್ಲಿ ಶಕಲ ನಿಯಮಗಳಿಗೆ ಅನುಗುಣವಾಗಿ ಎರಡು ವಿದ್ಯುತ್ಕಣಗಳು ಮಾತ್ರವಿದ್ದು 1s ಪರಮಾಣು ಕಕ್ಷೇಯದಲ್ಲಿರುತ್ತವೆ. ಇವು ಇಂಗಾಲದ ರಾಸಾಯನಿಕ ಸಂಯೋಗ ಕ್ರಿಯೆಯಲ್ಲಿ ಭಾಗವಹಿಸುವುದಿಲ್ಲ. ಮುಂದಿನ ಎರಡು ವಿದ್ಯುತ್ಕಣಗಳು ಗೋಳಾಕೃತಿಯ 2s ಕಕ್ಷೇಯದಲ್ಲಿವೆ.
ಮುಂದಿನ 2p ಶಕ್ತಿಹಂತದಲ್ಲಿ ಪರಸ್ಪರ ಲಂಬಕೋನಗಳಲ್ಲಿರುವ ಮೂರು ಕಕ್ಷೇಯಗಳಿವೆ. ಪ್ರತಿ ಕಕ್ಷೇಯವೂ x,y,z ಆಕಾಶ ಅಕ್ಷಗಳ (ಸ್ಪೇಷಿಯಲ್ ಆಕ್ಸಿಸ್) ಮೇಲಿದ್ದು ಎರಡು ಭಾಗಗಳಲ್ಲಿರುತ್ತವೆ. ಇದನ್ನು Px,Py,Pz, ಕಕ್ಷೇಯಗಳೆಂದು ಕರೆದಿದೆ. Px ಕಕ್ಷೇಯದ ಎರಡು ಭಾಗಗಳು x ಅಕ್ಷದ ಮೇಲೆ ಬೀಜದ ಎಡಬಲ ಭಾಗಗಳಲ್ಲಿದ್ದು ಪ್ರತಿಭಾಗವೂ ಗೋಳಾಕಾರವಾಗಿದೆ. ಎಂದರೆ Px ನ ಪೂರ್ಣ ಆಕಾರ ಎರಡು ಗೋಳಗಳು ಬೀಜದಲ್ಲಿ ಪರಸ್ಪರ ತಗುಲಿದಂತಿದೆ. Py ಮತ್ತು Pz ಕಕ್ಷೇಯಗಳ ಆಕೃತಿಯೂ ಇದೇ ರೀತಿ ಇದೆ. ಆದರೆ ಅವುಗಳ ಇರುವಿಕೆಯ ಅಕ್ಷಗಳು y ಮತ್ತು z ಅಕ್ಷಗಳು.
ಇಂಗಾಲದ ಪರಮಾಣು ಆರು ವಿದ್ಯುತ್ಕಣಗಳನ್ನು ಪಡೆದಿದ್ದು ಅವುಗಳಲ್ಲಿ ಮೊದಲ ನಾಲ್ಕು ಯಾವ ಯಾವ ಕಕ್ಷೇಯದಲ್ಲಿ ಹಂಚಿಕೆಯಾಗಿರುತ್ತವೆಂಬುದನ್ನು ಈಗ ಅರಿತಿದ್ದೇವೆ. ಉಳಿದ ಇನ್ನೆರಡು ವಿದ್ಯುತ್ಕಣಗಳು ಸಮಾನ ಶಕ್ತಿಯನ್ನುಳ್ಳ ಎರಡು p ಕಕ್ಷೇಯಗಳಲ್ಲಿ ಒಂದೊಂದರಲ್ಲಿ ಒಂದರಂತೆ ಹಂಚಿಕೆಯಾಗಿರುತ್ತವೆ. 2s ಕಕ್ಷೇಯದಲ್ಲಿ ಎರಡು ವಿದ್ಯುತ್ಕಣಗಳಿದ್ದು ಈ ಕಕ್ಷೇಯ ಪೂರ್ಣವಾಗಿ ತುಂಬಿದೆ. ಸಂಯೋಗರೀತಿಯ ನಿಯಮಗಳಿಗನುಗುಣವಾಗಿ ಈ ವಿದ್ಯುತ್ಕಣಗಳು ಬಂಧಗಳಲ್ಲಿ ಭಾಗವಹಿಸುವಂತಿಲ್ಲ. ಇಂಗಾಲದ ಪರಮಾಣುವಿನ ವೇಲೆನ್ಸಿ 2p ಕಕ್ಷೇಯಗಳಲ್ಲಿ ಎರಡರಲ್ಲಿ ಪ್ರತಿಯೊಂದರಲ್ಲಿ ಒಂದೊಂದರಂತೆ ಇರುವ ಎರಡು ವಿದ್ಯುತ್ಕಣಗಳಲ್ಲಿ ಮಾತ್ರ ಅಡಕವಾಗಿದೆ ಎಂದಂತಾಯಿತು. ಇದರಿಂದ ಇಂಗಾಲದ ಸಂಯೋಗಶಕ್ತಿ ಎರಡೆಂದೂ p ಕಕ್ಷೇಯಗಳು ಒಂದಕ್ಕೊಂದು ಲಂಬಕೋನದಲ್ಲಿರುವುದರಿಂದ ಇಂಗಾಲದ ಬಂಧಗಳು ಒಂದಕ್ಕೊಂದು ಲಂಬಕೋನದಲ್ಲಿ ಇವೆಯೆಂದೂ ಅರಿವಾಗುತ್ತದೆ. ಆದರೆ ಇದು ಸತ್ಯಕ್ಕೆ ದೂರವಾದ ವಿಷಯ. ಇಂಗಾಲದ ವೇಲೆನ್ಸಿ ನಾಲ್ಕೆಂದೂ ನಾಲ್ಕು ಬಂಧಗಳೂ ಆಕಾಶದಲ್ಲಿ ಸಮಾನ ಕೋನಾಂತರದಲ್ಲಿ ಪಸರಿಸಿ ಇಂಗಾಲಸಂಯುಕ್ತಗಳಲ್ಲಿ ಇಂಗಾಲದ ಪರಮಾಣು ಸಮಚತುರ್ಮುಖಿಯ (ರೆಗ್ಯುಲರ್ ಟೆಟ್ರಹೆಡ್ರನ್) ಆಕಾರವನ್ನು ತಳೆದಿರುತ್ತದೆಂದೂ ಶಕಲಬಲವಿಜ್ಞಾನದ (ಕ್ವಾಂಟಂ ಮೆಕ್ಯಾನಿಕ್ಸ್) ಉಗಮಕ್ಕಿಂತಲೂ ಎಷ್ಟೋ ಮೊದಲೇ ವಿವಿಧ ಪರಿಶೀಲನೆಗಳಿಂದ ತಿಳಿದಿತ್ತು. ಆದ್ದರಿಂದ ಸಂಯುಕ್ತಗಳಲ್ಲಿರುವ ಇಂಗಾಲದ ಪರಮಾಣುವಿನ ಸ್ವರೂಪ ಮುಕ್ತ ಇಂಗಾಲ ಪರಮಾಣುವಿನ ಸ್ವರೂಪಕ್ಕಿಂತಲೂ ಭಿನ್ನವಾಗಿರಬೇಕು. ಆದರೆ ಮೇಲೆ ವಿವರಿಸಿದ 1s22s22p’xP’y ಸ್ಥಿತಿಗಿಂತ ಭಿನ್ನವಾದ ಮತ್ತಾವ ಸ್ವರೂಪವೇ ಆದರೂ ಮುಕ್ತ ಇಂಗಾಲಕ್ಕಿಂತಲೂ ಹೆಚ್ಚು ಪ್ರಚ್ಛನ್ನಶಕ್ತಿಯನ್ನು (ಪೊಟೆನ್ಯಿಯಲ್ ಎನರ್ಜಿ) ಪಡೆದಿರುತ್ತದೆ. ಕನಿಷ್ಠ ಪ್ರಚ್ಛನ್ನಶಕ್ತಿಯನ್ನುಳ್ಳ ಸ್ವರೂಪ ಇತರ ಯಾವುದೇ ಸ್ವರೂಪಕ್ಕಿಂತಲೂ ಸ್ಥಿರವಾದುದು. ಆದ್ದರಿಂದ ಹೆಚ್ಚು ಶಕ್ತಿಯ ಬಿಡುಗಡೆಗೆ ಕಾರಣವಾಗುವ ಮತ್ತೊಂದು ಘಟನೆ ಇರಬೇಕು. ಸ್ಥಿರ ಬಂಧಗಳ ನಿರ್ಮಾಣ ಇಂಥದೊಂದು ಘಟನೆ. ಪರಮಾಣುಗಳ ಕಕ್ಷೇಯಗಳು ಬಳಿಸಾರಿ ಒಂದರ ಮೇಲೊಂದು ವ್ಯಾಪಿಸಿ ಏಕವಾಗುವುದರಿಂದ ಬಂಧ ನಿರ್ಮಾಣವಾಗುತ್ತದೆ. ಹೀಗೆ ಅವು ಏಕವಾದಾಗ ಹಳೆಯ ಎರಡು ಪರಮಾಣು ಕಕ್ಷೇಯಗಳು ಮಾಯವಾಗಿ ಹೊಸದೊಂದು ಕಕ್ಷೇಯ ಸೃಷ್ಟಿಯಾಗುತ್ತದೆ. ಈ ಕಕ್ಷೇಯ ಯಾವೊಂದು ಪರಮಾಣುವಿಗೂ ಸೇರಿದುದಲ್ಲವಾದ್ದರಿಂದ ಅದನ್ನು ಅಣು ಕಕ್ಷೇಯ (ಮಾಲೆಕ್ಯುಲರ್ ಆರ್ಬಿಟಲ್) ಎಂದು ಕರೆದಿದೆ. ಸ್ಥಿರಬಂಧ ನಿರ್ಮಾಣದಲ್ಲಿ ಹೊಸ ಕಕ್ಷೇಯದ ಶಕ್ತಿ (ಎಂದರೆ ಅದರಲ್ಲಿನ ವಿದ್ಯುತ್ಕಣಗಳ ಪ್ರಚ್ಛನಶಕ್ತಿ) ಹಳೆಯ ಪರಮಾಣು ಕಕ್ಷೇಯಗಳ ಶಕ್ತಿಗಿಂತ ಕಡಿಮೆ ಇದ್ದು ಬಂಧ ನಿರ್ಮಾಣವಾಗುವಾಗ ಶಕ್ತಿ ವಿಸರ್ಜನೆಯಾಗುತ್ತದೆ. ಎರಡು ಪರಮಾಣುಗಳ ನಡುವಣ ಅಣು ಕಕ್ಷೇಯವೊಂದರಲ್ಲಿ ಎರಡಕ್ಕಿಂತ ಹೆಚ್ಚು ವಿದ್ಯುತ್ಕಣಗಳು ಇರಲು ಸಾಧ್ಯವಿಲ್ಲ. ಆದ್ದರಿಂದ ವಿದ್ಯುತ್ಕಣಗಳನ್ನುಳ್ಳ ಎರಡು ಪರಮಾಣು ಕಕ್ಷೇಯಗಳು ಬಂಧ ನಿರ್ಮಾಣಕಾರ್ಯದಲ್ಲಿ ಭಾಗವಹಿಸುವುದಾದರೆ, ಅಂಥ ಕಕ್ಷೇಯಗಳಲ್ಲಿ ಒಂದೊಂದೇ ವಿದ್ಯುತ್ಕಣವಿರಬೇಕಾಗುತ್ತದೆ. ಆದ್ದರಿಂದಲೇ ಎರಡು ವಿದ್ಯುತ್ಕಣಗಳನ್ನುಳ್ಳ ಇಂಗಾಲದ 2s ಕಕ್ಷೇಯ ಬಂಧನಿರ್ಮಾಣದಲ್ಲಿ ಪಾಲುಗೊಳ್ಳಲು ಸಾಧ್ಯವಿಲ್ಲ.
ಈಗ ಇಂಗಾಲಸಂಯುಕ್ತಗಳಲ್ಲಿ ಇಂಗಾಲ ಪರಮಾಣುವಿನ ಸ್ವರೂಪವನ್ನು ಪ್ರತ್ಯೇಕವಾಗಿ ಪರಿಶೀಲಿಸಬಹುದು. ಇಂಗಾಲದ ವೇಲೆನ್ಸಿ ೪. ಆದ್ದರಿಂದ ವೇಲೆನ್ಸಿಗೆ ಕಾರಣವಾದ ಎರಡನೆಯ ಮುಖ್ಯವಲಯದ ನಾಲ್ಕು ವಿದ್ಯುತ್ಕಣಗಳೂ ಬೇರೆ ಬೇರೆ ಕಕ್ಷೇಯಗಳಲ್ಲಿರಬೇಕು. ಹೀಗಾಗಲು 2s ಕಕ್ಷೇಯದಲ್ಲಿರುವ ವಿದ್ಯುತ್ಕಣವೊಂದು ಹೊಸ ಕಕ್ಷೇಯವನ್ನು ಪಡೆಯಬೇಕಾಗುತ್ತದೆ. ಆದ್ದರಿಂದ ಅದು ಮರುಹಂತದ ಇನ್ನೂ ತೆರವಾಗಿರುವ ಒಂದು 2p ಕಕ್ಷೇಯವನ್ನು ಸೇರುತ್ತದೆಂದು ಭಾವಿಸಬಹುದು. ಹೀಗೆ ಒಂದು ವಿದ್ಯುತ್ಕಣ ಕೆಳಗಿನ ಶಕ್ತಿಮಟ್ಟಕ್ಕಿಂತ (2s) ಹೆಚ್ಚಿನ ಶಕ್ತಿ ಮಟ್ಟಕ್ಕೆ (2p) ಏರಲು ಶಕ್ತಿಯನ್ನು ಪೂರೈಸಬೇಕಾಗುತ್ತದೆ. ಆದರೆ ಈಗ ಎರಡರ ಬದಲು ನಾಲ್ಕು ಬಂಧಗಳು ನಿರ್ಮಾಣವಾಗುವುದರಿಂದ ಶಕ್ತಿ ವಿಸರ್ಜನೆಯೂ ಹೆಚ್ಚುತ್ತದೆ. ಹೀಗೆ ವಿಸರ್ಜನೆಯಾದ ಶಕ್ತಿ ವಿದ್ಯುತ್ಕಣವೊಂದರ ಶಕ್ತಿ ಮಟ್ಟವನ್ನು ಹೆಚ್ಚಿಸಲು ಬೇಕಾಗುವುದಕ್ಕಿಂತಲೂ ಹೆಚ್ಚಾಗಿದ್ದರೆ ಭಾವಿಸಿರುವಂತೆ ಒಂದು 2s ವಿದ್ಯುತ್ಕಣದ ಶಕ್ತಿಮಟ್ಟ ಹೆಚ್ಚಿ ನಾಲ್ಕು ಬಂಧಗಳು ನಿರ್ಮಾಣವಾಗಬಹುದು. ಶಕ್ತಿ ಪರಿಗಣನೆಗಳಿಂದ ನಾಲ್ಕು ಬಂಧಗಳ ನಿರ್ಮಾಣ ಹೀಗೆ ಸಾಧ್ಯವಾದರೂ ಇಂಗಾಲಸಂಯುಕ್ತಗಳಲ್ಲಿನ ಇಂಗಾಲದ ಪರಮಾಣುವಿನ ಬಂಧಗಳು ಈ ಬಗೆಯ ಬಂಧಗಳಿಗಿಂತ ಸ್ಥಿರವಾದವುಗಳೆಂದು ಶಕಲಬಲವಿಜ್ಞಾನ ಲೆಕ್ಕಾಚಾರಗಳಿಂದ ತಿಳಿದುಬಂದಿದೆ. ಅಷ್ಟೇ ಅಲ್ಲದೆ ಬಂಧಗಳು ಈ ಬಗೆಯಾಗಿ ನಿರ್ಮಾಣವಾಗಿದ್ದಲ್ಲಿ p ಹಂತದ ವಿದ್ಯುತ್ಕಣಗಳು ಭಾಗವಹಿಸಿದ ಮೂರು ಬಂಧಗಳ ಶಕ್ತಿ ಒಂದಾಗಿದ್ದು s ಹಂತದ ವಿದ್ಯುತ್ಕಣದಿಂದಾದ ಬಂಧದ ಶಕ್ತಿ ಬೇರೆಯಾಗಿರಬೇಕಾಗಿತ್ತು. ಅಲ್ಲದೆ ಮೂರು ಬಂಧಗಳು ಒಂದಕ್ಕೊಂದು ಲಂಬಕೋನದಲ್ಲಿದ್ದು ಕಡೆಯ ಬಂಧ ದಿಗ್ರಹಿತ ಬಂಧವಾಗಿರಬೇಕಾಗಿತ್ತು. ಆದರೆ ಇಂಗಾಲದ ಬಂಧಗಳು ನಾಲ್ಕೂ ಸಮಾನ ಶಕ್ತಿಯುಳ್ಳವು ಮತ್ತು ನಾಲ್ಕರ ದಿಕ್ಕುಗಳೂ ನಿರ್ದಿಷ್ಟವಾಗಿದ್ದು ಬಂಧಗಳ ನಡುವಿನ ಕೋನಾಂತರ ೧೦೯೦೨೮’, ಆದ್ದರಿಂದ 2s ಮತ್ತು 2p ಕಕ್ಷೇಯಗಳ ಶಕ್ತಿ ಮತ್ತು ಸ್ವರೂಪಗಳಲ್ಲಿ ತೀವ್ರ ಬದಲಾವಣೆಗಳಾಗುವುದು ಆವಶ್ಯಕ.[೫] ಸಂಯುಕ್ತ ಸ್ವರೂಪದಲ್ಲಿ ತಮ್ಮ ಪ್ರಚ್ಛನ್ನಶಕ್ತಿಯನ್ನು ಆದಷ್ಟುಮಟ್ಟಿಗೆ ಕಡಿಮೆ ಮಾಡಿಕೊಳ್ಳಲು ಪರಮಾಣು ಕಕ್ಷೇಯಗಳು ಹೊಸ ವಿಧಾನವನ್ನು ಅನುಸರಿಸುತ್ತವೆ. ಕಕ್ಷೇಯಗಳ ಮೇರೆಗಳು ಹಲವು ನಿಯಮಗಳಿಗೆ ಒಳಪಟ್ಟಿದ್ದರೂ ಶಕ್ತಿಯ ಪೂರೈಕೆ ವಿಸರ್ಜನೆಗಳಿಂದ ಅವು ಬದಲಾಗಬಹುದು. ಇಂಗಾಲದ ಪರಮಾಣುವಿನ 2s ಮತ್ತು ಮೂರು 2p ಕಕ್ಷೇಯಗಳು ಮಿಶ್ರಗೊಂಡು ನಾಲ್ಕು ಹೊಸದಾದ ಸರಿಸಮ ಶಕ್ತಿ ಮತ್ತು ಆಕಾರಗಳನ್ನುಳ್ಳ ಸಂಕರ ಕಕ್ಷೇಯಗಳ (ಹೈಬ್ರಿಡ್ ಆರ್ಬಿಟಲ್ಸ್) ಸೃಷ್ಟಿಯಾಗುತ್ತದೆ. ಈ ಸಂಕರ ಕಕ್ಷೇಯಗಳ ವ್ಯಾಪ್ತಿ s ಮತ್ತು p ಕಕ್ಷೇಯಗಳೆರಡರ ವ್ಯಾಪ್ತಿಗಳಿಗಿಂತಲೂ ಹೆಚ್ಚಿದ್ದು ತಮ್ಮ ಪ್ರಭಾವವನ್ನು ಬೀಜದಿಂದ ಇನ್ನೂ ಸ್ವಲ್ಪ ಹೆಚ್ಚು ದೂರ ಹರಡಬಲ್ಲವಾದ್ದರಿಂದ ಈ ಬಗೆಯ ಕಕ್ಷೇಯಗಳು ಭಾಗವಹಿಸಿರುವ ಬಂಧಗಳು s ಅಥವಾ p ಕಕ್ಷೇಯಗಳಿಂದ ಉಂಟಾಗುವ ಬಂಧಗಳಿಗಿಂತ ಸ್ಥಿರವಾದವು-ಎಂದರೆ ಕಡಿಮೆ ಶಕ್ತಿ ಮಟ್ಟದವು ಅಥವಾ ಇವುಗಳ ನಿರ್ಮಾಣದಲ್ಲಿ ಇನ್ನೂ ಅಧಿಕ ಶಕ್ತಿ ವಿಸರ್ಜನೆಯಾಗುತ್ತದೆ.

ಶಕಲಬಲವಿಜ್ಞಾನದ ಲೆಕ್ಕಾಚಾರಗಳು ಶಕ್ತಿವೆಚ್ಚ, ಶಕ್ತಿವಿಸರ್ಜನೆಗಳೆರಡನ್ನೂ ಪರಿಗಣನೆಗೆ ತೆಗೆದುಕೊಂಡು ಈ ಬಗೆಯ sp3 ಎಂದೆನ್ನಿಸಿಕೊಳ್ಳುವ ಸಂಕರ ಕಕ್ಷೇಯಗಳಿಂದ ನಿರ್ಮಾಣವಾಗುವ ಬಂಧಗಳು ಕನಿಷ್ಠ ಶಕ್ತಿಮಟ್ಟದವೆಂದು ತೋರಿಸಿವೆ. sp3 ಸಂಕರಕಕ್ಷೇಯಗಳು ಆಕಾಶದಲ್ಲಿ ಸರಿಸಮನಾಗಿ ಹರಡಿಕೊಂಡಿದ್ದು ಯಾವುದೇ ಎರಡು ಕಕ್ಷೇಯಗಳ ನಡುವಿನ ಕೋನಾನಂತರ ೧೦೯೦೨೮’ ಆಗಿದೆ. ಇಂಗಾಲಸಂಯುಕ್ತಗಳಲ್ಲಿ ಬಂಧಗಳ ನಡುವೆ ಇದೇ ಕೋನಾಂತರ ಇರುವುದನ್ನು ಸಂಕರಕಕ್ಷೇಯಗಳ ವಾದ ಸಮರ್ಪಕವಾಗಿ ವಿವರಿಸುತ್ತದೆ. ಸಂಯುಕ್ತರೂಪದಲ್ಲಿರುವ ಇಂಗಾಲಪರಮಾಣು ಎಂದರೆ sp3 ಸಂಕರಕಕ್ಷೇಯಗಳನ್ನುಳ್ಳ ಇಂಗಾಲ ಪರಮಾಣುವನ್ನು ಸಮ ಚತುರ್ಮುಖಿಯೊಂದರ ಮಧ್ಯಭಾಗದಲ್ಲಿರುವಂತೆಯೂ ಅದರ ಬಂಧಗಳು ಅಥವಾ ಕಕ್ಷೇಯಗಳು ಚತುರ್ಮುಖಿಯ ನಾಲ್ಕು ಮೂಲೆಗಳ ಕಡೆಗೆ ಚಾಚಿಕೊಂಡಿರುವಂತೆಯೂ ಭಾವಿಸಬಹುದು.[೬] ಈ ಬಗೆಯ ನಿರೂಪಣೆ ಏಕಬಂಧಗಳನ್ನುಳ್ಳ ಇಂಗಾಲ ಪರಮಾಣುವಿನ ಸ್ವರೂಪವನ್ನು ಸಂಪೂರ್ಣವಾಗಿ ಸ್ಪಷ್ಟಪಡಿಸುತ್ತದೆ.
ಆದರೆ ದ್ವಿಬಂಧವನ್ನುಳ್ಳ ಇಂಗಾಲ ಪರಮಾಣುವಿನ ಸ್ವರೂಪ ಇದಕ್ಕಿಂತ ಭಿನ್ನವಾಗಿದ್ದು, ಇದರಲ್ಲಿ ಇಂಗಾಲದ ಸುತ್ತಲೂ ಕೇವಲ ಮೂರು ಇತರ ಪರಮಾಣುಗಳು ಒಂದೇ ಸಮತಲದಲ್ಲಿದ್ದು ಬಂಧಕೋನಗಳು (ಬಾಂಡ್ ಆಂಗಲ್ಸ್) ೧೨೦೦ ಇರುತ್ತವೆ. ದ್ವಿಬಂಧ ಪರಿಸ್ಥಿತಿಯಲ್ಲಿರುವ ಇಂಗಾಲ ಪರಮಾಣುಗಳಲ್ಲಿ ಆಗುವ ಕಕ್ಷೇಯ ಸಂಕರ sp2 ಮಾದರಿಯದು. ಎಂದರೆ ಒಂದು s ಕಕ್ಷೇಯ ಮತ್ತು ಎರಡು p ಕಕ್ಷೇಯಗಳ ಮಿಶ್ರಣದಿಂದ ಆದುದು. ಹೊಸ ಏಕರೀತಿಯ ಮೂರು ಸಂಕರ ಕಕ್ಷೇಯಗಳು ಒಂದೇ ಸಮತಲದಲ್ಲಿದ್ದು ಅವುಗಳ ಅಕ್ಷಾಂತರ ಕೋನಗಳು ೧೨೦೦ ಇರುತ್ತವೆ. ಈ ಸಂಕರ ಕಕ್ಷೇಯಗಳಲ್ಲಿ ಪ್ರತಿಯೊಂದರಲ್ಲೂ ಒಂದೊಂದು ವಿದ್ಯುತ್ಕಣವಿದ್ದು ನಾಲ್ಕನೆಯ ವಿದ್ಯುತ್ಕಣ ಸಂಕರದಲ್ಲಿ ಭಾಗವಹಿಸದ sp2 ಸಂಕರ ಕಕ್ಷೇಯಗಳನ್ನುಳ್ಳ ಸಮತಲಕ್ಕೆ ಲಂಬಕೋನದಲ್ಲಿರುವ p ಕಕ್ಷೇಯದಲ್ಲಿರುತ್ತದೆ.

ತ್ರಿಬಂಧವುಳ್ಳ ಇಂಗಾಲದ ಪರಮಾಣುವಿನಲ್ಲಿ ಆಗುವ ಕಕ್ಷೇಯ ಸಂಕರ ಎರಡೇ ಕಕ್ಷೇಯಗಳಿಂದ ಆದದ್ದಾಗಿ sp ಸಂಕರ ಎಂದೆನ್ನಿಸಿಕೊಳ್ಳುತ್ತದೆ. ಎರಡು ಸಮಾನ sp ಸಂಕರ ಕಕ್ಷೇಯಗಳಲ್ಲಿ ಎರಡು ವಿದ್ಯುತ್ಕಣಗಳೂ ಸಂಕರದಲ್ಲಿ ಭಾಗವಹಿಸದ ಎರಡು p ಕಕ್ಷೇಯಗಳಲ್ಲಿ ಒಂದೊಂದರಲ್ಲಿ ಒಂದೊಂದರಂತೆ ಉಳಿದ ಇನ್ನೆರಡು ವಿದ್ಯುತ್ಕಣಗಳೂ ಇರುತ್ತವೆ. sp ಸಂಕರ ಕಕ್ಷೇಯಗಳು ಒಂದೇ ನೇರದಲ್ಲಿದ್ದು ಬೀಜದ ಇಬ್ಬದಿಗಳಲ್ಲಿಯೂ ಇರುತ್ತವೆ. ಅಸಂಕರ p ಕಕ್ಷೇಯಗಳೆರಡೂ ಪರಸ್ಪರ ಲಂಬಕೋನಗಳಲ್ಲಿರುವುದು ಮಾತ್ರವಲ್ಲದೆ ಎರಡೂ ಸಂಕರ ಕಕ್ಷೇಯಗಳ ಅಕ್ಷಕ್ಕೆ ಲಂಬಕೋನಗಳಲ್ಲಿರುತ್ತವೆ.
sp3, sp2 ಮತ್ತು sp, ಸಂಕರ ಕಕ್ಷೇಯಗಳು ಬಂಧಗಳಲ್ಲಿ ಹೇಗೆ ಭಾಗವಹಿಸುತ್ತವೆಂಬುದನ್ನು ಮೀಥೇನ್, ಎಥಿಲೀನ್ ಮತ್ತು ಅಸಿಟಲೀನ್ ಸಂಯುಕ್ತಗಳನ್ನು ನಿದರ್ಶನಗಳಾಗಿ ತೆಗೆದುಕೊಂಡು ಪರಿಶೀಲಿಸಬಹುದು.
CH4 ಎಂಬ ಸೂತ್ರವಿರುವ ಮೀಥೇನಿನಲ್ಲಿ ಇಂಗಾಲ ನಾಲ್ಕು ಏಕಬಂಧಗಳಿಂದ ನಾಲ್ಕು ಹೈಡ್ರೊಜನ್ನುಗಳಿಗೆ ಬಂಧವಾಗಿರುತ್ತದೆ. ಇದರಲ್ಲಿ ಇಂಗಾಲದ ಸಂಕರಕಕ್ಷೇಯರೂಪ sp3. ಹೈಡ್ರೊಜನ್ನಿನಲ್ಲಿ 1s ಕಕ್ಷೇಯವೊಂದೇ ಇದ್ದು ಅದರಲ್ಲಿ ಒಂದು ವಿದ್ಯುತ್ಕಣವಿದೆ. ಹೈಡ್ರೊಜನ್ ಪರಮಾಣುವೊಂದು ಇಂಗಾಲದ ಸಂಕರ ಕಕ್ಷೇಯದ ಅಕ್ಷದಲ್ಲಿಯೇ ಇಂಗಾಲದ ಪರಮಾಣುವನ್ನು ಸಮೀಪಿಸಿದಾಗ ಎರಡು ಪರಮಾಣು ಕಕ್ಷೇಯಗಳು ಒಂದಾಗಿ ಅಣುಕಕ್ಷೇಯ ಮತ್ತು C-H ಬಂಧವೊಂದರ ಸೃಷ್ಟಿಯಾಗುತ್ತದೆ. ನಾಲ್ಕು C-H ಬಂಧಗಳೂ ಇದೇ ರೀತಿ ನಿರ್ಮಾಣವಾಗಿ CH4 ಅಣುವಿನ ಉತ್ಪತ್ತಿಯಾಗುತ್ತದೆ. ಹೀಗೆ ಪರಮಾಣುಗಳ ಕಕ್ಷೇಯ ಒಂದೇ ಅಕ್ಷದಲ್ಲಿ ಪರಸ್ಪರ ಸಮೀಪಿಸಿ ನಿರ್ಮಾಣವಾಗುವ ಬಂಧ σ ಬಂಧವೆನ್ನಿಸಿಕೊಳ್ಳುತ್ತದೆ. ಮೀಥೇನಿನಲ್ಲಿರುವ ನಾಲ್ಕು ಬಂಧಗಳೂ σ ಬಂಧಗಳು.
ಎಥಿಲೀನಿನಲ್ಲಿ (H2C=CH2) ಪ್ರತಿ ಇಂಗಾಲ ಪರಮಾಣುವೂ ಮೂರು ಇತರ ಪರಮಾಣುಗಳಿಗೆ ಬಂಧಗೊಂಡಿದೆ. ಇದರಲ್ಲಿ ಇಂಗಾಲಗಳ ಸಂಕರ ಕಕ್ಷೇಯ ರೂಪ sp2. ಪ್ರತಿ ಇಂಗಾಲವೂ ಮತ್ತೊಂದು ಇಂಗಾಲ ಮತ್ತು ಎರಡು ಹೈಡ್ರೊಜನ್ನುಗಳೊಡನೆ σ ಬಂಧದ ಮೂಲಕ ಬಂಧಗೊಂಡಿರುತ್ತದೆ (ಚಿತ್ರದಲ್ಲಿ σ ಬಂಧಗಳನ್ನು ಗೆರೆಗಳ ಮೂಲಕ ತೋರಿಸಿದೆ). C-C ಮತ್ತು ನಾಲ್ಕು C-H ಬಂಧಗಳು ಒಂದೇ ಸಮತಲದಲ್ಲಿವೆ. ಎರಡು ಇಂಗಾಲಗಳ ಉಳಿದ p ಕಕ್ಷೇಯಗಳು ಈ ಸಮತಲಕ್ಕೆ ಲಂಬಕೋನದಲ್ಲಿವೆ. ಇವೆರಡು ಕಕ್ಷೇಯಗಳ ಅಕ್ಷಗಳು ಬೇರೆ ಬೇರೆಯಾಗಿದ್ದರೂ ಎರಡು ಇಂಗಾಲಗಳ ನಡುವಿನ σ ಬಂಧ ಅವನ್ನು ಸಮೀಪಕ್ಕೆ ತರುವುದರಿಂದ p ಕಕ್ಷೇಯಗಳು ಒಂದರ ಮೇಲೊಂದು ವ್ಯಾಪಿಸಿ ಅಣು ಕಕ್ಷೇಯವೊಂದು ಸೃಷ್ಟಿಯಾಗಿ ಬಂಧ ಏರ್ಪಡುತ್ತದೆ. ಈ ಬಗೆಯ P-P ಕಕ್ಷೇಯಗಳು ಸೇರಿ ಆಗುವ ಬಂಧದ ಹೆಸರು π - ಬಂಧ. π - ಬಂಧದ ಅಣು ಕಕ್ಷೇಯ ಎರಡು ಭಾಗಗಳಾಗಿದ್ದು σ ಬಂಧಗಳನ್ನುಳ್ಳ ಸಮತಲದ ಮೇಲೆ ಮತ್ತು ಕೆಳಗೆ ಒಂದೊಂದು ಭಾಗವಿದೆ.
sp ಸಂಕರ ಕಕ್ಷೇಯವಿರುವ ಅಸಿಟಲೀನಿನಲ್ಲಿ ಒಂದು C-C ಬಂಧ ಮತ್ತು ಎರಡು C-H ಬಂಧಗಳು σ ಬಂಧಗಳು.

ಸಂಕರದಲ್ಲಿ ಭಾಗವಹಿಸದೆ ಉಳಿದಿರುವ ನಾಲ್ಕು (ಪ್ರತಿ ಇಂಗಾಲದ ಎರಡೆರಡು) ಕಕ್ಷೇಯಗಳು ಸೇರಿ ಎಥಿಲೀನಿನಲ್ಲಿ ಆದಂತೆ ಎರಡು π ಬಂಧಗಳು ನಿರ್ಮಾಣವಾಗುತ್ತವೆ.
ಚಿತ್ರದಲ್ಲಿ ಎರಡು π ಬಂಧಗಳನ್ನೂ ಅಣು ಕಕ್ಷೇಯಗಳ ಮೂಲಕ ತೋರಿಸುವುದು ಕಷ್ಟವಾದ್ದರಿಂದ ಕಕ್ಷೇಯಗಳ ಅಕ್ಷಗಳನ್ನು ಮಾತ್ರ ತೋರಿಸಿ ಯಾವ ಯಾವ ಕಕ್ಷೇಯಗಳು ಪರಸ್ಪರ ವ್ಯಾಪಿಸಿ ಬಂಧಗಳನ್ನು ನಿರ್ಮಾಣಮಾಡುತ್ತವೆಂಬುದನ್ನು ತೋರಿಸಿದೆ.
ಇಂಗಾಲಸಂಯುಕ್ತಗಳ ಆಕಾರದ ಸ್ಪಷ್ಟೀಕರಣದ ಅಧ್ಯಯನವಾದ ಪರಮಾಣು ವಿನ್ಯಾಸರಸಾಯನಶಾಸ್ತ್ರ (ಸ್ಟೀರಿಯೋ ಕೆಮಿಸ್ಟ್ರಿ) ಇಂಗಾಲ ರಸಾಯನಶಾಸ್ತ್ರದ ಒಂದು ಮುಖ್ಯಭಾಗ. ಸಂಯುಕ್ತಗಳು ಜಟಿಲವಾದಂತೆ ಅವುಗಳ ಆಕಾರ ಸ್ಪಷ್ಟೀಕರಣದ ಸಮಸ್ಯೆಯೂ ಜಟಿಲವಾಗುತ್ತ ಹೋಗುತ್ತದೆ. ಆಕಾರಗಳು ಸಂಯುಕ್ತಗಳ ಲಕ್ಷಣಗಳ ಮೇಲೆ ಪ್ರಭಾವ ಬೀರುವುದರಿಂದ ಅವುಗಳ ಅಧ್ಯಯನ ಅನೇಕ ಬಾರಿ ಅತ್ಯಾವಶ್ಯಕ.
ವೈಶಿಷ್ಟ್ಯಗಳ ವಿವರಣೆ
[ಬದಲಾಯಿಸಿ]ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ಬಹುಮಟ್ಟಿಗೆ ಮಿಶ್ರಣಗಳಾಗಿರುವುದರಿಂದ, ಅವುಗಳ ಶುದ್ಧತೆಯನ್ನು ಅಳೆಯಲು ಅನೇಕ ತಂತ್ರಗಳನ್ನು ಮಾಡಲಾಗಿದೆ, ಪ್ರಮುಖವಾಗಿ HPLC ಹಾಗೂ ಅನಿಲ ವರ್ಣರೇಖನದಂತಹ ವರ್ಣರೇಖನ ತಂತ್ರಗಳನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ. ಸಾಂಪ್ರದಾಯಿಕ ಪ್ರತ್ಯೇಕಿಸುವ ವಿಧಾನಗಳೆಂದರೆ ಸಾಂದ್ರೀಕರಣ, ಸ್ಫಟಿಕೀಕರಣ ಹಾಗೂ ದ್ರಾವಕ ನಿಗಮನ. ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು "ತೇವ ವಿಧಾನಗಳೆಂದು" ಕರೆಯಲ್ಪಡುವ ವಿವಿಧ ಸಾಂಪ್ರದಾಯಿಕ ರಾಸಾಯನಿಕ ಪರೀಕ್ಷೆಗಳಲ್ಲಿ ತಮ್ಮ ವೈಶಿಷ್ಟ್ಯಗಳನ್ನು ತೋರುತ್ತಿದ್ದರೆ, ಪ್ರಸ್ತುತ ಅಂತಹಾ ಪರೀಕ್ಷೆಗಳನ್ನು ರೋಹಿತ ದರ್ಶನ ಅಥವಾ ಇನ್ನಿತರ ಗಣಕೀಕೃತ ವಿಶ್ಲೇಷಣಾ ವಿಧಾನಗಳ ಮೂಲಕ ನಡೆಸಲಾಗುತ್ತಿದೆ.[೭] ಬಳಕೆಯ ಅಂದಾಜಿನ ಕ್ರಮದ ಪ್ರಕಾರ ಪಟ್ಟಿ ಮಾಡಬಹುದಾದ ಪ್ರಮುಖ ವಿಶ್ಲೇಷಣಾ ವಿಧಾನಗಳೆಂದರೆ:
- ಅಣುಕಾಂತೀಯ ಅನುರಣನ (NMR) ರೋಹಿತದರ್ಶನವು ಅನ್ಯೋನ್ಯಾವಲಂಬನೆಯ ರೋಹಿತದರ್ಶನ ಬಳಸಿಕೊಂಡು ಸ್ಟೀರಿಯೋರಸಾಯನಶಾಸ್ತ್ರ ಅಣು ಸಂಯೋಜಕತೆಯ ಸಂಪೂರ್ಣ ಹಂಚಿಕೆಯನ್ನು ಮಾಡಲು ಅವಕಾಶ ನೀಡುವ ಬಹುಸಾಮಾನ್ಯವಾದ ತಂತ್ರವಾಗಿದೆ. ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಮೂಲ ಅಣುಗಳಾದ - ಜಲಜನಕ ಹಾಗೂ ಇಂಗಾಲಗಳು- ಅನುಕ್ರಮವಾಗಿ 1H ಹಾಗೂ 13C NMR-ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕ ಸಮಸ್ಥಾನಿಗಳಲ್ಲಿ ನೈಸರ್ಗಿಕವಾಗಿಯೇ ಲಭ್ಯವಿರುತ್ತವೆ.
- ಧಾತುರೂಪಿ ವಿಶ್ಲೇಷಣೆ: ಅಣುವಿನ ಧಾತುರೂಪಿ ಸಂಯೋಜನೆಯನ್ನು ತಿಳಿದುಕೊಳ್ಳುವ ವಿನಾಶಕ ವಿಧಾನವಾಗಿದೆ. ಕೆಳಗೆ ರಾಶಿ ರೋಹಿತ ಮಾಪನವನ್ನೂ ನೋಡಿ..
- ರಾಶಿ ರೋಹಿತಮಾಪನವು ಸಂಯುಕ್ತವೊಂದರ ಅಣುತೂಕವನ್ನು ಸೂಚಿಸುತ್ತದೆ, ಹಾಗೂ ವಿಘಟನ ಮಾದರಿಗಳಿಂದ ಅದರ ರಚನೆಯನ್ನು ಸೂಚಿಸುತ್ತದೆ. ಉಚ್ಚ ಅಭಿನಿವೇಶ ರಾಶಿ ರೋಹಿತಮಾಪನವು ಸಾಮಾನ್ಯವಾಗಿ ಸಂಯುಕ್ತವೊಂದರ ನಿಖರ ಸೂತ್ರವನ್ನು ಗುರುತಿಸಬಲ್ಲದಾದುದರಿಂದ ಧಾತುರೂಪಿ ವಿಶ್ಲೇಷಣೆಯ ಬದಲಿಗೆ ಅದನ್ನು ಬಳಸಲಾಗುತ್ತದೆ. ಹಿಂದೆ, ರಾಶಿ ರೋಹಿತಮಾಪನವು ಬಾಷ್ಪಶೀಲತೆ ಇರುವ ತಟಸ್ಥ ಅಣುಗಳ ಮಟ್ಟಿಗೆ ಮಾತ್ರ ಸೀಮಿತವಾಗಿತ್ತು, ಆದರೆ ಆಧುನಿಕ ಅಯಾನೀಕರಣ ವಿಧಾನಗಳಿಂದ ಬಹುತೇಕ ಯಾವುದೇ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತದ "ರಾಶಿ ವಿವರ" ಪಡೆಯಲು ಸಾಧ್ಯವಿದೆ.
- ಸ್ಫಟಿಕೀಕರಣವು ಅಣು ಜ್ಯಾಮಿತಿಯನ್ನು ಪತ್ತೆ ಹಚ್ಚಲು ಬಳಸುವ ಸ್ಪಷ್ಟ ವಿಧಾನವಾಗಿದೆ, ಆದರೆ ವಸ್ತುವಿನ ಬಿಡಿ ಸ್ಫಟಿಕಗಳು ಲಭ್ಯವಿರಬೇಕು ಹಾಗೂ ಸ್ಫಟಿಕವು ವಸ್ತುವನ್ನು ಪ್ರತಿನಿಧಿಸುವಂತಿರಬೇಕು ಎಂಬುದೊಂದು ಮಿತಿಯಿದೆ. ಸೂಕ್ತ ಸ್ಫಟಿಕವು ಲಭ್ಯವಿದ್ದರೆ ಕೆಲ ಗಂಟೆಗಳಲ್ಲೇ ರಚನೆಯನ್ನು ನಿರ್ಣಯಿಸಬಲ್ಲ ಉಚ್ಚ ಸ್ವಯಂಚಲಿ ತಂತ್ರಾಂಶಗಳು ಲಭ್ಯವಿವೆ.
ಸಾಂಪ್ರದಾಯಿಕ ರೋಹಿತದರ್ಶಕ ವಿಧಾನಗಳಾದ ಅವಗೆಂಪು ರೋಹಿತದರ್ಶನ, ದ್ಯುತಿ ಭ್ರಮಣ, UV/VIS ರೋಹಿತದರ್ಶನಗಳು ಸಂಯುಕ್ತಗಳ ನಿರ್ದಿಷ್ಟ ವರ್ಗಕ್ಕೆ ಮಾತ್ರ ಉಪಯುಕ್ತವಾದ ರಚನೆಯ ಬಗ್ಗೆ ಅನಿರ್ದಿಷ್ಟ ಮಾಹಿತಿಯನ್ನು ಮಾತ್ರ ನೀಡುತ್ತವೆ. ವಿಶ್ಲೇಷಕ ರಸಾಯನಶಾಸ್ತ್ರದ ಲೇಖನದಲ್ಲಿ ಹೆಚ್ಚಿನ ವಿಧಾನಗಳ ಬಗ್ಗೆ ವಿವರಿಸಲಾಗಿದೆ.
ಗುಣಲಕ್ಷಣಗಳು
[ಬದಲಾಯಿಸಿ]ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ಆಸಕ್ತಿದಾಯಕ ಭೌತಿಕ ಲಕ್ಷಣಗಳು ಪರಿಮಾಣಾತ್ಮಕ ಹಾಗೂ ಗುಣಾತ್ಮಕ ವೈಶಿಷ್ಟ್ಯಗಳನ್ನು ಹೊಂದಿವೆ. ಪರಿಮಾಣಾತ್ಮಕ ಮಾಹಿತಿಗಳಲ್ಲಿ ಕರಗುವ ಬಿಂದು,ಕುದಿಯುವ ಬಿಂದು ಹಾಗೂ ವಕ್ರೀಭವನ ಬಿಂದುಗಳು ಸೇರಿವೆ. ಗುಣಾತ್ಮಕ ಲಕ್ಷಣಗಳಲ್ಲಿ ವಾಸನೆ,ವಿಲಯನತ್ವ ಹಾಗೂ ವರ್ಣಗಳು ಸೇರಿವೆ.
ಕರಗುವ ಹಾಗೂ ಕುದಿಯುವ ಲಕ್ಷಣಗಳು
[ಬದಲಾಯಿಸಿ]ಅನೇಕ ಅಜೈವಿಕ ವಸ್ತುಗಳ ಹಾಗಲ್ಲದೇ, ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಕರಗುತ್ತವೆ ಹಾಗೂ ಕೆಲವು ಕುದಿಯುತ್ತವೆ. ಹಿಂದೆ, ಕರಗುವ ಬಿಂದು (m.p.) ಹಾಗೂ ಕುದಿಯುವ ಬಿಂದುಗಳು (b.p.) ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ಶುದ್ಧತೆ ಹಾಗೂ ಸ್ವರೂಪವನ್ನು ಅರಿಯುವ ನಿರ್ಣಾಯಕ ಮಾಹಿತಿಗಳನ್ನು ನೀಡುತ್ತಿದ್ದವು. ಕರಗುವ ಹಾಗೂ ಕುದಿಯುವ ಬಿಂದುಗಳು ಅಣುಗಳ ಧೃವೀಯತೆ ಹಾಗೂ ಅಣುತೂಕಗಳ ಮೇಲೆ ಆಧಾರಿತವಾಗಿವೆ. ಕೆಲ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು, ವಿಶೇಷವಾಗಿ ಅನುರೂಪಿಗಳು, ಉದ್ಧೃತವಾಗಿರುತ್ತವೆ, ಅಂದರೆ ಅವು ಕರಗದೇ ಆವಿಯಾಗುತ್ತವೆ. ಉದ್ಧೃತವಾಗಬಲ್ಲ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತದ ಜನಪ್ರಿಯ ಉದಾಹರಣೆಯೆಂದರೆ ನುಸಿಗುಳಿಗೆಯಲ್ಲಿನ ವಾಸನಾದ್ರವ್ಯವಾದ ಪ್ಯಾರಾ-ಡೈಕ್ಲೋರೋಬೆಂಜೀನ್. ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು 300 °Cಗಿಂತ ಹೆಚ್ಚಿನ ತಾಪಮಾನದಲ್ಲಿ ಹೆಚ್ಚಿನ ಮಟ್ಟದ ಸ್ಥಿರತೆ ಕಾಪಾಡಿಕೊಳ್ಳಲಾರವಾದರೂ, ಕೆಲವು ಅಪವಾದಗಳೂ ಇವೆ.
ಬಣ್ಣ
[ಬದಲಾಯಿಸಿ]ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ಸಾಧಾರಣವಾಗಿ ವರ್ಣರಹಿತ ಇಲ್ಲವೇ ಬೆಳ್ಳಗಿರುತ್ತವೆ. ಆದರೆ ಅನೇಕ ನಿಕಟ ಬಂಧಕಗಳನ್ನು ಹೊಂದಿರುವ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ವಿಚಾರದಲ್ಲಿ ಸನ್ನಿವೇಶ ಬೇರೆಯೇ ಇದೆ. ದ್ವಿಬಂಧಕಗಳು "ಸಂಯೋಗ"ಗೊಂಡಿರುವ ಸಂಯುಕ್ತಗಳು ಕಡುವರ್ಣದವಾಗಿರಬಹುದು. ಜೈವಿಕ ವರ್ಣದ್ರವ್ಯಗಳಾದ ಕೆರೊಟೀನ್ ಹಾಗೂ ಹೀಮ್ಗಳು "ಸಂಯೋಜನೆ" ಹಾಗೂ ವರ್ಣಗಳ ನಡುವಿನ ಸಂಬಂಧವನ್ನು ವಿಷದೀಕರಿಸುತ್ತವೆ. ಅಶುದ್ಧ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ಹಾಗೂ ಅನೇಕ ಜೈವಿಕ ವಸ್ತುಗಳು ಗಾಢವರ್ಣದ ಕಲ್ಮಶಗಳ ಉಪಸ್ಥಿತಿಯನ್ನು ತೋರುವಂತೆ ಹಳದಿ ಇಲ್ಲವೇ ಕಂದು ವರ್ಣದವಾಗಿರುತ್ತವೆ.
ವಿಲಯನತ್ವ
[ಬದಲಾಯಿಸಿ]ತಟಸ್ಥ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ನೀರಿನಿಂದ ಒದ್ದೆಯಾಗಲಾರವು, ಅಂದರೆ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ದ್ರಾವಕಗಳಿಗಿಂತ ನೀರಿನಲ್ಲಿ ಕಡಿಮೆ ಕರಗುತ್ತವೆ. ಇದಕ್ಕೆ ಅಪವಾದವೆಂದರೆ ಅಯಾನೀಕರಿಸಬಲ್ಲ ಗುಂಪುಗಳನ್ನು ಹೊಂದಿದ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ಹಾಗೂ ಜಲಜನಕ ಬಂಧಕವಾಗುವ ಅಲ್ಪ ಅಣುತೂಕದ ಆಲ್ಕೋಹಾಲ್ಗಳು, ಅಮೈನ್ಗಳು, ಹಾಗೂ ಕಾರ್ಬಾಕ್ಸಿಲ್ ಆಮ್ಲಗಳು. ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ದ್ರಾವಕಗಳಲ್ಲಿ ಸಾಮಾನ್ಯವಾಗಿ ಕರಗಬಲ್ಲವು. ಈಥರ್ ಅಥವಾ ಈಥೈಲ್ ಆಲ್ಕೋಹಾಲ್ಗಳಂತಹ ಶುದ್ಧ ವಸ್ತುಗಳು ಅಥವಾ ಮಿಶ್ರಣಗಳು, ಅನೇಕ ಪೆಟ್ರೋಲಿಯಂ ಈಥರ್ಗಳು ಹಾಗೂ ಶ್ವೇತ ಮದ್ಯಸಾರದಂತಹ ಮೇಣದ ದ್ರಾವಕ, ಅಥವಾ ಶುದ್ಧ ಅಥವಾ ಮಿಶ್ರಿತ ಪೆಟ್ರೋಲಿಯಂನಿಂದ ಪಡೆದ ಅನೇಕ ಶುದ್ಧ ಅಥವಾ ಮಿಶ್ರಿತ ಅಥವಾ ಸುಗಂಧಿತ ದ್ರಾವಕಗಳು ಅಥವಾ ಕೀಲೆಣ್ಣೆ ಅಂಶಗಳನ್ನು ಭೌತಿಕ ಪ್ರತ್ಯೇಕತೆ ಅಥವಾ ರಾಸಾಯನಿಕ ಪರಿವರ್ತನೆಗಳ ಮೂಲಕ ಪಡೆಯುವ ದ್ರಾವಕಗಳು. ಅನೇಕ ದ್ರಾವಕಗಳು ದ್ರಾವಕದ ರೀತಿಯ ಮೇಲೆ ಆಧಾರಿತವಾಗಿ ಹಾಗೂ ಲಭ್ಯವಿದ್ದರೆ ಕಾರ್ಯಸಂಬಂಧಿ ವಿವಿಧ ಮಟ್ಟದ ವಿಲಯನತ್ವವನ್ನು ಹೊಂದಿರುತ್ತವೆ.
ಘನಸ್ಥಿತಿ ಲಕ್ಷಣಗಳು
[ಬದಲಾಯಿಸಿ]ಅನೇಕ ವಿಶೇಷ ಲಕ್ಷಣಗಳು ಅನ್ವಯಗಳ ಮೇಲೆ ಆಧಾರಿತವಾಗಿ ಆಸಕ್ತಿದಾಯಕವಾಗಿರುತ್ತವೆ, e.g. ಪೀಜೋವಿದ್ಯುತ್, ವಿದ್ಯುತ್ ವಾಹಕತ್ವ (ನೋಡಿ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಲೋಹಗಳು), ಹಾಗೂ ವಿದ್ಯುತ್-ದ್ಯುತಿಯಂತಹಾ (e.g. ಅರೇಖೀಯ ದೃಷ್ಟಿಶಾಸ್ತ್ರ) ಉಷ್ಣ-ಯಾಂತ್ರಿಕ ಹಾಗೂ ವಿದ್ಯುತ್-ಯಾಂತ್ರಿಕ ಲಕ್ಷಣಗಳು. ಚಾರಿತ್ರಿಕ ಕಾರಣಗಳಿಗೋಸ್ಕರ, ಈ ಲಕ್ಷಣಗಳು ಪಾಲಿಮರ್ ವಿಜ್ಞಾನ ಹಾಗೂ ವಸ್ತುವಿಜ್ಞಾನ ಕ್ಷೇತ್ರಗಳ ಪ್ರಮುಖ ವಿಷಯಗಳಾಗಿವೆ.
ನಾಮಕರಣ
[ಬದಲಾಯಿಸಿ]
ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ಹೆಸರುಗಳು ಒಂದೋ ಕ್ರಮಾತ್ಮಕವಾಗಿ, ತರ್ಕನಿಯಮಾನುಸಾರವಾಗಿದ್ದು ಇಲ್ಲವೇ ಕ್ರಮವಿಲ್ಲದೇ ಅನೇಕ ಸಂಪ್ರದಾಯಗಳನ್ನು ಪಾಲಿಸಿ ನೀಡಲಾಗುತ್ತದೆ. ಕ್ರಮಾತ್ಮಕ ಪರಿಭಾಷೆಯು IUPACಯ ಶಿಫಾರಸುಗಳಿಗೆ ಬದ್ಧವಾಗಿರುತ್ತದೆ. ಕ್ರಮಾತ್ಮಕ ಪರಿಭಾಷೆಯು ಆಸಕ್ತಿಯ ಅಣುವಿನ ಮೂಲರಚನೆಯ ಹೆಸರಿನಿಂದ ಆರಂಭವಾಗುತ್ತದೆ. ಮೂಲರಚನೆಯ ಹೆಸರನ್ನು ನಂತರ ಪೂರ್ವಪ್ರತ್ಯಯ, ಅಂತ್ಯಪ್ರತ್ಯಯ ಹಾಗೂ ಸಂಖ್ಯೆಗಳನ್ನು ಸೇರಿಸಿ ರಚನೆಯನ್ನು ಸೂಚಿಸುವಂತೆ ಬದಲಿಸಲಾಗುತ್ತದೆ. ದಶಲಕ್ಷಗಳಷ್ಟು ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ತಿಳಿದಿರುವಾಗ, ಕ್ರಮಾತ್ಮಕ ಹೆಸರುಗಳ ಕಟ್ಟುನಿಟ್ಟು ಪಾಲನೆ ತೊಡಕಾಗಬಲ್ಲದು. ಆದ್ದರಿಂದ, IUPAC ಶಿಫಾರಸುಗಳನ್ನು ಸರಳ ಸಂಯುಕ್ತಗಳಿಗೆ ಮಾತ್ರ ಬಳಸಿ, ಸಂಕೀರ್ಣ ಪರಮಾಣುಗಳಿಗೆ ಬಳಸಲಾಗುವುದಿಲ್ಲ. ಕ್ರಮಾತ್ಮಕ ನಾಮಕರಣವನ್ನು ಬಳಸಲು ಸಂರಚನೆ ಹಾಗೂ ಮೂಲ ಸಂರಚನೆಗಳ ಬಗ್ಗೆ ತಿಳಿದಿರಬೇಕಾದ್ದು ಅತ್ಯವಶ್ಯ. ಮೂಲ ಸಂರಚನೆಗಳೆಂದರೆ ಬದಲಿಕೆಯಿಲ್ಲದ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು, ವಿಭಿನ್ನಆವರ್ತನೆ, ಹಾಗೂ ಏಕಚಟುವಟಿಕಾತ್ಮಕ ರೂಪಾಂತರಗಳೂ ಸೇರಿವೆ.
ಕ್ರಮವಲ್ಲದ ಪರಿಭಾಷೆಯು ಕನಿಷ್ಟ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ರಸಾಯನಶಾಸ್ತ್ರ ತಜ್ಞರಿಗಾದರೂ ಸರಳ ಹಾಗೂ ಸ್ಪಷ್ಟವಾಗಿರುತ್ತವೆ. ಕ್ರಮವಲ್ಲದ ಹೆಸರುಗಳು ಸಂಯುಕ್ತದ ಸಂರಚನೆಯನ್ನು ಸೂಚಿಸುವುದಿಲ್ಲ. ಕ್ರಮವಲ್ಲದ ಹೆಸರುಗಳು ಬಹಳಷ್ಟು ಮಟ್ಟಿಗೆ ನೈಸರ್ಗಿಕ ಉತ್ಪನ್ನಗಳನ್ನು ಒಳಗೊಂಡಂತೆ ಸಂಕೀರ್ಣ ಪರಮಾಣುಗಳಿಗೆ ಸಮಾನವಾಗಿರುತ್ತವೆ. ಆದ್ದರಿಂದ, ಕ್ರಮವಿಲ್ಲದ ಹೆಸರನ್ನು ಹೊಂದಿರುವ ಲೈಸರ್ಜಿಕ್ ಆಮ್ಲ ಡೈಈಥೈಲಮೈಡ್ ಅನ್ನು ಕ್ರಮಾತ್ಮಕವಾಗಿ (6aR,9R)-N,N-ಡೈಈಥೈಲ್-7-ಮೀಥೈಲ್-4,6,6a,7,8,9-ಹೆಕ್ಸಾಹೈಡ್ರೋಇಂಡೋಲೋ-[4,3-fg] ಕ್ವಿನೋಲಿನ್-9-ಕಾರ್ಬಾಕ್ಸಮೈಡ್ ಎಂದು ಹೆಸರಿಸಲಾಗಿದೆ. ಹೆಚ್ಚಿದ ಗಣಕೀಕರಣದಿಂದಾಗಿ ಗಣಕ/ಯಂತ್ರಗಳು ಬಳಸಲುದ್ದೇಶಿಸಿದ ಇತರೆ ನಾಮಕರಣ ವಿಧಾನಗಳು ವಿಕಾಸಗೊಂಡಿವೆ. ಎರಡು ಜನಪ್ರಿಯ ಮಾದರಿಗಳೆಂದರೆ SMILES ಹಾಗೂ InChI.
ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಸಂಖ್ಯೆ ಅಧಿಕವಾಗಿರುವುದರಿಂದಲೂ ಸಮಘಟಕಗಳ ಇರುವಿಕೆಯಿಂದಲೂ ಇಂಗಾಲಸಂಯುಕ್ತಗಳನ್ನು ಹೆಸರಿಸಲು ಕ್ರಮಬದ್ಧನಿಯಮಗಳು ಅಗತ್ಯವಾಗುತ್ತವೆ. ಕಡಿಮೆ ಸಂಯುಕ್ತಗಳ ಪರಿಚಯವಿದ್ದಾಗ ಬಳಕೆಯಲ್ಲಿದ್ದು ಸಮರ್ಪಕವಾಗಿದ್ದ ಹಳೆಯ ಪದ್ಧತಿಯೊಂದು ಈಗಲೂ ತಕ್ಕಮಟ್ಟಿಗೆ ಉಪಯೋಗದಲ್ಲಿದೆ. ಈ ಪದ್ಧತಿಯ ಪ್ರಕಾರ ಸಂಯುಕ್ತದಲ್ಲಿನ ಒಟ್ಟು ಇಂಗಾಲದ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ ಮುಖ್ಯ. ಉದಾಹರಣೆಗೆ, ನಾಲ್ಕು ಇಂಗಾಲವನ್ನುಳ್ಳ ಎರಡು ಪರ್ಯಾಪ್ತ ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳೂ ಬ್ಯೂಟೇನ್ನುಗಳೇ. ಅಂತೆಯೇ ಐದು ಇಂಗಾಲಗಳಿರುವ ಎಲ್ಲ ಪರ್ಯಾಪ್ತ ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳೂ ಪೆಂಟೇನುಗಳು. ಈ ನಿಯಮದ ಪ್ರಕಾರ ಕರೆಯಲ್ಪಡುವ ಮೊದಲ ಹತ್ತು ಪರ್ಯಾಪ್ತ ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳ ಹೆಸರುಗಳನ್ನು ಮುಂದೆ ತೋರಿಸಲಾಗಿದೆ.
| ಇಂಗಾಲ
ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ |
ಅಣುಸೂತ್ರ | ಹೆಸರು |
|---|---|---|
| 1 | CH4 | ಮೀಥೇನ್ |
| 2 | C2H6 | ಈಥೇನ್ |
| 3 | C3H8 | ಪ್ರೊಪೇನ್ |
| 4 | C4H10 | ಬ್ಯೂಟೇನ್ |
| 5 | C5H12 | ಪೆಂಟೇನ್ |
| 6 | C6H14 | ಹೆಕ್ಸೇನ್ |
| 7 | C7H16 | ಹೆಪ್ಟೇನ್ |
| 8 | C8H18 | ಆಕ್ಟೇನ್ |
| 9 | C9H20 | ನೋನೇನ್ |
| 10 | C10H22 | ಡೆಕೇನ್ |
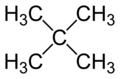
ಐದು ಇಂಗಾಲಗಳನ್ನುಳ್ಳ ಮೂರು ಸಮಘಟಕಗಳಿಗೆ ಕೆಳಗೆ ತೋರಿಸಿರುವ ಮೂರು ಹೆಸರುಗಳನ್ನು ಕೊಡಲಾಗಿತ್ತು.
-
ನಾರ್ಮಲ್ ಪೆಂಟೇನ್
-
ಐಸೊಪೆಂಟೇನ್
-
ನಿಯೊ ಪೆಂಟೇನ್
ಆದರೆ ಹೆಕ್ಸೇನ್ ಮತ್ತು ಅದಕ್ಕಿಂತ ಹಿರಿಯಗಾತ್ರದ ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳ ಸಮಘಟಕಗಳು ಅಧಿಕ ಸಂಖ್ಯೆಯಲ್ಲಿವೆ. (೫ ಹೆಕ್ಸೇನುಗಳು, ೯ ಹೆಪ್ಟೇನುಗಳು, ೭೫ ಡೆಕೇನುಗಳು ಇತ್ಯಾದಿ). ಹಳೆಯ ಪದ್ಧತಿಯ ಪ್ರಕಾರ ಹೆಚ್ಚು ಸಂಖ್ಯೆಯ ಸಮಘಟಕಗಳಿಗೆ ಹೆಸರುಗಳನ್ನು ಕೊಡುವುದು ಬಲು ಕಷ್ಟವಾಗುತ್ತದೆ. ಆದ್ದರಿಂದ ಅನೇಕಾನೇಕ ಸಮಘಟಕಗಳಿಗೂ ಸಮರ್ಪಕವಾಗಿ ಹೆಸರು ಕೊಡಲು ಅನುಕೂಲವಾಗುವಂಥ ಒಂದು ಕ್ರಮಬದ್ಧನಿಯಮ ಆವಶ್ಯಕ.
ಬಹುಕಾಲ ಈ ನಿಯಮಗಳ ಆವಶ್ಯಕತೆಯ ಬಗ್ಗೆ ವಿಜ್ಞಾನಿಗಳು ವಿಚಾರ ಮಾಡುತ್ತಿದ್ದರು. ೧೯೫೭ರಲ್ಲಿ ಇಂಟರ್ನ್ಯಾಷನಲ್ ಯೂನಿಯನ್ ಆಫ್ ಪ್ಯೂರ್ ಅಂಡ್ ಅಪ್ಲೈಡ್ ಕೆಮಿಸ್ಟ್ರಿ ಸಂಸ್ಥೆ ಈ ನಿಯಮಗಳ ಬಗೆಗೆ ಹಲವು ನಿರ್ಣಯಗಳನ್ನು ನೀಡಿತು. ಇವು ಈಗ ಜಗತ್ತಿನಾದ್ಯಂತ ಅಂಗೀಕೃತವಾಗಿವೆ. ಹಲವು ಮುಖ್ಯ ನಿರ್ಣಯ ನಿಯಮಗಳನ್ನು ಮುಂದೆ ಕೊಡಲಾಗಿದೆ.
ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳು-ಅಚಕ್ರೀಯ ಸಂಯುಕ್ತಗಳು (ನಾನ್ಸೈಕ್ಲಿಕ್ ಆರ್ ಅಸೈಕ್ಲಿಕ್ ಕಾಂಪೌಂಡ್ಸ್) ಅಚಕ್ರೀಯ ಪರ್ಯಾಪ್ತ ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳು (ಆಲ್ಕೇನುಗಳು): ಕವಲೊಡೆಯದ ನೇರ ಸರಣಿಯಲ್ಲಿರುವ ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳ ಹೆಸರುಗಳು ಹಳೆಯ ಪದ್ಧತಿಯಂತೆ ಇಂಗಾಲ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ಅನುಸರಿಸುತ್ತವೆ.
ಕವಲೊಡೆಯದ ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳಲ್ಲಿ ಅಂತಿಮ ಇಂಗಾಲದಿಂದ ಒಂದು ಹೈಡ್ರೊಜನ್ ನಷ್ಟವಾಗಿ ದೊರೆಯುವ ಒಂದು ವೇಲೆನ್ಸಿಯಿರುವ ಪುಂಜದ ಹೆಸರನ್ನು ಪಡೆಯಲು ಮಾತೃ ಸಂಯುಕ್ತದ ಹೆಸರಿನ ಆನ್ ಎಂಬ ಅಂತ್ಯ ಭಾಗವನ್ನು ಐಲ್ ಎಂಬ ಭಾಗದಿಂದ ಪಲ್ಲಟನೆ ಮಾಡಬೇಕು. ಈ ಬಗೆಯ ಪುಂಜಗಳು ನಾರ್ಮಲ್ ಆಲ್ಕೈಲ್ ಪುಂಜಗಳೆನ್ನಿಸಿಕೊಳ್ಳುತ್ತವೆ. ಉದಾಹರಣೆ:
CH3.CH2.CH2.CH2---ಬ್ಯೂಟೈಲ್ CH3(CH2)10-CH2—ಡೊಡೆಕೈಲ್
ಕವಲೊಡೆದ ಸಂಯುಕ್ತದ ಹೆಸರು ಅತಿ ಉದ್ದದ ನೇರಸರಣಿಯ ಮಾತೃ ಸಂಯುಕ್ತದ ಹೆಸರನ್ನು ಅವಲಂಬಿಸಿದೆ. ಕವಲುಗಳನ್ನು ಆದೇಶಿತ (ಸಬ್ಸ್ಟಿಟ್ಯೂಟೆಡ್) ಆಲ್ಕೈಲ್ ಪುಂಜಗಳೆಂದು ಪರಿಗಣಿಸಬೇಕು. ಈ ಆದೇಶಿತ ಆಲ್ಕೈಲ್ ಪುಂಜದ ಸ್ಥಾನವನ್ನು ನಿರ್ದೇಶಿಸಲು ಮಾತೃ ಸಂಯುಕ್ತ ಸರಣಿಯ ಇಂಗಾಲಗಳಿಗೆ ಕ್ರಮಾಂಕಗಳನ್ನು ಕೊಡಬೇಕು. ಕ್ರಮಾಂಕಗಳನ್ನು ಎರಡು ಬಗೆಯಾಗಿ (ಬಲದಿಂದ ಮತ್ತು ಎಡದಿಂದ) ಕೊಡಬಹುದಾದ್ದರಿಂದ ಆದೇಶಿತ ಪುಂಜವನ್ನು ಪಡೆದಿರುವ ಇಂಗಾಲದ ಕ್ರಮಾಂಕ ಕನಿಷ್ಠವಾಗಿರುವಂತೆ ಕೊಡಬೇಕು. ಉದಾಹರಣೆ:
5 4 3 2 1
CH3-CH2-CH2-CH-CH3
| 2-ಮೀಥೈಲ್ ಪೆಂಟೇನ್
CH3
ಅಥವಾ
1 2 3 4 5
CH3-CH2-CH2-CH-CH3
| 4-ಮೀಥೈಲ್ ಪೆಂಟೇನ್
CH3
ಇವುಗಳಲ್ಲಿ ೪-ಮೀಥೈಲ್ ಪೆಂಟೇನ್ ಎಂಬ ಹೆಸರು ತಪ್ಪು. ಅಲ್ಲದೆ ಎರಡು ಆದೇಶಿತ ಆಲ್ಕೈಲ್ ಪುಂಜಗಳಲ್ಲಿ ಹಿರಿಯ ಗಾತ್ರದ ಪುಂಜಕ್ಕೆ ಕನಿಷ್ಠ ಕ್ರಮಾಂಕ ಬರುವಂತೆ ಹೆಸರು ಕೊಡಬೇಕು. ಉದಾಹರಣೆ:
1(6) 2(5) 3(4) 4(3) 5(2) 6(1)
CH3 - CH2 - CH - CH - CH2 - CH3
| |
C2H5 CH3
೩-ಮೀಥೈಲ್-೪-ಈಥೈಲ್ ಹೆಕ್ಸೇನ್-ತಪ್ಪು
೩-ಈಥೈಲ್-೩-ಮೀಥೈಲ್ ಹೆಕ್ಸೇನ್-ಸರಿ
ಅಂತಿಮ ಇಂಗಾಲದಿಂದಲ್ಲದೆ ಮಧ್ಯಮ ಇಂಗಾಲವೊಂದರಿಂದ ಹೈಡ್ರೊಜನ್ ನಷ್ಟವಾಗಿ ಪುಂಜಗಳ ಸೃಷ್ಟಿಯಾದಾಗ ವೇಲೆನ್ಸಿಯಿರುವ ಇಂಗಾಲದಿಂದ ಆರಂಭಿಸಿ ಅತಿ ಉದ್ದನೆಯ ಸರಣಿಗೆ ಕ್ರಮಾಂಕಗಳನ್ನು ಕೊಡಬೇಕು ಮತ್ತು ಆದೇಶಿತ ಪುಂಜಗಳ ಸ್ಥಾನಗಳನ್ನು ನಿರ್ದೇಶಿಸಬೇಕು. ಉದಾಹರಣೆ:
4 3 2 1
CH3. CH2 . CH2 .CH 1 - ಮೀಥೈಲ್ ಬ್ಯೂಟೈಲ್
|
CH3
ಇವುಗಳಲ್ಲಿ ಮೊದಲನೆಯದರ ಕ್ರಮಾಂಕ ಎರಡನೆಯ ಪುಂಜದ ಕ್ರಮಾಂಕಕ್ಕಿಂತಲೂ ಮೊದಲು ಬರುತ್ತದೆ.
ಹಲವು ಸರಳ ಪುಂಜಗಳನ್ನು ತಿಳಿಸುವಾಗ ಇಂಗ್ಲಿಷ್ ಅಕ್ಷರಮಾಲೆಯ ಕ್ರಮವನ್ನು ಅನುಸರಿಸಬಹುದು. ಉದಾಹರಣೆ, ಬ್ಯೂಟೈಲ್, ಈಥೈಲ್, ಮೀಥೈಲ್, ಪ್ರೋಪೈಲ್.
ದ್ವಿಬಂಧ ಸಂಯುಕ್ತಗಳ ಅಂತ್ಯ ಈನ್ ಎಂದೂ ತ್ರಿಬಂಧ ಸಂಯುಕ್ತಗಳ ಅಂತ್ಯ ಐನ್ ಎಂದೂ ಇರಬೇಕು. ಮೂಲ ಆಲ್ಕೇನುಗಳ ಹೆಸರಿನಿಂದ ಆನ್ ಎಂಬ ಅಂತ್ಯವನ್ನು ತೆಗೆದ ಅನಂತರ ಉಳಿಯುವುದು. ದ್ವಿಬಂಧ ಅಥವಾ ತ್ರಿಬಂಧ ಸ್ಥಾನಗಳನ್ನು ಆ ಬಗೆಯ ಬಂಧಗಳನ್ನು ಪಡೆದಿರುವ ಇಂಗಾಲದ ಕ್ರಮಾಂಕದಿಂದ ತಿಳಿಸಬೇಕು. ಕ್ರಮಾಂಕಗಳನ್ನು ನಿರ್ದೇಶಿಸಲು ಆದೇಶಿತ ಪುಂಜಗಳ ಗಾತ್ರಗಳನ್ನು ಗಮನಿಸದೆ ಅಪರ್ಯಾಪ್ತ ಬಂಧವನ್ನೊಳಗೊಂಡಿರುವ ಅತಿ ದೀರ್ಘಸರಣಿಯನ್ನು ಆರಿಸಬೇಕು; ಮತ್ತು ಅಪರ್ಯಾಪ್ತ ಬಂಧದ ಸ್ಥಾನವನ್ನು ನಿರ್ದೇಶಿಸುವ ಕ್ರಮಾಂಕ ಕನಿಷ್ಠವಾಗಿರಬೇಕು. ಉದಾಹರಣೆ:
5 4 3 2
CH3 - CH2 - CH2 - C – CH2 – CH2 – CH3
‖ 2--ಪ್ರೊಪೈಲ್ --1---ಪೆಂಟೇನ್
1CH2
ಎರಡು ದ್ವಿಬಂಧಗಳುಳ್ಳ ಸಂಯುಕ್ತ – ಡಯೀನ್
ಮೂರು ದ್ವಿಬಂಧಗಳುಳ್ಳ ಸಂಯುಕ್ತ – ಟ್ರಯೀನ್
ಎರಡು ತ್ರಿಬಂಧಗಳುಳ್ಳ ಸಂಯುಕ್ತ - ಡೈಯೈನ್
ಮೂರು ತ್ರಿಬಂಧಗಳುಳ್ಳ ಸಂಯುಕ್ತ - ಟ್ರಯೈನ್
ಆಲ್ಕೀನ್ ಮತ್ತು ಆಲ್ಕೈನ್ ನಿಷ್ಪನ್ನ (ಡೆರವಟ್ಯೂ) ಪುಂಜಗಳ ಹೆಸರುಗಳ ಮೂಲ ಸಂಯುಕ್ತದ ಹೆಸರಿಗೆ ಐಲ್ ಸೇರಿಸಿದಾಗ ದೊರೆಯುತ್ತವೆ. ಪುಂಜಗಳಲ್ಲಿ ಕ್ರಮಾಂಕಗಳನ್ನು ವೇಲೆನ್ಸಿಯಿರುವ ಇಂಗಾಲದಿಂದ ಆರಂಭಿಸಬೇಕು. ಉದಾಹರಣೆ:
2 1
CH2= C---- 1-ಮೀಥೈಲ್ ಎಥಿನೈಲ್ (ಸಾಮಾನ್ಯ ಹೆಸರು ---
| ಐಸೋ ಪ್ರೊಪೀನೈಲ್)
CH3
5 4 3 2 1
CH ≡ C = CH= CH—CH2 2--- ಪೆಂಟೇನ್-- 4----ಯಿನೈಲ್ :
ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳು-ಏಕಚಕ್ರೀಯ ಸಂಯುಕ್ತಗಳು: ಮಾತೃವೃತ್ತಗಳ ಮತ್ತು ಅವುಗಳ ನಿಷ್ಪನ್ನ ಪುಂಜಗಳ ಹೆಸರುಗಳನ್ನು ಪಡೆಯಲು ಅದೇ ಸಂಖ್ಯೆಯ ಇಂಗಾಲ ಪರಮಾಣುಗಳನ್ನುಳ್ಳ ಆಲ್ಕೇನುಗಳ ಹೆಸರುಗಳ ಹಿಂದೆ ಸೈಕ್ಲೋ ಸೇರಿಸಬೇಕು.
ವೃತ್ತಗಳಲ್ಲಿ ದ್ವಿಬಂಧ, ತ್ರಿಬಂಧಗಳಿದ್ದರೆ ಹೆಸರಿನಲ್ಲಿ ಏನ್ ಅಂತ್ಯದ ಬದಲು ಈನ್ ಅಥವಾ ಐನ್ ಅಂತ್ಯ ಸೇರುತ್ತದೆ. ಎರಡೂ ಇದ್ದರೆ ಕ್ರಮಾಂಕದಲ್ಲಿ ದ್ವಿಬಂಧದ ಕ್ರಮಾಂಕದಲ್ಲಿ ದ್ವಿಬಂಧದ ಕ್ರಮಾಂಕ ಕನಿಷ್ಠ.
ಹೆಚ್ಚು ಅಪರ್ಯಾಪ್ತ ಬಂಧಗಳಿದ್ದರೆ ಈನ್, ಐನ್, ಡಯೀನ್ ಟ್ರಯೀನ್ ಮೊದಲಾದುವನ್ನು ಆಲಿಫ್ಯಾಟಿಕ್ ಅಥವಾ ಚಕ್ರೀಯ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಉಪಯೋಗಿಸುವಂತೆಯೇ ಉಪಯೋಗಿಸಲಾಗುತ್ತದೆ.
ಏಕಚಕ್ರೀಯ ಆರೋಮ್ಯಾಟಿಕ್ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಮೊದಲನೆಯದಕ್ಕೆ ಬೆಂಜ಼ೀನ್ ಎಂದು ಹೆಸರು. ಅನೇಕ ಆದೇಶಿತ ಬೆಂಜ಼ೀನ್ಗಳಿಗೆ ಹಳೆಯ ಹೆಸರುಗಳೇ ಉಳಿಯುತ್ತವೆ.
ಕೂಡಿಕೊಂಡಿರುವ ಬಹುಚಕ್ರೀಯ ಸಂಯುಕ್ತಗಳು ಅಥವಾ ವೃತ್ತಪುಂಜಗಳು ಮತ್ತು ಹೆಟಿರೊಸೈಕ್ಲಿಕ್ ಸಂಯುಕ್ತಗಳು: ಇವುಗಳಲ್ಲಿ ಮೊದಲಿನಿಂದ ಪರಿಚಿತವಿರುವ ವೃತ್ತಗಳಿಗೆ ಕ್ರಮಬದ್ಧವಾದ ಹೆಸರಿನ ಬದಲು ಹಳೆಯ ಹೆಸರುಗಳನ್ನೇ ಉಪಯೋಗಿಸಲಾಗುತ್ತದೆ. ಜಟಿಲ ಸಂಯುಕ್ತಗಳಿಗೂ ಕ್ರಮಬದ್ಧವಾದರೂ ಸುಲಭವಲ್ಲದ ಹೆಸರುಗಳಿಗಿಂತಲೂ ಸುಲಭವಾದ ಸಾಮಾನ್ಯ ಹೆಸರುಗಳನ್ನೇ ಉಪಯೋಗಿಸಬಹುದು. ಈ ರೀತಿಯ ಎಲ್ಲ ಬಗೆಯ ವೃತ್ತಗಳ ಹೆಸರುಗಳನ್ನೂ ರಿಂಗ್ಇಂಡೆಕ್ಸ್ ಎಂಬ ಪುಸ್ತಕದಿಂದ ಪಡೆಯಬಹುದು. ಇವುಗಳಲ್ಲಿ ಸ್ಥಾನಗಳ ಕ್ರಮಾಂಕಗಳನ್ನೂ ನಿರ್ದೇಶಿಸಲಾಗುತ್ತದೆ. ಹೊಸದಾಗಿ ಪರಿಚಿತವಾದ ಚಕ್ರೀಯ ಪುಂಜಗಳ ಕ್ರಮಬದ್ಧ ಹೆಸರಗಳೂ ಇಲ್ಲಿವೆ.
ಕ್ರಿಯಾಪುಂಜಗಳು ಮತ್ತು ಅವುಗಳನ್ನುಳ್ಳ ಸಂಯುಕ್ತಗಳ ಹೆಸರುಗಳು:
-O- ಈಥರ್
-OH ಆಲ್ಕೊಹಾಲ್; ಸಂಯುಕ್ತದ ಹೆಸರಿನ ಅಂತ್ಯ ಆಲ್
-N< ಆಮೈನ್
-CH=0 ಆಲ್ಡಿಹೈಡ್; ಸಂಯುಕ್ತದ ಹೆಸರಿನ ಅಂತ್ಯ ಆಲ್
-CO- ಕೀಟೋನ್ (ಆಕ್ಸೋ ಪುಂಜ)
-COOH ಆಮ್ಲ, ಕಾರ್ಬಾಕ್ಸಿಲಿಕ್ ಆಮ್ಲ
-CO-N< ಆಮೈಡ್, ಕಾರ್ಬಾಕ್ಸಮೈಡ್
-COOR ಎಸ್ಟರ್
-CO-X ಆಮ್ಲ ಹ್ಯಾಲೈಡ್
-X ಹ್ಯಾಲೈಡ್
ಕೇವಲ ಇಷ್ಟು ನಿಯಮಗಳ ಕಲೆಯುವಿಕೆಯಿಂದ ಎಲ್ಲ ಸಂಯುಕ್ತಗಳ ಹೆಸರುಗಳನ್ನೂ ಸರಿಯಾಗಿ ಹೇಳಲಾಗದು. ಅನೇಕ ಸಂಯುಕ್ತಗಳಿಗೆ ಹಳೆಯ ಹೆಸರುಗಳೇ ಬಹಳವಾಗಿ ಬಳಕೆಯಲ್ಲಿರುವುದರಿಂದ ಆ ಹೆಸರುಗಳನ್ನು ಹಳೆಯ ಹೆಸರುಗಳೆನ್ನುವುದಕ್ಕಿಂತಲೂ ಬಳಕೆಯ ಹೆಸರುಗಳೆನ್ನುವುದು ಸೂಕ್ತ. ಜಟಿಲ ಸಂಯುಕ್ತಗಳಿಗೆ ಹೆಸರಿಡುವಾಗ ಅವುಗಳ ಆಕರ, ಉಪಯುಕ್ತತೆ ಮೊದಲಾದುವನ್ನು ಆಧಾರವಾಗಿ ತೆಗೆದುಕೊಳ್ಳಬೇಕಾಗುತ್ತದೆ.
ರಚನಾತ್ಮಕ ರೇಖಾ/ಚಿತ್ರಗಳು
[ಬದಲಾಯಿಸಿ]ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಪರಮಾಣುಗಳನ್ನು ಚಿತ್ರಗಳ ಅಥವಾ ಸಂರಚನಾ ಸೂತ್ರಗಳು ಹಾಗೂ ಚಿತ್ರ ಹಾಗೂ ರಾಸಾಯನಿಕ ಚಿಹ್ನೆಗಳ ಸಂಯೋಜನೆಯ ಮೂಲಕ ಸಾಮಾನ್ಯವಾಗಿ ವಿವರಿಸಲಾಗುತ್ತದೆ. ರೇಖೆ-ಕೋನ ಸೂತ್ರವು ಸರಳ ಹಾಗೂ ಸ್ಪಷ್ಟವಾಗಿದೆ. ಈ ವ್ಯವಸ್ಥೆಯಲ್ಲಿ ಅಂತ್ಯಬಿಂದುಗಳು ಹಾಗೂ ಪ್ರತಿರೇಖೆಯ ಛೇದನಗಳು ಒಂದು ಇಂಗಾಲ ಹಾಗೂ ಜಲಜನಕದ ಪರಮಾಣುಗಳನ್ನು ಸ್ಫುಟವಾಗಿ ಲೇಖಿಸಬಹುದು ಅಥವಾ ಸಂಯೋಗ ಸಾಮರ್ಥ್ಯ ನಾಲ್ಕನ್ನು ಹೊಂದಿರುವ ಇಂಗಾಲದ ಉಪಸ್ಥಿತಿಯಿಂದ ಅವುಗಳಿವೆ ಎಂದು ಅಂದಾಜಿಸಬಹುದು. ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳನ್ನು ಚಿತ್ರಗಳ ಮೂಲಕ ಸೂಚಿಸುವುದು ಎಲ್ಲಾ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಇಂಗಾಲವು ನಾಲ್ಕು ಬಂಧಕಗಳನ್ನು ಹೊಂದಿದ್ದು, ಆಮ್ಲಜನಕ ಎರಡು, ಜಲಜನಕ ಒಂದು, ಹಾಗೂ ಸಾರಜನಕ ಮೂರನ್ನು ಹೊಂದಿರುತ್ತದೆ ಎಂಬ ವಿಚಾರದಿಂದ ಸರಳವಾಗಿದೆ.
ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ವರ್ಗೀಕರಣ
[ಬದಲಾಯಿಸಿ]ಕಾರ್ಯಸಂಬಂಧಿ ಗುಂಪುಗಳು
[ಬದಲಾಯಿಸಿ]
ಕಾರ್ಯಸಂಬಂಧಿ ಗುಂಪುಗಳ ಕಲ್ಪನೆಯು ಸಂರಚನೆಗಳನ್ನು ವರ್ಗೀಕರಿಸಲು ಹಾಗೂ ಲಕ್ಷಣಗಳನ್ನು ಅಂದಾಜಿಸಲು ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಕೇಂದ್ರವಾಗಿದೆ. ಕಾರ್ಯಸಂಬಂಧಿ ಗುಂಪು ಎಂದರೆ ಪರಮಾಣು ಘಟಕವಾಗಿದ್ದು ಕಾರ್ಯಸಂಬಂಧಿ ಗುಂಪಿನ ಕಾರ್ಯಶೈಲಿಯನ್ನು ಒಂದು ಮಿತಿಯಲ್ಲಿ ಕೆಲ ವಿಧದ ಪರಮಾಣುಗಳಲ್ಲಿ ಸಮಾನವಾಗಿರುತ್ತದೆ ಎಂದು ಅಂದಾಜಿಸಲಾಗಿರುತ್ತದೆ. ಕಾರ್ಯಸಂಬಂಧಿ ಗುಂಪುಗಳು ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ರಾಸಾಯನಿಕ ಹಾಗೂ ಭೌತಿಕ ಲಕ್ಷಣಗಳ ಮೇಲೆ ನಿರ್ಣಾಯಕ ಪ್ರಭಾವ ಬೀರಬಲ್ಲವು. ಪರಮಾಣುಗಳನ್ನು ಅವುಗಳ ಕಾರ್ಯಸಂಬಂಧಿ ಗುಂಪುಗಳ ಆಧಾರದ ಮೇಲೆ ವರ್ಗೀಕರಿಸಲಾಗಿದೆ. ಉದಾಹರಣೆಗೆ ಎಲ್ಲಾ ಆಲ್ಕೋಹಾಲ್ಗಳು, C-O-H ಉಪ-ಘಟಕವನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಎಲ್ಲಾ ಆಲ್ಕೋಹಾಲ್ಗಳು ಬಹುಮಟ್ಟಿಗೆ ಜಲಾರ್ದ್ರೀಯವಾಗಿ ಈಸ್ಟರ್ಗಳಾಗಿ ನಂತರ ಸಾಮಾನ್ಯವಾಗಿ ಅನುಗುಣವಾದ ಹಾಲೈಡ್ಗಳಾಗಿ ಮಾರ್ಪಡಿಸಲು ಸಾಧ್ಯ. ಬಹಳಷ್ಟು ಕಾರ್ಯಸಂಬಂಧಿ ಗುಂಪುಗಳು ಭಿನ್ನಾಣುಗಳನ್ನು (C ಮತ್ತು H ಅಲ್ಲದ ಪರಮಾಣುಗಳು) ಹೊಂದಿರುತ್ತದೆ. ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳನ್ನು ಕಾರ್ಯಸಂಬಂಧಿ ಗುಂಪುಗಳ ಪ್ರಕಾರ ಆಲ್ಕೋಹಾಲ್ಗಳು, ಕಾರ್ಬೋಆಕ್ಸಿಲ್ ಆಮ್ಲಗಳು, ಅಮೈನ್ಗಳು, etc ಎಂದು ವರ್ಗೀಕರಿಸಲಾಗುತ್ತದೆ.
ಇಂಗಾಲಸಂಯುಕ್ತಗಳಲ್ಲಿ ಅತಿ ಸರಳ ಸಂಯುಕ್ತಗಳೆಂದರೆ ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳು (ಜಲಜನಕೇಂಗಾಲ). ಇವು ಹೈಡ್ರೊಜನ್ ಮತ್ತು ಇಂಗಾಲ ಇವೆರಡೇ ಧಾತುಗಳು ಕೂಡಿ ಆಗಿವೆ. ಇವುಗಳಲ್ಲಿರುವ ಹೈಡ್ರೊಜನ್ನಿನ ಒಂದು ಅಥವಾ ಹೆಚ್ಚು ಪರಮಾಣುಗಳು ಇತರ ಬಗೆಯ ಪುಂಜಗಳಿಂದ ಆದೇಶಿತವಾಗಿ ಇತರ ಬಗೆಯ ಇಂಗಾಲಸಂಯುಕ್ತಗಳ ಸೃಷ್ಟಿಯಾಗಿದೆಯೆಂದು ಭಾವಿಸಬಹುದು. ಈ ಬಗೆಯ ಹೊಸ ಸಂಯುಕ್ತಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು ಈ ಆದೇಶಿತ ಪುಂಜಗಳನ್ನು ಅವಲಂಬಿಸಿವೆ. ಈ ಸಂಯುಕ್ತಗಳು ಭಾಗವಹಿಸುವ ಕ್ರಿಯೆಗಳಿಗೆ ಅನುಗುಣವಾಗಿ ಸಂಯುಕ್ತಗಳನ್ನು ವರ್ಗೀಕರಿಸಲಾಗುವುದರಿಂದ ಈ ಲಕ್ಷಣಕಾರಣ ಪುಂಜಗಳನ್ನು ಕ್ರಿಯಾಪುಂಜಗಳೆಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಮೊದಲ ಬಗೆಯ ವರ್ಗೀಕರಣ ಅಣುಗಳ ಆಕಾರಗಳನ್ನು ಅವಲಂಬಿಸಿದೆ. ಆಕಾರಗಳೂ ಸಂಯುಕ್ತಗಳ ಲಕ್ಷಣಗಳ ಮೇಲೆ ಪ್ರಭಾವ ಬೀರುವುದರಿಂದ ಈ ಬಗೆಯ ವರ್ಗೀಕರಣ ಸಂಯುಕ್ತಗಳ ಅಭ್ಯಾಸಕ್ಕೆ ಅನುಕೂಲವಾಗಿದೆ.
ಹೆಟಿರೋಸೈಕ್ಲಿಕ್ ಸಂಯುಕ್ತಗಳು: ಹೆಸರಿನಿಂದಲೇ ವ್ಯಕ್ತವಾಗುವಂತೆ ಈ ಸಂಯುಕ್ತಗಳು ಚಕ್ರೀಯ ಸಂಯುಕ್ತಗಳು. ಇದುವರೆಗೆ ವಿವರಿಸಿದ ಚಕ್ರೀಯ ಸಂಯುಕ್ತಗಳಿಗೂ ಇವುಗಳಿಗೂ ಇರುವ ವ್ಯತ್ಯಾಸವೆಂದರೆ ಈ ಸಂಯುಕ್ತಗಳು ವೃತ್ತ ನಿರ್ಮಾಣದಲ್ಲಿ ಪಾಲುಗೊಂಡಿರುವ ಪರಮಾಣುಗಳೆಲ್ಲ ಇಂಗಾಲಗಳಲ್ಲ. ಚಕ್ರದ ಒಂದು ಅಥವಾ ಅನೇಕ ಪರಮಾಣುಗಳು ಇತರ ಧಾತುಗಳ ಪರಮಾಣುಗಳು. ನೈಟ್ರೊಜನ್, ಆಕ್ಸಿಜನ್, ಸಲ್ಫರುಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಹೆಟಿರೊಸೈಕ್ಲಿಕ್ ಚಕ್ರಗಳಲ್ಲಿರುವ ಇತರ ಪರಮಾಣುಗಳು. ಇತರ ಚಕ್ರೀಯ ಸಂಯುಕ್ತಗಳಂತೆಯೇ ಈ ಬಗೆಯ ಸಂಯುಕ್ತಗಳಲ್ಲಿಯೂ ಐದು ಅಥವಾ ಆರು ಪರಮಾಣುಗಳನ್ನುಳ್ಳ ಚಕ್ರಗಳೇ ಹೆಚ್ಚುಮಟ್ಟಿಗೆ ಕಾಣಸಿಗುತ್ತವೆ. ಹಲವು ಮುಖ್ಯ ಮತ್ತು ಸಾಮಾನ್ಯ ಹೆಟಿರೊಸೈಕ್ಲಿಕ್ ಸಂಯುಕ್ತಗಳ ರಚನಾಸೂತ್ರಗಳನ್ನು ಕೆಳಗೆ ಕೊಡಲಾಗಿದೆ.
ಚಿತ್ರದಲ್ಲಿ ತೋರಿಸಿರುವ ಸಂಯುಕ್ತಗಳೆಲ್ಲವೂ ಆರೊಮ್ಯಾಟಿಕ್ ಸಂಯುಕ್ತಗಳಾಗಿದ್ದರೂ ಹೆಟಿರೊಸೈಕ್ಲಿಕ್ ಸಂಯುಕ್ತ ಆರೊಮ್ಯಾಟಿಕ್ ಸಂಯುಕ್ತವಾಗಿ ಇರಬೇಕಾದ ಆವಶ್ಯಕತೆಯೇನೂ ಇಲ್ಲ. ಚಕ್ರಕ್ಕೆ ಸೇರಿದ ಹೈಡ್ರೊಜನ್ನನ್ನು ಕ್ರಿಯಾಪುಂಜದಿಂದ ಆದೇಶಿಸಿದಾಗ ಕ್ರಿಯಾಪುಂಜಗಳನ್ನುಳ್ಳ ಹೆಟಿರೋಸೈಕ್ಲಿಕ್ ಸಂಯುಕ್ತಗಳು ದೊರೆಯುತ್ತವೆ.

ಹೆಟೆರೊಸೈಕ್ಲಿಕ್ ಚಕ್ರಗಳು ಅನೇಕ ಪ್ರಕೃತಿದತ್ತ ಜಟಿಲ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳಲ್ಲಿವೆ. ಉದಾಹರಣೆಗೆ ಕ್ಲೊರೋಫಿಲ್ ಮತ್ತು ಬಿ-೧೨ ಜೀವಾತುವಿನಲ್ಲಿ ಪಿರೋಲ್ ವೃತ್ತಗಳಿವೆ. ಇಂಡಿಗೋ ವರ್ಣದ್ರವ್ಯದಲ್ಲಿ ಇಂಡೋಲ್ ಎಂಬ ಹೆಟಿರೋಸೈಕ್ಲಿಕ್ ವೃತ್ತ (ರಿಂಗ್) ರಚನೆಯಿದೆ. ಅನೇಕ ಆಲ್ಕಲಾಯ್ಡುಗಳಲ್ಲಿ ಪಿರೋಲ್, ಪಿಂಡಿನ್, ಕ್ವಿನೋಲಿನ್ ಮತ್ತು ಐಸೋ ಕ್ವಿನೋಲಿನ್ ವೃತ್ತರಚನೆಗಳಿವೆ. ಅದ್ದರಿಂದ ಪ್ರಕೃತಿಯಲ್ಲಿ ದೊರೆಯುವ ಅನೇಕ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳು ಮತ್ತು ಅದರ ಸಂಬಂಧಿಗಳ ಸಂಶ್ಲೇಷಣೆಗಳಲ್ಲಿ ಹೆಟೆರೊಸೈಕ್ಲಿಕ್ ಸಂಯುಕ್ತಗಳನ್ನು ಆರಂಭವಸ್ತುಗಳಾಗಿ ಉಪಯೋಗಿಸಲಾಗುತ್ತದೆ. ಅನೇಕ ಹೆಟೆರೊಸೈಕ್ಲಿಕ್ ಸಂಯುಕ್ತಗಳು ಪ್ರಕೃತಿಯಲ್ಲಿ ದೊರೆಯುವುವು ಮಾತ್ರವಲ್ಲದೆ ಅಸಂಖ್ಯಾತ ಸಂಯುಕ್ತಗಳನ್ನು ಪ್ರಯೋಗಶಾಲೆಯಲ್ಲಿ ಕೃತಕವಾಗಿ ಸಂಶ್ಲೇಷಿಸಲಾಗಿದೆ.
ಜಟಿಲ ಸಂಯುಕ್ತಗಳು: ಇವನ್ನು ಮೇಲೆ ತಿಳಿಸಿದ ಯಾವೊಂದು ವರ್ಗಕ್ಕೂ ಸೇರಿಸಲು ಸಾಧ್ಯವಿಲ್ಲ. ಸಾಮಾನ್ಯವಾಗಿ ಅನೇಕ ಕ್ರಿಯಾಪುಂಜಗಳನ್ನು ಪಡೆದಿರುವುದರಿಂದ ಕ್ರಿಯಾಪುಂಜಕ್ಕನುಗುಣವಾಗಿ ಮಾಡಿದ ವರ್ಗೀಕರಣದಲ್ಲೂ ಸೇರಿಸುವಂತಿಲ್ಲ. ಈ ಸಂಯುಕ್ತಗಳ ಪ್ರತ್ಯೇಕ ವರ್ಗೀಕರಣ ವಿಧಾನಕ್ಕೆ ಆಕರ ಸಾಮ್ಯ, ರಚನಾಸಾಮ್ಯ ಅಥವಾ ಉಪಯುಕ್ತತಾಸಾಮ್ಯಗಳು ಆಧಾರಗಳು.
ಪ್ರಕೃತಿದತ್ತ ಜಟಿಲ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಮುಖ್ಯವಾದ ಗುಂಪುಗಳು ಪ್ರೋಟೀನ್ ಮತ್ತು ಪಾಲಿಪೆಪ್ಟೈಡುಗಳು, ಶರ್ಕರಪಿಷ್ಟಗಳು (ಕಾರ್ಬೊಹೈಡ್ರೇಟುಗಳು) ತೈಲ ಮತ್ತು ಕೊಬ್ಬುಗಳು (ಆಯ್ಲ್ಸ್ ಅಂಡ್ ಫ್ಯಾಟ್ಸ್), ಆಲ್ಕಲಾಯ್ಡುಗಳು, ಜೀವಾತುಗಳು (ವಿಟಮಿನ್ಸ್), ಸ್ಟೆರಾಯ್ಡುಗಳು, ಹಾರ್ಮೋನುಗಳು, ಅಷ್ಟೇ ಅಲ್ಲದೆ ಅನೇಕ ಔಷಧ ದ್ರವ್ಯಗಳು ಮತ್ತು ವರ್ಣದ್ರವ್ಯಗಳೂ ಪ್ರಕೃತಿಯಲ್ಲಿ ದೊರೆಯುತ್ತವೆ.
ಕೃತಕ ಜಟಿಲ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ಮುಖ್ಯವಾದವು ಕೃತಕ ಔಷಧ ದ್ರವ್ಯಗಳು ಮತ್ತು ಬಹ್ವಂಗಗಳು (ಪಾಲಿಮರುಗಳು). ಕೃತಕ ಎಳೆ, ಕೃತಕ ರಬ್ಬರ್, ಪ್ಲಾಸ್ಟಿಕ್ ಮೊದಲಾದುವುಗಳೆಲ್ಲ ಬಹ್ವಂಗಗಳು.
ಕ್ರಿಯಾಪುಂಜಗಳಾವುವೂ ಇಲ್ಲದ ಹೈಡ್ರೊಕಾರ್ಬನ್ನುಗಳು ಮೊದಲನೆಯವು. ಅವುಗಳ ನಿಷ್ಪನ್ನಗಳೆಂದು ಪರಿಗಣಿಸಬಹುದಾದ ಇತರ ಸಂಯುಕ್ತಗಳನ್ನು ಕ್ರಿಯಾಪುಂಜಗಳಿಗನುಗುಣವಾಗಿ ವರ್ಗೀಕರಿಸಲಾಗುತ್ತದೆ.
ಮೇದಸ್ಸಿನ ಸಂಯುಕ್ತಗಳು
[ಬದಲಾಯಿಸಿ]ಮೇದಸ್ಸಿನ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳನ್ನು ಅವುಗಳ ಕ್ಲೇದನ ಸ್ಥಿತಿಯ ಮೇಲೆ ಆಧಾರಿತವಾಗಿ ಮೂರು ಸದೃಶ ಸರಣಿಗಳ ಗುಂಪುಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ:
- ಮೇಣವಸ್ತುಗಳು, ಇವು ದ್ವಿಬಂಧಕ ಅಥವಾ ತ್ರಿಬಂಧಕವಿಲ್ಲದ ಅಲ್ಕೇನ್ಗಳು,
- ಓಲೆಫಿನ್ಗಳು ಅಥವಾ ಅಲ್ಕೀನ್ಗಳು ಒಂದು ಅಥವಾ ಹೆಚ್ಚಿನ ದ್ವಿಬಂಧಕಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ, i.e ಡೈ-ಓಲೆಫಿನ್ಗಳು (ಡೈಯೀನ್ಗಳು) ಅಥವಾ ಪಾಲಿ-ಓಲೆಫಿನ್ಗಳು.
- ಅಲ್ಕೈನ್ಗಳು, ಇವು ಒಂದು ಅಥವಾ ಹೆಚ್ಚಿನ ತ್ರಿಬಂಧಕಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ.
ಗುಂಪಿನ ಉಳಿದವನ್ನು ಲಭ್ಯವಿರುವ ಕಾರ್ಯಸಂಬಂಧಿ ಗುಂಪುಗಳಿಗನುಸಾರವಾಗಿ ವರ್ಗೀಕರಿಸಲಾಗುತ್ತದೆ. ಅಂತಹಾ ಸಂಯುಕ್ತಗಳು "ನೇರ-ಸರಪಣಿಯ," ಶಾಖಾ-ಸರಪಣಿಯ ಅಥವಾ ಆವರ್ತದವಾಗಿರಬಹುದು. ವರ್ಗೀಕರಣದ ಮಟ್ಟವು ಪೆಟ್ರೋಲಿಯಂ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಆಕ್ಟೇನ್ ಸಂಖ್ಯೆ ಅಥವಾ ಸೀಟೇನ್ ಸಂಖ್ಯೆ ಇದ್ದಂತೆ ಲಕ್ಷಣಗಳ ಮೇಲೆ ಪ್ರಭಾವ ಬೀರುತ್ತದೆ. (ಅಲಿಸೈಕ್ಲಿಕ್ ಸಂಯುಕ್ತಗಳು ಹಾಗೂ ಕ್ಲೇದಿತವಲ್ಲದ ಸಂಯುಕ್ತಗಳೆರಡೂ ಆವರ್ತ ರೂಪಾಂತರಗಳಾಗಿರುತ್ತವೆ. ಹೆಚ್ಚಿನ ಸ್ಥಿರತೆಯ ವರ್ತುಲಗಳು ಐದು ಅಥವಾ ಆರು ಇಂಗಾಲ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿದ್ದರೆ, ದೊಡ್ಡ ವರ್ತುಲಗಳು(ಮ್ಯಾಕ್ರೋಸೈಕಲ್ಗಳು) ಹಾಗೂ ಚಿಕ್ಕ ವರ್ತುಲಗಳು ಸಾಮಾನ್ಯವಾಗಿವೆ. ಅತಿ ಸಣ್ಣ ಸೈಕ್ಲೋಆಲ್ಕೇನ್ ಕುಟುಂಬವೆಂದರೆ ಮೂರು ಸದಸ್ಯರ ಸೈಕ್ಲೋಪ್ರೊಪೇನ್ ((CH2)3). ಕ್ಲೇದಿತ ಆವರ್ತ ಸಂಯುಕ್ತಗಳು ಏಕ ಬಂಧಕವನ್ನು ಮಾತ್ರ ಹೊಂದಿದ್ದರೆ, ಸುವಾಸಿತ ವರ್ತುಲಗಳು ಸರದಿಯ (ಅಥವಾ ಸಂಯೋಗದ) ದ್ವಿಬಂಧಕವನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಸೈಕ್ಲೋಆಲ್ಕೇನ್ಗಳು ಬಹುಬಂಧಕಗಳನ್ನು ಹೊಂದಿರುವುದಿಲ್ಲ, ಆದರೆ ಸೈಕ್ಲೋಆಲ್ಕೀನ್ಗಳು ಹಾಗೂ ಸೈಕ್ಲೋಆಲ್ಕೈನ್ಗಳು ಹೊಂದಿರುತ್ತವೆ.
ಸುಗಂಧಿತ ಸಂಯುಕ್ತಗಳು
[ಬದಲಾಯಿಸಿ]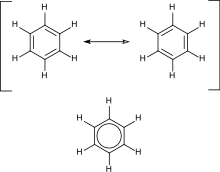
ಸುಗಂಧಿತ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಸಂಯೋಜಿತ ದ್ವಿಬಂಧಕಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಪ್ರಮುಖ ಉದಾಹರಣೆಯೆಂದರೆ ಬೆಂಜೀನ್, ಕೆಕುಲೇ ಇದನ್ನು ಸೂತ್ರೀಕರಿಸಿದ್ದುದಲ್ಲದೇ ಕೇಂದ್ರೀಕರಣ ಅಥವಾ ಅನುರಣನ ಮೂಲತತ್ವದ ಮೂಲಕ ಅದರ ಸಂರಚನೆಯನ್ನು ವಿವರಿಸಿದ್ದರು. "ಸಾಂಪ್ರದಾಯಿಕ" ಆವರ್ತ ಸಂಯುಕ್ತಗಳಿಗೆ, ಸುಗಂಧತ್ವವು n ಒಂದು ಪೂರ್ಣಾಂಕವಾಗಿರುವಾಗ 4n + 2 ಸಂಖ್ಯೆಯ ಕೇಂದ್ರೀಕೃತ ಪೈ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಲಭ್ಯತೆಯ ಮೇರೆಗೆ ಲಭ್ಯವಾಗುತ್ತದೆ. ನಿರ್ದಿಷ್ಟ ಅಸ್ಥಿರತೆಯು (ಸುಗಂಧತ್ವವಲ್ಲದ್ದು) 4n ಸಂಯೋಜಿತ ಪೈ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಲಭ್ಯತೆಯ ಮೇರೆಗೆ ಲಭ್ಯವಾಗುತ್ತದೆ.
ಆವರ್ತಕವಲ್ಲದ ಸಂಯುಕ್ತಗಳು
[ಬದಲಾಯಿಸಿ]ಆವರ್ತಕ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ಲಕ್ಷಣಗಳು ಭಿನ್ನಾಣುಗಳು ಇದ್ದರೆ ಮತ್ತೆ ಬದಲಾಗುತ್ತದೆ ಇವು ವರ್ತುಲಕ್ಕೆ ಬಾಹ್ಯವಾಗಿ ಸಂಪರ್ಕಿತವಾದ, (ಎಕ್ಸೋಸೈಕ್ಲಿಕ್) ಅಥವಾ ವರ್ತುಲದ ಸದಸ್ಯವಾಗಿಯೇ (ಎಂಡೋಸೈಕ್ಲಿಕ್) ಲಭ್ಯವಿರುವ ಆದೇಶ್ಯವಾಗಿರುತ್ತವೆ. ದ್ವಿತೀಯ ಸಂದರ್ಭದಲ್ಲಿ ವರ್ತುಲವನ್ನು ಅನಾವರ್ತ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಪೈರಿಡೈನ್ ಹಾಗೂ ಫುರಾನ್ಗಳು ಸುಗಂಧಿತ ಅನಾವರ್ತಗಳ ಉದಾಹರಣೆಯಾದರೆ ಪಿಪೆರಿಡೈನ್ ಹಾಗೂ ಟೆಟ್ರಾಹೈಡ್ರೋಫುರಾನ್ಗಳು ಸಂಬಂಧಿತ ಅಲಿಸೈಕ್ಲಿಕ್ ಅನಾವರ್ತಗಳಾಗಿವೆ. ಅನಾವರ್ತಿತ ಪರಮಾಣುಗಳ ಭಿನ್ನಾಣುಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಆಮ್ಲಜನಕ, ಗಂಧಕ, ಅಥವಾ ಸಾರಜನಕ, ಅದರಲ್ಲೂ ಕೊನೆಯದು ಜೀವರಾಸಾಯನಿಕ ವ್ಯವಸ್ಥೆಗಳಲ್ಲಿ ಸಾಮಾನ್ಯವಾಗಿದೆ. ಅನಾವರ್ತಗಳಲ್ಲಿನ ಗುಂಪುಗಳ ಉದಾಹರಣೆಯೆಂದರೆ ಅನಿಲೈನ್ ಡೈಗಳು, ಜೀವರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಪ್ರಸ್ತಾಪಗೊಳ್ಳುವ ಅಲ್ಕಲಾಯ್ಡ್ಗಳು, ಜೀವಸತ್ವಗಳಿಗೆ ಸಂಬಂಧಪಟ್ಟ ಅನೇಕ ಸಂಯುಕ್ತಗಳು, ಸ್ಟಿರಾಯ್ಡ್ಗಳು, ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲಗಳು (e.g. DNA, RNA) ಹಾಗೂ ಅನೇಕ ಔಷಧಿಗಳಲ್ಲಿ ಬಳಸಲಾಗುವ ಸಂಯುಕ್ತಗಳು. ಸರಳ ಸಂರಚನೆಯ ಅನಾವರ್ತಗಳೆಂದರೆ ಪೈರ್ರೋಲ್ (5-ಸದಸ್ಯರ) ಹಾಗೂ ಇಂಡೋಲ್ (6-ಸದಸ್ಯರ ಇಂಗಾಲದ ವರ್ತುಲ). ವರ್ತುಲಗಳು ಇತರೆ ವರ್ತುಲಗಳೊಂದಿಗೆ ಒಂದು ತುದಿಯಲ್ಲಿ ಸೇರಿಕೊಂದು ಬಹುಆವರ್ತದ ಸಂಯುಕ್ತಗಳನ್ನು ನೀಡುತ್ತವೆ. ಪ್ಯೂರಿನ್ ನ್ಯೂಕ್ಲಿಯೋಸೈಡ್ ಪ್ರತ್ಯಾಮ್ಲಗಳು ಪ್ರಮುಖ ಬಹುಆವರ್ತಿತ ಸುಗಂಧಿತ ಅನಾವರ್ತಗಳಾಗಿವೆ. ವರ್ತುಲಗಳು ಒಂದು "ಮೂಲೆಯಲ್ಲಿ" ಸೇರಿ ಒಂದು ಪರಮಾಣು (ಬಹುಮಟ್ಟಿಗೆ ಯಾವಾಗಲೂ ಇಂಗಾಲ) ಎರಡು ಬಂಧಕಗಳನ್ನು ಹೊಂದಿರುವ ಒಂದು ಆವರ್ತವಾಗಿದ್ದು ಹಾಗೂ ಎರಡನೆಯದಕ್ಕೆ ಎರಡು ಆವರ್ತಗಳಾಗಿರುತ್ತವೆ. ಅಂತಹಾ ಸಂಯುಕ್ತಗಳನ್ನು ಸ್ಪೈರೋ ಎಂದು ಕರೆಯಲಾಗುತ್ತದಲ್ಲದೇ ಅನೇಕ ನೈಸರ್ಗಿಕ ಉತ್ಪನ್ನಗಳಲ್ಲಿ ಅವು ಬಹಳ ಮುಖ್ಯವಾಗಿವೆ.
ಪಾಲಿಮರ್ಗಳು
[ಬದಲಾಯಿಸಿ]
ಇಂಗಾಲದ ಒಂದು ಪ್ರಮುಖ ಲಕ್ಷಣವೆಂದರೆ ಇಂಗಾಲ-ಇಂಗಾಲ ಬಂಧಕಗಳಿಂದ ಸಂಪರ್ಕಿತಗೊಳ್ಳುವ ಸರಪಣಿ ಹಾಗೂ ಜಾಲಗಳನ್ನು ಸಹಾ ಕೂಡಲೇ ನಿರ್ಮಿಸಿಕೊಳ್ಳಬಲ್ಲದು. ಸಂಪರ್ಕಗೊಳ್ಳುವಿಕೆಯ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಪಾಲಿಮರೀಕರಣ ಎನ್ನಲಾಗುತ್ತದಲ್ಲದೇ ಮೂಲ ಸಂಯುಕ್ತವು ಮಾನೋಮರ್ ಆಗಿದ್ದಾಗ ಇದು ಪಾಲಿಮರ್ಗಳನ್ನು ಬಂಧಿಸುತ್ತದೆ ಇಲ್ಲವೇ ಜಾಲವನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ. ಪಾಲಿಮರ್ಗಳ ಎರಡು ಪ್ರಮುಖ ಗುಂಪುಗಳಿವೆ: ಕೃತಕವಾಗಿ ಉತ್ಪಾದನೆಯಾದವನ್ನು ಔದ್ಯಮಿಕ ಪಾಲಿಮರ್ಗಳು[೮] ಅಥವಾ ಕೃತಕ ಪಾಲಿಮರ್ಗಳು ಹಾಗೂ ನೈಸರ್ಗಿಕವಾಗಿ ರಚಿತವಾದವನ್ನು ಜೈವಿಕ ಪಾಲಿಮರ್ಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಪ್ರಥಮ ಕೃತಕ ಪಾಲಿಮರ್, ಬೇಕ್ಲೈಟ್ನ ಆವಿಷ್ಕಾರದ ನಂತರ, ಅದರ ಕುಟುಂಬವು ಇತರೆ ಪಾಲಿಮರ್ಗಳ ಆವಿಷ್ಕಾರಗಳೊಂದಿಗೆ ತೀವ್ರ ಬೆಳವಣಿಗೆ ಕಂಡಿತು. ಸಾಮಾನ್ಯ ಕೃತಕ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಪಾಲಿಮರ್ಗಳೆಂದರೆ ಪಾಲಿಈಥೈಲೀನ್ (ಪಾಲಿಥಿನ್), ಪಾಲಿಪ್ರಾಪೈಲೀನ್, ನೈಲಾನ್, ಟೆಫ್ಲಾನ್ (PTFE), ಪಾಲಿಸ್ಟೈರೀನ್, ಪಾಲಿಸ್ಟರ್ಗಳು, ಪಾಲಿಮೀಥೈಲ್ಮೆಥಾಕ್ರೈಲೇಟ್ (ಪರ್ಸ್ಪ್ಲೆಕ್ಸ್ ಹಾಗೂ ಪ್ಲೆಕ್ಸಿಗ್ಲಾಸ್ ಎಂದು ಕರೆಯಲ್ಪಡುತ್ತವೆ), ಹಾಗೂ ಪಾಲಿವಿನೈಲ್ಕ್ಲೋರೈಡ್ (PVC). ಕೃತಕ ಹಾಗೂ ನೈಸರ್ಗಿಕ ರಬ್ಬರ್ಗಳು ಸಹಾ ಪಾಲಿಮರ್ಗಳೇ ಆಗಿವೆ. ಉದಾಹರಣೆಗಳು ಸಾಧಾರಣ ಪದಗಳಾಗಿದ್ದು, ಭೌತಿಕ ಲಕ್ಷಣಗಳನ್ನು ನಿರ್ದಿಷ್ಟ ಬಳಕೆಗೆಂದು ಹೊಂದಿಸಿದ ಪ್ರತಿಯೊಂದರ ಅನೇಕ ವಿಧಗಳು ಇರಬಹುದಾಗಿದೆ. ಸರಪಣಿಯ ಉದ್ದ ಬದಲಿಸುವ, ಅಥವಾ ಶಾಖೆ ಅಥವಾ ಟ್ಯಾಕ್ಟಿಸಿಟಿ ರಚಿಸುವ ಮೂಲಕ ಪಾಲಿಮರೀಕರಣದ ಸ್ಥಿತಿಗಳ ಬದಲಿಕೆಯು ಉತ್ಪನ್ನದ ರಾಸಾಯನಿಕ ಸಂಯೋಜನೆಯನ್ನೇ ಬದಲಿಸುತ್ತದೆ. ಏಕ ಮಾನೋಮರ್ ಬಳಕೆಯ ಉತ್ಪನ್ನವೆಂದರೆ ಹೋಮೋಪಾಲಿಮರ್. ಅಲ್ಲದೇ, ಮಾಧ್ಯಮಿಕ ಘಟಕ(ಗಳ)ನ್ನು ಸೇರಿಸಿ ಹೆಟಿರೋಪಾಲಿಮರ್ (ಕೋ-ಪಾಲಿಮರ್) ಹಾಗೂ ವಿವಿಧ ಘಟಕಗಳ ಸಮುದಾಯಗಳನ್ನು ಜೋಡಿಸುವಿಕೆಯ ಮಟ್ಟವನ್ನು ಸಹಾ ನಿಯಂತ್ರಿಸಬಹುದಾಗಿದೆ. ಗಡಸುತನ, ಸಾಂದ್ರತೆ, ಯಾಂತ್ರಿಕ ಅಥವಾ ಕರ್ಷಕ ಬಲ, ಸವೆತ ವಿರೋಧ, ಉಷ್ಣವಿರೋಧ, ಪಾರದರ್ಶಕತೆ, ವರ್ಣ etc. ಭೌತಿಕ ಲಕ್ಷಣಗಳು ಅಂತಿಮ ಸಂಯುಕ್ತದ ಮೇಲೆ ಆಧಾರಿತವಾಗಿರುತ್ತವೆ.
ಜೈವಿಕ ಪರಮಾಣುಗಳು
[ಬದಲಾಯಿಸಿ]
ಜೈವಿಕ ಪರಮಾಣುಗಳ ರಸಾಯನಶಾಸ್ತ್ರವು ಜೈವಿಕರಸಾಯನ ತಜ್ಞರು ಆಗ್ಗಾಗ್ಗೆ ಅಧ್ಯಯನಕ್ಕೊಳಪಡುವ ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಒಂದು ಪ್ರಮುಖ ವಿಭಾಗವಾಗಿದೆ. ಅನೇಕ ಸಂಕೀರ್ಣ ಬಹುಕಾರ್ಯ ಗುಂಪು ಪರಮಾಣುಗಳು ಜೀವಿಗಳಲ್ಲಿ ಅತಿ ಪ್ರಮುಖವಾದವು. ಕೆಲವು ದೀರ್ಘ-ಬಂಧಕದ ಜೈವಿಕಪಾಲಿಮರ್ಗಳು, ಹಾಗೂ ಇವು ಪೆಪ್ಟೈಡ್ಗಳು, DNA, RNA ಹಾಗೂ ಪ್ರಾಣಿಗಳಲ್ಲಿ ಪಿಷ್ಟ ಹಾಗೂ ಸಸ್ಯಗಳಲ್ಲಿ ಕೋಶಗಳಂತೆ ಪಾಲಿಸಕರೈಡ್ಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಇತರೆ ಪ್ರಮುಖ ವರ್ಗಗಳೆಂದರೆ ಅಮೈನೋ ಆಮ್ಲಗಳು (ಪ್ರೋಟೀನ್ಗಳ ಪ್ರಮುಖ ಅಂಶವಾದ ಮಾನೋಮರ್), ಕಾರ್ಬೋಹೈಡ್ರೇಟ್ಗಳು (ಪಾಲಿಸಕರೈಡ್ಗಳನ್ನು ಹೊಂದಿರುವ), ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲಗಳು (DNA ಹಾಗೂ RNAಗಳನ್ನು ಪಾಲಿಮರ್ಗಳಾಗಿ ಹೊಂದಿರುವ), ಹಾಗೂ ಮೇದಸ್ಸು. ಇದರೊಂದಿಗೆ ಪ್ರಾಣಿಗಳ ದೇಹವು ಕ್ರೆಬ್ಸ್ ಆವರ್ತದ ಮೂಲಕ ಶಕ್ತಿ ಉತ್ಪಾದನೆಗೆ ಸಹಾಯ ಮಾಡುವ ಅನೇಕ ಸಣ್ಣ ಮಧ್ಯವರ್ತಿ ಅಣುಗಳನ್ನು ಹೊಂದಿರುವುದಲ್ಲದೇ, ಪ್ರಾಣಿಗಳಲ್ಲಿ ಬಹು ಸಾಮಾನ್ಯ ಹೈಡ್ರೋಕಾರ್ಬನ್ ಆದ ಐಸೋಪ್ರೀನ್ ಅನ್ನು ಉತ್ಪಾದಿಸುತ್ತದೆ. ಪ್ರಾಣಿಗಳಲ್ಲಿ ಐಸೋಪ್ರೀನ್ಗಳು ಪ್ರಮುಖ ಸಂರಚನಾತ್ಮಕ ಸ್ಟಿರಾಯ್ಡ್ (ಕೊಲೆಸ್ಟರಾಲ್ ) ಹಾಗೂ ಸ್ಟಿರಾಯ್ಡ್ ಹಾರ್ಮೋನ್ ಸಂಯುಕ್ತಗಳಾಗುವವಲ್ಲದೇ; ಸಸ್ಯಗಳಲ್ಲಿ ಟರ್ಪೀನ್ಗಳು, ಟರ್ಪಿನಾಯ್ಡ್ಗಳು, ಕೆಲ ಅಲ್ಕಲಾಯ್ಡ್ಗಳು, ಹಾಗೂ ರಬ್ಬರ್ ಉತ್ಪಾದಿಸಲು ಬಳಸುವ ಜೈವಿಕ ಪಾಲಿಮರ್ ಪಾಲಿಐಸೋಪ್ರೆನಾಯ್ಡ್ಗಳೆಂದು ಕರೆಯಲ್ಪಡುವ ಸಸ್ಯಕ್ಷೀರದ ಸತ್ವದಲ್ಲಿ ಲಭ್ಯವಿರುವ ವಿಶಿಷ್ಟ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಇರುತ್ತವೆ.
- ಪೆಪ್ಟೈಡ್ ಸಂಶ್ಲೇಷೀಕರಣ
- ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೋಟೈಡ್ ಸಂಶ್ಲೇಷೀಕರಣ
- ಕಾರ್ಬೋಹೈಡ್ರೇಟ್ ಸಂಶ್ಲೇಷೀಕರಣ
ಸಣ್ಣ ಪರಮಾಣುಗಳು
[ಬದಲಾಯಿಸಿ]ಔಷಧವಸ್ತುಶಾಸ್ತ್ರದಲ್ಲಿ, 'ಸಣ್ಣ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು' ಎಂದೂ ಕರೆಯಲ್ಪಡುವ ಸಣ್ಣ ಪರಮಾಣುಗಳು ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ಪ್ರಮುಖ ಗುಂಪಾಗಿವೆ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಸಣ್ಣ ಪರಮಾಣುವೆಂದರೆ ಜೈವಿಕವಾಗಿ ಸಕ್ರಿಯವಾಗಿರುವ ಪಾಲಿಮರ್ ಅಲ್ಲದ ಸಣ್ಣ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತವಾಗಿರುತ್ತದೆ. ಬಳಕೆಯಲ್ಲಿ ಸಣ್ಣ ಪರಮಾಣುಗಳು ಸರಿಸುಮಾರು 1000 g/molಗಿಂತ ಕಡಿಮೆ ಪ್ರಮಾಣದ ಮೋಲಾರ್/ಆರ್ದ್ರ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಹೊಂದಿರುತ್ತವೆ.

ಫುಲ್ಲರೀನ್ಗಳು
[ಬದಲಾಯಿಸಿ]ಅಂಡಗೋಳ ಹಾಗೂ ಕೊಳವೆಯಂತಹಾ ರಚನೆಯ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳಾದ ಫುಲ್ಲರೀನ್ಗಳು ಹಾಗೂ ಇಂಗಾಲ ನ್ಯಾನೋಟ್ಯೂಬ್ಗಳು, ವಸ್ತುವಿಜ್ಞಾನದ ಸಂಬಂಧಿತ ಕ್ಷೇತ್ರದಲ್ಲಿ ಹೆಚ್ಚಿನ ಸಂಶೋಧನೆಗಳಿಗೆ ಇಂಬು ನೀಡಿವೆ.
ಇತರೆ:
[ಬದಲಾಯಿಸಿ]ಇಂಗಾಲದಿಂದ ಸಾರಜನಕ, ಆಮ್ಲಜನಕ ಹಾಗೂ ಹಾಲೋಜನ್ಗಳೊಂದಿಗೆ ಬಂಧಿತವಾಗಿರುವ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳನ್ನು ಪ್ರತ್ಯೇಕವಾಗಿ ವರ್ಗೀಕರಿಸಲಾಗಿದೆ. ಇತರವುಗಳನ್ನು ಕೆಲಬಾರಿ ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿಯೇ ಪ್ರಮುಖ ವರ್ಗಗಳಲ್ಲಿ ಸೇರಿಸಲಾಗುತ್ತದೆ ಹಾಗೂ ಸಾವಯವ ಗಂಧಕರಸಾಯನಶಾಸ್ತ್ರ, ಸಾವಯವ ಲೋಹರಸಾಯನಶಾಸ್ತ್ರ, ಸಾವಯವ ರಂಜಕರಸಾಯನಶಾಸ್ತ್ರ ಹಾಗೂ ಸಾವಯವ ಸಿಲಿಕಾನ್ರಸಾಯನಶಾಸ್ತ್ರ ಎಂಬ ಶೀರ್ಷಿಕೆಗಳಡಿಯಲ್ಲಿ ಸೇರಿಸಲಾಗುತ್ತದೆ.
ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಶ್ಲೇಷೀಕರಣ
[ಬದಲಾಯಿಸಿ]
ಕೃತಕ ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ ಎಂಬುದು "ರಚನೆ, ವಿಶ್ಲೇಷಣೆ, ಹಾಗೂ/ಅಥವಾ ಕಾರ್ಯಶೀಲ ಉದ್ದೇಶಗಳಿಗೆ ಕಾರ್ಯ ನಿರ್ಮಾಣ"ವಾದ ಯಂತ್ರಜ್ಞಾನಕ್ಕೆ ಸಮೀಪವಾಗಿರುವ ಕಾರಣ ಅನ್ವಯಿಕ ವಿಜ್ಞಾನವೆಂದೆನಿಸಿಕೊಳ್ಳುತ್ತದೆ. ಉದ್ದೇಶಿತ ಪರಮಾಣುವಿಗೆಂದು ಸೂಕ್ತ ಆರಂಭಿಕ ವಸ್ತುಗಳನ್ನು ಆಯ್ಕೆ ಮಾಡಿ ಸಿದ್ಧಪಡಿಸುವ ಸಂಶ್ಲೇಷೀಕರಣದಂತಹಾ ಅಪೂರ್ವ ಸಂಯುಕ್ತವೊಂದರ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಶ್ಲೇಷೀಕರಣವು ಸಮಸ್ಯೆ ಪರಿಹಾರದಂತಹಾ ಕಾರ್ಯವಾಗಿದೆ. ಸಂಕೀರ್ಣ ಸಂಯುಕ್ತಗಳು ಅಗತ್ಯದ ಪರಮಾಣುವನ್ನು ರಚಿಸುವ ಹತ್ತಾರು ಅನುಕ್ರಮ ಪ್ರತಿಕ್ರಿಯಾ ಹಂತಗಳನ್ನು ಹೊಂದಿರಬಹುದು. ಸಂಶ್ಲೇಷೀಕರಣವು ಪರಮಾಣುವಿನ ಕಾರ್ಯಕಾರಿ ಗುಂಪುಗಳ ಪ್ರತಿಕ್ರಿಯಾಶೀಲತೆಯನ್ನು ಬಳಸಿಕೊಂಡು ಮುಂದುವರೆಯುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ಕಾರ್ಬೋನಿಲ್ ಸಂಯುಕ್ತವನ್ನು ಎನೋಲೇಟ್ ಆಗಿ ಇಲ್ಲವೇ ಎಲೆಕ್ಟ್ರೋಫೈಲ್; ಆಗಿ ಪರಿವರ್ತಿಸಿ ನ್ಯೂಕ್ಲಿಯೋಫೈಲ್ ಆಗಿ ಬಳಸಬಹುದು ಎರಡರ ಸಂಯೋಜನೆಯನ್ನು ಅಲ್ಡೋಲ್ ಪ್ರಕ್ರಿಯೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಪ್ರಯೋಗಾಲಯದಲ್ಲಿ ವಾಸ್ತವಿಕ ಸಂಶ್ಲೇಷೀಕರಣ ಮಾಡುವ ಮೂಲಕ ಮಾತ್ರವೇ ಕಾರ್ಯತಃ ಉಪಯುಕ್ತ ಸಂಶ್ಲೇಷೀಕರಣವನ್ನು ರಚಿಸಬಹುದು. ಸಂಕೀರ್ಣ ಪರಮಾಣುಗಳಿಗೆಂದು ಅಪೂರ್ವ ಕೃತಕ ಮಾರ್ಗಗಳನ್ನು ನಿರ್ಮಿಸುವುದನ್ನು ಸಂಪೂರ್ಣ ಸಂಶ್ಲೇಷೀಕರಣ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಸಂಶ್ಲೇಷೀಕರಣವನ್ನು ರಚಿಸಲು ಅನೇಕ ಕಾರ್ಯನೀತಿಗಳಿವೆ. E.J. ಕೊರೆಯವರು ಅಭಿವೃದ್ಧಿಪಡಿಸಿದ ಆಧುನಿಕ ಪ್ರತಿಸಂಶ್ಲೇಷೀಕರಣ ವಿಧಾನವು, ಉದ್ಧೇಶಿತ ಪರಮಾಣುವಿನೊಂದಿಗೆ ಆರಂಭವಾಗಿ ಪರಿಚಿತ ಬಿಡಿ ಪ್ರಕ್ರಿಯೆಗಳಾಗಿ ಪ್ರತ್ಯೇಕಗೊಳ್ಳುತ್ತದೆ. ಬಿಡಿ ಪ್ರಕ್ರಿಯೆಗಳು ಅಥವಾ ಪ್ರಸ್ತಾಪಿತ ಪೂರ್ವಗಾಮಿಗಳೊಂದಿಗೆ ಲಭ್ಯವಾಗುವವರೆಗೆ ಹಾಗೂ ಅಗ್ಗದ ಆರಂಭಿಕ ವಸ್ತುಗಳ ಹಂತಕ್ಕೆ ತಲುಪುವವರೆಗೆ ಅದೇ ಪ್ರಕ್ರಿಯೆಗೆ ಒಳಗಾಗುತ್ತಿರುತ್ತವೆ. ನಂತರ ಪ್ರತಿಸಂಶ್ಲೇಷೀಕರಣದ ವಿಧಾನವನ್ನು ವಿರುದ್ಧ ದಿಕ್ಕಿನಲ್ಲಿ ದಾಖಲಿಸಿ ಸಂಶ್ಲೇಷೀಕರಣವನ್ನು ಪಡೆಯಲಾಗುತ್ತದೆ. "ಕೃತಕ ಮರ"ವನ್ನು ನಿರ್ಮಿಸಬಹುದು, ಏಕೆಂದರೆ ಪ್ರತಿ ಸಂಯುಕ್ತವು ಹಾಗೂ ಪ್ರತಿ ಪೂರ್ವಗಾಮಿಯು ಬಹು ಸಂಶ್ಲೇಷಣೆಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ.
ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಪ್ರತಿಕ್ರಿಯೆಗಳು
[ಬದಲಾಯಿಸಿ]ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳನ್ನೊಳಗೊಂಡ ರಾಸಾಯನಿಕ ಪ್ರತಿಕ್ರಿಯೆಗಳಾಗಿರುತ್ತವೆ. ಶುದ್ಧ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ನಿರ್ದಿಷ್ಟ ವರ್ಗದ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಮಾತ್ರ ನೀಡಿದರೆ, ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಸಂಯುಕ್ತಗಳು ಒಳಗಾಗುವ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಬಹುಮಟ್ಟಿಗೆ ಕಾರ್ಯಕಾರಿ ಗುಂಪುಗಳ ಮೇಲೆ ಆಧಾರವಾಗಿರುತ್ತದೆ. ಈ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಸಾಮಾನ್ಯ ಸಿದ್ಧಾಂತವು ಪ್ರಮುಖ ಪರಮಾಣುಗಳ ಎಲೆಕ್ಟ್ರಾನ್ ಸಾಮ್ಯತೆ, ಬಂಧದ ಸಾಮರ್ಥ್ಯ ಹಾಗೂ ಕ್ರಿಯಾರೋಧಗಳಂತಹ ಲಕ್ಷಣಗಳ ಎಚ್ಚರಿಕೆಯ ವಿಶ್ಲೇಷಣೆಯನ್ನೊಳಗೊಂಡಿರುತ್ತದೆ. ಈ ಪರಿಣಾಮಗಳು ಪ್ರತಿಕ್ರಿಯೆಯ ಮಾರ್ಗವನ್ನು ನಿರ್ಧರಿಸುವ ಅಲ್ಪಕಾಲೀನ ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕ ಮಧ್ಯವರ್ತಿಗಳ ಸಾಪೇಕ್ಷ ದೃಢತೆಯನ್ನು ನಿರ್ಧರಿಸಬಲ್ಲವು.
ಮೂಲಭೂತ ಪ್ರತಿಕ್ರಿಯಾ ಪ್ರಭೇದಗಳೆಂದರೆ: ಅನುಬಂಧಕ ಪ್ರತಿಕ್ರಿಯೆಗಳು, ನಿವಾರಣಾತ್ಮಕ ಪ್ರತಿಕ್ರಿಯೆಗಳು, ಬದಲಿಕೆಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು, ಆವರ್ತವನ್ನಾವರಿಸಿದ ಪ್ರತಿಕ್ರಿಯೆಗಳು, ಪ್ರತಿಕ್ರಿಯೆಗಳ ಹಾಗೂ ಆಕ್ಸಿಡೀಕರಣ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಪುನರ್-ಹೊಂದಾಣಿಕೆಗಳು. ಸಾಧಾರಣ ಪ್ರತಿಕ್ರಿಯೆಯ ಉದಾಹರಣೆಯೆಂದರೆ ಬದಲಿಕೆಯ ಪ್ರತಿಕ್ರಿಯೆಯಾದ:
- Nu− + C-X → C-Nu + X−
ಇಲ್ಲಿ X ಒಂದು ಕಾರ್ಯಕಾರಿ ಗುಂಪು ಹಾಗೂ Nu ಒಂದು ನ್ಯೂಕ್ಲಿಯೋಫೈಲ್ ಆಗಿರುತ್ತದೆ. ಸಂಭವನೀಯ ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಸಂಖ್ಯೆ ಮೂಲಭೂತವಾಗಿ ಅಪರಿಮಿತ. ಆದಾಗ್ಯೂ ಅನೇಕ ಸಾಧಾರಣ ಅಥವಾ ಉಪಯುಕ್ತ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ವಿವರಿಸಬಲ್ಲ ನಿರ್ದಿಷ್ಟ ಸಾಧಾರಣ ಶೈಲಿಗಳನ್ನು ವಿಷದೀಕರಿಸಬಹುದಾಗಿದೆ. ಪ್ರತಿ ಪ್ರತಿಕ್ರಿಯೆಯು ಕ್ರಮವಾದ ಸರಣಿಯಲ್ಲಿನ ಪ್ರತಿಕ್ರಿಯಾ ವಿಧಾನವನ್ನು ಹೊಂದಿರುತ್ತವೆ, ಆದರೆ ಕೇವಲ ಭಾಗಿಗಳ ಪಟ್ಟಿಯಿಂದಲೇ ಹಂತಗಳ ವಿವರಣಾತ್ಮಕ ವರ್ಣನೆ ಯಾವಾಗಲೂ ಸಾಧ್ಯವಾಗಲೇ ಬೇಕೆಂದೇನಿಲ್ಲ.
ಉಪಯೋಗಗಳು
[ಬದಲಾಯಿಸಿ]ಅಧಿಕ ಸಂಖ್ಯೆಯ ಜೀವಜನ್ಯ ಸಂಯುಕ್ತಗಳು ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳಾದ್ದರಿಂದ ಅವನ್ನು ಕಾಣುವುದು ಮತ್ತು ಉಪಯೋಗಿಸುವುದು ಅನಿವಾರ್ಯವೇ ಆಗಿದೆ. ಕೂಲಂಕಷ ಪರಿಶೀಲನೆಯ ಪರಿಣಾಮವಾಗಿ ಜೀವನದ ಇರುವಿಕೆಗೇ ಕಾರಣವಾದ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ವಿಷಯವಾಗಿ ಇಂದು ಅಧಿಕ ಜ್ಞಾನ ಪಡೆದಿದ್ದೇವೆ. ಪ್ರೋಟೀನ್, ಎನ್ಜೈಮ್, ಹಾರ್ಮೊನ್ ಮೊದಲಾದುವುಗಳ ವಿಷಯವಾದ ತಿಳಿವಳಿಕೆ ಜೀವ ರಸಾಯನಶಾಸ್ತ್ರ ಮತ್ತು ಅಣುಜೀವಶಾಸ್ತ್ರದ ಅಭ್ಯಾಸಗಳ ಮೊದಲ ಹಂತ. ವಿಜ್ಞಾನದ ಉಳಿದ ಅನೇಕ ವಿಭಾಗಗಳ ಅಭ್ಯಾಸಿಗಳು ಸದಾ ತಮಗೆ ಬೇಕಾದ ಸಲಕರಣೆಗಳಿಗಾಗಿ, ವಿಧಾನಗಳಿಗಾಗಿ ಇಂಗಾಲಸಂಯುಕ್ತಗಳತ್ತ ನೋಡುತ್ತಲೇ ಇರಬೇಕಾಗುತ್ತದೆ. ಜೀವರಸಾಯನಶಾಸ್ತ್ರ ಮತ್ತು ಅಣುಜೀವಶಾಸ್ತ್ರಗಳು ಇಂಗಾಲ ಸಂಯುಕ್ತರಸಾಯನಶಾಸ್ತ್ರದಿಂದಲೇ ಅಂಕುರಗೊಂಡಿರುವ ಹೊಸ ರಸಾಯನಶಾಸ್ತ್ರ ವಿಭಾಗಗಳು.
ಸಸ್ಯ ಮತ್ತು ಪ್ರಾಣಿಸಂಪತ್ತು: ಕಳೆದ ಮೂವತ್ತೈದು ವರ್ಷಗಳಿಂದ ಪ್ರಪಂಚದ ಪ್ರತಿ ದೇಶದಲ್ಲಿಯೂ ಬೇಸಾಯಗಾರರು ಹಚ್ಚು ಬೆಳೆ ಪಡೆಯಲು ಪ್ರಯುತ್ನಿಸುತ್ತಿದ್ದಾರೆ. ಈ ಪ್ರಯತ್ನಗಳಿಗೆ ಪೋಷಕವಾಗಿರುವ ವಸ್ತುಗಳೆಂದರೆ ಕೃತಕ ಗೊಬ್ಬರ ಮತ್ತು ಕೀಟ-ವೈರಸ್ ನಾಶಕಗಳು ಮತ್ತು ಕಳೆನಾಶಕಗಳು. ಕೃತಕ ಗೊಬ್ಬರಗಳು ಬಲುಮಟ್ಟಿಗೆ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳಲ್ಲ - ನಿರವಯವ ಲವಣಗಳು.
ಔಷಧ ವಿಜ್ಞಾನ: ಔಷಧ ರಂಗದಲ್ಲಿ ಉಪಯೋಗಿಸುತ್ತಿರುವ ಅಸಂಖ್ಯಾತ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ೯೦%ಕ್ಕೂ ಮೀರಿದ ಸಂಯುಕ್ತಗಳು ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳು. ಹೊರಗಾಯಕ್ಕೆ ಹಚ್ಚುವ ಮುಲಾವಿನಲ್ಲಿ, ಒಳಹುಣ್ಣಿನ ಉಪಶಮನದಲ್ಲಿ, ಎಲ್ಲ ಬಗೆಯ ದೈಹಿಕ ರೋಗ ಚಿಕಿತ್ಸೆಗಳಲ್ಲಿ ಅನೇಕ ಮಾನಸಿಕ ರೋಗ ಚಿಕಿತ್ಸೆಗಳಲ್ಲಿ ಶಸ್ತ್ರ ಚಿಕಿತ್ಸೆಗಳಲ್ಲಿ (ವೇದನಾಪ್ರತಿಬಂಧಕವಾಗಿ), ರೋಗಕಾರಕ ಸೂಕ್ಷಾಣು ಜೀವಿಗಳ ಎದುರು ಚಿಕಿತ್ಸೆಗಳಲ್ಲಿ ಶರೀರದ ಅಂಗಗಳ ಕಾರ್ಯಗಳನ್ನು ನಿಯಂತ್ರಿಸಲು, ಜನನ ನಿಯಂತ್ರಣಕ್ಕಾಗಿ - ಹೀಗೆ ಕೊನೆಯಿಲ್ಲದಷ್ಟು ಉಪಯೋಗಗಳನ್ನು ಪಡೆದಿರುವ ಔಷಧಗಳು ಬಲು ಪಾಲಿಗೆ ಇಂಗಾಲಸಂಯುಕ್ತಗಳು. ರಾಸಾಯನಿಕ ಚಿಕಿತ್ಸೆ ಇಂದು ನಾವು ಅನೇಕ ರೋಗಗಳನ್ನು ಗೆಲ್ಲಲು ನೆರವು ನೀಡಿದೆ.
ಕೈಗಾರಿಕೋದ್ಯಮಗಳು: ಯಾವ ಕೈಗಾರಿಕೋದ್ಯಮವೂ ಪ್ರಕೃತಿಯ ಕಚ್ಚಾ ವಸ್ತುಗಳಿಲ್ಲದೆ ಬಲುಕಾಲ ನಡೆಯುವಂತಿಲ್ಲ. ಪ್ರಕೃತಿಯ ಬಲುಪಾಲು ವಸ್ತುಗಳು ಇಂಗಾಲಸಂಯುಕ್ತಪೂರಿತವಾದ್ದರಿಂದ ಇಂಗಾಲಸಂಯುಕ್ತಗಳನ್ನು ಸ್ವಲ್ಪವಾದರೂ ಉಪಯೋಗಿಸದ ಉದ್ಯಮಗಳೇ ಇಲ್ಲವೆನ್ನಬಹುದು. ಇಂದಿನ ದಿವಸಗಳಲ್ಲಿ ಹೆಚ್ಚು ಹೆಚ್ಚು ಪ್ರಮಾಣದಲ್ಲಿ ಉಪಯೋಗಿಸಲಾಗುತ್ತಿರುವ ಪ್ಲಾಸ್ಟಿಕ್ಕುಗಳು, ಕೃತಕ ಎಳೆಗಳು, ಚೊಕ್ಕಾರಕಗಳು, ವಿವಿಧ ಕೃತಕ ಮತ್ತು ಸಹಜ ವರ್ಣದ್ರವ್ಯಗಳು, ವಾಹನಗಳಿಗೆ ಉರುವಲಾಗಿ ಉಪಯೋಗಿಸುತ್ತಿರುವ ಪೆಟ್ರೋಲ್, ಸೀಮೆಎಣ್ಣೆ, ಡೀಸೆಲ್ ಎಣ್ಣೆಗಳ ಮೂಲವಾದ ಪೆಟ್ರೋಲಿಯಂ ಮೊದಲಾದುವುಗಳೆಲ್ಲ ಇಂಗಾಲಸಂಯುಕ್ತರಸಾಯನಶಾಸ್ತ್ರದ ಅಂಕೆಗೆ ಒಳಪಟ್ಟಿವೆ.
ದೇಶಸಂರಕ್ಷಣೆ: ಯುದ್ಧರಂಗದಲ್ಲಿಯೂ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಉಪಯೋಗ ಬೇಕಾದಷ್ಟಿದೆ. ಪ್ರಸಿದ್ಧ ಸ್ಪೋಟಕಗಳಾದ ಟಿ.ಎನ್.ಟಿ., ನೈಟ್ರೊಗ್ಲಿಸರಿನ್ ಮೊದಲಾದವುಗಳು ಇಂಗಾಲಸಂಯುಕ್ತಗಳು. ನೈಟ್ರೋಸಂಯುಕ್ತಗಳಿಂದ ಕೂಡಿದ ರಾಕೆಟ್ ಇಂಧನಗಳು, ರಾಕೆಟ್ ಇಂಧನದ ಆವರಣಗಳಿಗಾಗಿ ಉಪಯೋಗಿಸುವ ವಿಶಿಷ್ಟ ದರ್ಜೆಯ ಪ್ಲಾಸ್ಟಿಕ್ಕುಗಳೇ ಮೊದಲಾದುವು ಈ ರಂಗದಲ್ಲಿ ಇಂಗಾಲ ಸಂಯುಕ್ತಗಳ ಮುಖ್ಯ ಉಪಯೋಗಗಳನ್ನು ಪ್ರತಿನಿಧಿಸುತ್ತವೆ. ವಿಪರೀತ ದೈಹಿಕ ಮತ್ತು ಮಾನಸಿಕ ಪರಿಣಾಮಗಳನ್ನುಂಟುಮಾಡುವ ಅಶ್ರುವಾಯುವಿನಂಥ (ಟಿಯರ್ ಗ್ಯಾಸ್) ಮತ್ತು ಅದಕ್ಕೂ ಹೆಚ್ಚು ಹಾನಿಕರವಾದ ಅನೇಕ ಇಂಗಾಲಸಂಯುಕ್ತಗಳನ್ನು ಯುದ್ದಗಳಲ್ಲಿ ಉಪಯೋಗಿಸಲಾಗುತ್ತದೆ.
ಇವನ್ನೂ ಗಮನಿಸಿ
[ಬದಲಾಯಿಸಿ]- ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಪ್ರಮುಖ ಪ್ರಕಟಣೆಗಳು
- ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಪಟ್ಟಿ
- ಪರಮಾಣುಗಳ ಮಾದರಿಗಳು
ಆಕರಗಳು
[ಬದಲಾಯಿಸಿ]- ↑ [0] ^ ರಾಬರ್ಟ್ T. ಮಾರ್ರಿಸನ್, ರಾಬರ್ಟ್ N. ಬಾಯ್ಡ್, ಹಾಗೂ ರಾಬರ್ಟ್ K. ಬಾಯ್ಡ್, ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ , 6ನೇ ಆವೃತ್ತಿ (ಬೆಂಜಮಿನ್ ಕಮ್ಮಿಂಗ್ಸ್, 1992, ISBN 0-13-643669-2) - ಇದು "ಮಾರಿಸನ್ ಹಾಗೂ ಬಾಯ್ಡ್", ಅತ್ಯುತ್ತಮ ಪುಸ್ತಕ
- ↑ [1] ^ ಜಾನ್ D. ರಾಬರ್ಟ್ಸ್, ಮರ್ಜೋರಿ C. ಕ್ಯಾಸೆರಿಯೋ, ಬೇಸಿಕ್ ಪ್ರಿನ್ಸಿಪಲ್ಸ್ ಆಫ್ ಆರ್ಗ್ಯಾನಿಕ್ ಕೆಮಿಸ್ಟ್ರಿ ,(W. A. ಬೆಂಜಮಿನ್, Inc. ,1964) - ಮತ್ತೊಂದು ಶ್ರೇಷ್ಟ ಪುಸ್ತಕ
- ↑ [2] ^ ರಿಚರ್ಡ್ F. ಹಾಗೂ ಸ್ಯಾಲಿ J. ಡಾಲೆ, ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ , ಆನ್ಲೈನ್ ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ ಪುಸ್ತಕ. Ochem4free.info
- ↑ Orchin, Milton; Macomber, Roger S.; Pinhas, Allan; Wilson, R. Marshall (2005). "1. Atomic Orbital Theory" (PDF). The Vocabulary and Concepts of Organic Chemistry (2nd ed.). Wiley. Archived (PDF) from the original on 9 October 2022.
- ↑ Brittin, W. E. (1945). "Valence Angle of the Tetrahedral Carbon Atom". J. Chem. Educ. 22 (3): 145. Bibcode:1945JChEd..22..145B. doi:10.1021/ed022p145.
- ↑ L. Pauling The Nature of the Chemical Bond (3rd ed., Oxford University Press 1960) p.111–120.
- ↑ [5] ^ "ದ ಸಿಸ್ಟಮ್ಯಾಟಿಕ್ ಐಡೆಂಟಿಫಿಕೇಷನ್ ಆಫ್ ಆರ್ಗ್ಯಾನಿಕ್ ಕಾಂಪೌಂಡ್ಸ್ " R.L. ಷ್ರೀನರ್r, C.K.F. ಹರ್ಮನ್, T.C. ಮಾರ್ರಿಲ್, D.Y. ಕರ್ಟಿನ್, ಹಾಗೂ R.C. ಫ್ಯೂಸನ್ ಜಾನ್ ವಿಲೇ & ಸನ್ಸ್, 1997 0-471-59748-1
- ↑ "ಇಂಡಸ್ಟ್ರಿಯಲ್ ಪಾಲಿಮರ್ಸ್ , ಕೆಮಿಸ್ಟ್ರಿ ಆಫ್." ಬ್ರಿಟಾನಿಕಾ ವಿಶ್ವಕೋಶ 2006
ಹೊರಗಿನ ಕೊಂಡಿಗಳು
[ಬದಲಾಯಿಸಿ]- MIT.edu Archived 2007-04-21 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ಓಪನ್ಕೋರ್ಸ್ವೇರ್ : ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ I
- HaverFord.edu, ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ ಉಪನ್ಯಾಸಗಳು, ವಿಡಿಯೋಗಳು ಹಾಗೂ ಲೇಖನಗಳು
- ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ವೈಜ್ಞಾನಿಕ ಪತ್ರಿಕೆ (ಸದಸ್ಯತ್ವ ಅಗತ್ಯ) (ಪರಿವಿಡಿ)
- ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಪತ್ರಗಳು(Pubs.ACS.org, ಪರಿವಿಡಿ)
- Thime-Connect.com Archived 2008-01-24 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ಸಿನ್ಲೆಟ್
- Thieme-Connect.com Archived 2009-01-19 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ಸಂಶ್ಲೇಷೀಕರಣ
- Organic-Chemistry.org, ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ ಜಾಲತಾಣ - ಇತ್ತೀಚಿನ ಸಾರಾಂಶಗಳು ಹಾಗೂ (ನಾಮ)ಪ್ರತಿಕ್ರಿಯೆಗಳು
- Orgsyn.org, ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ ಸಂಶ್ಲೇಷೀಕರಣ ವೈಜ್ಞಾನಿಕ ಪತ್ರಿಕೆ
- Ochem4free.info, ಸಂಪೂರ್ಣ ಆನ್ಲೈನ್, ತಜ್ಞರಿಂದ-ವಿಮರ್ಶಿತ ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಲೇಖನಗಳ ಮೂಲತಾಣ
- CEM.MSU.edu, ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಅವಾಸ್ತವ ಪುಸ್ತಕ
- ವಿಶ್ವವ್ಯಾಪಿ ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ ಸ್ರೋತಗಳು - ಕೊಂಡಿಗಳ ಸಂಗ್ರಹ Archived 2015-03-16 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ.
- Thinkquest.org Archived 2009-02-26 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ಇಂಗಾಲೀಯ/ಜೈವಿಕ/ಸಾವಯವ ಕುಟುಂಬಗಳು ಹಾಗೂ ಅವುಗಳ ಕಾರ್ಯಕಾರಿ ಗುಂಪುಗಳು
- Organic.RogerFrost.com, ರೋಗ/ಜರ್ ಫ್ರಾಸ್ಟ್ರ ಆರ್ಗ್ಯಾನಿಕ್ ಕೆಮಿಸ್ಟ್ರಿ - ಮಲ್ಟಿಮೀಡಿಯಾ ಫಾರ್ ಟೀಚಿಂಗ್ ಅಂಡ್ ಲರ್ನಿಂಗ್
- ChemHelper.com Archived 2020-02-03 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಸಹಾಯ
- Organic-Chemistry-Tutor.com Archived 2019-08-01 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ ಶಿಕ್ಷಕ
- ACDlabs.com Archived 2010-07-22 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ರಾಸಾಯನಿಕ ಉಚಿತ ತಂತ್ರಾಂಶ
- Chemaxon.com Archived 2010-01-20 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ಕೆಮ್ಆಕ್ಸಾನ್ನಿಂದ ರಾಸಾಯನಿಕ ಉಚಿತ ತಂತ್ರಾಂಶ.
- AceOrganicChem.com Archived 2010-01-23 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ.,
- OrgChemInfo.8k.com Archived 2010-06-16 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಸ್ರೋತಗಳ ಸಂಗ್ರಹ
- Benzylene.com Archived 2009-10-16 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ., ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರ ಪ್ರಕ್ರಿಯೆಗಳು, ವಿಧಾನಗಳು, ಹಾಗೂ ಸಮಸ್ಯೆಗಳು
- Beilstein-Journals.org, ಇಂಗಾಲೀಯ ರಸಾಯನಶಾಸ್ತ್ರದ ಬೇಲ್ಸ್ಟೇನ್ ವೈಜ್ಞಾನಿಕ ಪತ್ರಿಕೆ (ಮುಕ್ತ ಲಭ್ಯತೆ))