ವಿದ್ಯುದ್ವಿಭಜನೆ (ಎಲೆಕ್ಟ್ರೋಲೈಸಿಸ್)
Lua error in package.lua at line 80: module 'Module:Pagetype/setindex' not found.

ರಸಾಯನ ಶಾಸ್ತ್ರ ಮತ್ತು ಉತ್ಪನ್ನ ತಯಾರಿಕೆಯಲ್ಲಿ, ವಿದ್ಯುದ್ವಿಭಜನೆ ಎಂಬುದು ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯನ್ನು ವೇಗದಲ್ಲಿ ಚಾಲನೆಗೊಳಿಸಲು ವಿದ್ಯುತ್ಪ್ರವಾಹವನ್ನು ಬಳಸುವ ಒಂದು ವಿಧಾನ. ಸ್ವಾಭಾವಿಕವಾಗಿ ದೊರೆಯುವ ಅದಿರುಗಳಲ್ಲಿರುವ ಮೂಲವಸ್ತುಗಳನ್ನು ವಿದ್ಯುದ್ವಿಭಜನಿಯ ಕೋಶಗಳನ್ನು ಬಳಸಿ ಧಾತುಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸುವ ಹಂತದಲ್ಲಿ ವಿದ್ಯುದ್ವಿಭಜನೆಯು ವಾಣಿಜ್ಯಾತ್ಮಕವಾಗಿ ಅತ್ಯಂತ ಪ್ರಮುಖ ಪಾತ್ರವಹಿಸುತ್ತದೆ.
ಇತಿಹಾಸ[ಬದಲಾಯಿಸಿ]
- 1800ರಲ್ಲಿ - ವಿಲಿಯಂ ನಿಕೋಲ್ಸನ್ ಮತ್ತು ಜಾನ್ ರೀಟರ್ ನೀರಿನಿಂದ ಜಲಜನಕ ಮತ್ತು ಆಮ್ಲಜನಕವನ್ನು ವಿಭಜನೆ ಮಾಡಿದರು.
- 1807ರಲ್ಲಿ - ಸರ್ ಹಂಫ್ರೆಯ್ ಡೇವೀಯವರು ವಿದ್ಯುದ್ವಿಭಜನೆಯನ್ನು ಬಳಸಿ ಪೊಟ್ಯಾಶಿಯಂ,ಸೋಡಿಯಂ,ಬೇರಿಯಂ,ಕ್ಯಾಲ್ಸಿಯಂ ಮತ್ತು ಮೆಗ್ನೀಶಿಯಂಗಳನ್ನು ಕಂಡುಹಿಡಿದರು.
- 1886ರಲ್ಲಿ - ಹೆನ್ರಿ ಮೈಸಾನ್ ವಿದ್ಯುದ್ವಿಭಜನೆಯನ್ನು ಬಳಸಿ ಪ್ಲೋರಿನ್ ಅನ್ನು ಕಂಡುಹಿಡಿದರು.
- 1886ರಲ್ಲಿ - ಅಲ್ಯೂಮಿನಿಯಂ ಉತ್ಪಾದನೆಗೆ ಹಾಲ್ ಹೆರೌಲ್ಟ್ ವಿಧಾನವನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಯಿತು.
- 1890ರಲ್ಲಿ - ಸೋಡಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್ ಉತ್ಪಾದನೆಗೆ ಕ್ಯಾಸ್ಟ್ನೇರ್-ಕೆಲ್ಲ್ನೇರ್ ವಿಧಾನವನ್ನು ವೃದ್ಧಿಪಡಿಸಲಾಯಿತು.
ಸ್ಥೂಲ ಅವಲೋಕನ[ಬದಲಾಯಿಸಿ]
ವಿದ್ಯುದ್ವಿಭಜನೆಯು ವಿದ್ಯುತ್ಪ್ರವಾಹವು ಕರಗಿದ ಅಯಾನು ರೂಪದಲ್ಲಿರುವ ದ್ರಾವಕದ ಮೂಲಕ ಹಾದು ಹೋಗುವಂತೆ ಮಾಡುವ ಮಾರ್ಗವಾಗಿದ್ದು, ಇದರ ಪರಿಣಾಮದಿಂದಾಗಿ ವಿದ್ಯುದ್ಧ್ರುವಗಳಲ್ಲಿ ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳು ಉಂಟಾಗಿ ಮೂಲವಸ್ತುಗಳು ಬೇರ್ಪಡುತ್ತವೆ.
ವಿದ್ಯುದ್ವಿಭಜನೆ ಮಾಡಲು ಬೇಕಾಗುವ ಪ್ರಮುಖ ಅಂಶಗಳು (ಘಟಕಗಳು):
- ದ್ರವಪದಾರ್ಥ ಹೊಂದಿರುವಂತಹ ಸುಲಭವಾಗಿ ಚಲಿಸುವಂತಹ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳು -ವಿದ್ಯುದ್ವಿಭಾಜಕ
- ನೇರ ವಿದ್ಯುತ್ಪ್ರವಾಹದ ಬಾಹ್ಯ ಮೂಲ
- ಎರಡು ಘನವಾದ ಕಡ್ಡಿಗಳು ಅಥವಾ ತಟ್ಟೆಗಳನ್ನು ವಿದ್ಯುದ್ಧ್ರುವಗಳೆನ್ನುತ್ತಾರೆ.
ಈ ಘಟಕಗಳು ವಿದ್ಯುದ್ವಿಭಜನೆಯ ವಿಧಾನದಲ್ಲಿ ಕೆಳಗಿನ ಪಾತ್ರಗಳನ್ನು ನಿರ್ವಹಿಸುತ್ತವೆ:
- ಸುಲಭವಾಗಿ ಚಲಿಸುವಂತಹ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳು ದ್ರವಪದಾರ್ಥ(ವಿದ್ಯುದ್ವಿಭಾಜಕ) ದಲ್ಲಿನ ವಿದ್ಯುತ್ಪ್ರವಾಹದ ವಾಹಕಗಳಾಗಿರುತ್ತವೆ. ಘನವಾದ ಲವಣದಲ್ಲಿ, ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳು ಸುಲಭವಾಗಿ ಚಲಿಸದೆ ಇದ್ದಲ್ಲಿ ವಿದ್ಯುದ್ವಿಭಜನೆ ಉಂಟಾಗುವುದಿಲ್ಲ.
- ಬಾಹ್ಯವಾಗಿ ಪೂರೈಸಿರುವ ನೇರ ವಿದ್ಯುತ್ಪ್ರವಾಹ, ದ್ರವ ಪದಾರ್ಥ ಅಥವಾ ದ್ರಾವಣದಲ್ಲಿ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳನ್ನು ಉತ್ಪತ್ತಿ ಮಾಡಲು ಅಥವಾ ವಿಸರ್ಜಿಸಲು ಬೇಕಾಗುವ ಶಕ್ತಿಯನ್ನು ಒದಗಿಸುತ್ತದೆ. ಹೊರಗಿನ ವಿದ್ಯುತ್ಪಥದಲ್ಲಿರುವ ವಿದ್ಯುದ್ಧ್ರುವಗಳಿಂದ ವಿದ್ಯುತ್ಪ್ರವಾಹವನ್ನು ಸರಬರಾಜು ಮಾಡುತ್ತದೆ.
- ವಿದ್ಯುದ್ಧ್ರುವಗಳು ಈ ಕೆಳಗನವುಗಳ ನಡುವೆ ಭೌತಿಕ ಸಂಪರ್ಕವನ್ನು ಏರ್ಪಡಿಸುತ್ತವೆ.
- ವಿದ್ಯುದ್ವಿಭಜನೆ ಉಂಟಾಗಲು ವಿದ್ಯುತ್ಪಥವು ಶಕ್ತಿಯನ್ನು ಒದಗಿಸುತ್ತದೆ.
- ವಿದ್ಯುದ್ವಿಭಾಜಕ ಪ್ರತ್ಯೇಕಗೊಂಡಿರುವ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳ ಪದಾರ್ಥಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ.
ವಿದ್ಯುದ್ಧ್ರುವಗಳು ವಿದ್ಯುತ್ ವಾಹಕಗಳಾಗಿ ವರ್ತಿಸುವಂತಹವುಗಳಾಗಿರ ಬೇಕು. ಲೋಹ, ಗ್ರಾಫೈಟ್ ಮತ್ತು ಅರೆವಾಹಕ ವಸ್ತುಗಳನ್ನು ಹೆಚ್ಚಾಗಿ ವಿದ್ಯುದ್ಧ್ರುವಗಳಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ. ಸೂಕ್ತ ವಿದ್ಯುದ್ಧ್ರುವವು ಈ ಕೆಳಗಿನ ಆಯ್ಕೆಗಳ ಮೇಲೆ ಆಧಾರವಾಗಿರುತ್ತದೆ:
- ವಿದ್ಯುದ್ಧ್ರುವ ಮತ್ತು ವಿದ್ಯುದ್ವಿಭಾಜಕಗಳ ನಡುವೆ ರಾಸಾಯನಿಕ ಪ್ರತಿಕ್ರಿಯೆಗಳು.
- ವಿದ್ಯುದ್ಧ್ರುವ ತಯಾರಿಕೆಯ ವೆಚ್ಚ
ಕೆಳಗಿನವುಗಳನ್ನೊಳಗೊಂಡು ವಿದ್ಯುದ್ವಿಭಜನೆಯನ್ನು ಸಾಧಿಸಲು ಪೂರಕ ಪ್ರಾಯೋಗಿಕ ಸಾಧಾನ ಸಾಮಗ್ರಿಗಳ ಅವ್ಯಶಕವಿದೆ:
- ಪ್ರತಿಕ್ರಿಯಾಕಾರಿಗಳು ಮತ್ತು ಉತ್ಪನ್ನಗಳನ್ನು ಒದಗಿಸಲು, ಹೊಂದಿಸಲು ಮತ್ತು ತೆಗೆಯಲು ನಾಳಗಳು ಅಥವಾ ಕೊಳವೆಗಳು ಬೇಕಾಗುತ್ತವೆ.
- ವಿದ್ಯುತ್ಪಥ
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ವಿಧಾನ[ಬದಲಾಯಿಸಿ]
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಸ್ಥಾಯಿ ವಿಧಾನವೆಂದರೆ, ಬಾಹ್ಯ ವಿದ್ಯುತ್ಪಥದಿಂದ ವಿದ್ಯುತ್ಕಣಗಳನ್ನು (ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು) ತೆಗೆದುಹಾಕುವಿಕೆ ಅಥವಾ ಸೇರಿಸುವಿಕೆಯಿಂದ ಅಣುಗಳು ಮತ್ತು ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳನ್ನು(ಅಯಾನ್ಗಳು) ವಿನಿಮಯಮಾಡುವುದು. ವಿದ್ಯುದ್ವಿಭಜನೆಗೆ ಅವಶ್ಯಕವಾಗಿರುವ ಸಾಮಗ್ರಿಗಳು, ವಿದ್ಯುದ್ವಿಭಾಜಕಲ್ಲಿ ಕೆಲವು ವಿಭಿನ್ನ ಭೌತಿಕ ಸ್ಥಿತಿಯಲ್ಲಿರುತ್ತವೆ, ಮತ್ತು ಕೆಲವು ಭೌತಿಕ ವಿಧಾನದಿಂದ ಅದನ್ನು ತೆಗೆದುಹಾಕಬಹುದಾಗಿದೆ.
ಉದಾಹರಣೆಗೆ, ಹೈಡ್ರೋಜನ್, ಕ್ಲೋರಿನ್ಗಳನ್ನು ಉತ್ಪತ್ತಿ ಮಾಡುವ ಉಪ್ಪುನೀರಿನ ವಿದ್ಯುದ್ವಿಭಜನೆಯಲ್ಲಿ ಉತ್ಪನ್ನಗಳು ಅನಿಲರೂಪದಲ್ಲಿರುತ್ತವೆ. ಈ ಅನಿಲರೂಪದ ಉತ್ಪನ್ನಗಳು ವಿದ್ಯುದ್ವಿಭಾಜಕದಲ್ಲಿ ಗುಳ್ಳೆಯಾಗಿ ಸಂಗ್ರಹವಾಗುತ್ತವೆ.
ದ್ರವಪದಾರ್ಥ ಹೊಂದಿರುವಂತಹ ಮೊಬೈಲ್ ಅಯಾನ್ಗಳು (ಸುಲಭವಾಗಿ ಚಲಿಸುವಂತಹ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳು) (ವಿದ್ಯುದ್ವಿಭಾಜಕ) ಈ ಕೆಳಗಿನ ಅಂಶಗಳ ಪ್ರಕಾರ ತಯಾರಾಗುತ್ತವೆ.
- ಸುಲಭವಾಗಿ ಚಲಿಸುವಂತಹ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳ ಉತ್ಪತ್ತಿ ಮಾಡಲು, ದ್ರಾವಕದೊಂದಿಗೆ (ಒಂದು ರೀತಿಯ ಆಮ್ಲೀಯ) ದ್ರವೀಕರಣ ಅಥವಾ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳ ರೂಪದಲ್ಲಿರುವ ಸಂಯುಕ್ತದ ಪ್ರಕ್ರಿಯೆ.
- ಶಾಖದಿಂದ ದ್ರವೀಕರಿಸಿದ (ಕರಗಿಸಿದ )ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳ ರೂಪದಲ್ಲಿರುವ ಸಂಯುಕ್ತ
ವಿದ್ಯುದ್ವಿಭಾಜಕದೊಳಗೆ ಮುಳುಗಿಸಿರುವ ಜೋಡಿ ವಿದ್ಯುದ್ಧ್ರುವಗಳಿಗೆ ಅಡ್ದಲಾಗಿ ವಿದ್ಯುತ್ತಿನ ಸಾಮರ್ಥ್ಯವನ್ನು ಆನ್ವಯಿಕೆ ಮಾಡಬೇಕು.
ಪ್ರತಿ ವಿದ್ಯುದ್ಧ್ರುವವು ವಿರುದ್ದ ವಿದ್ಯುದಂಶದಲ್ಲಿರುವ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳನ್ನು ಆಕರ್ಷಿಸುತ್ತವೆ. ಧನಾತ್ಮಕ-ವಿದ್ಯುದಂಶವಾಗಿರುವ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳು (ಧನ ಅಯಾನುಗಳು ಅಥವಾ ಧನ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳು) ವಿದ್ಯುತ್ಕಣ-ಕ್ಯಾಥೋಡ್ (ಋಣಾತ್ಮಕ) ಪೂರೈಕೆಯ ಕಡೆಗೆ ಸಾಗುತ್ತವೆ, ಆದರೆ ಋಣಾತ್ಮಕ-ವಿದ್ಯುದಂಶವಾಗಿರುವ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳು (ಋಣ ಅಯಾನುಗಳು ಅಥವಾ ಋಣ ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳು) ಧನಾತ್ಮಕ ಅನೋಡ್ ಕಡೆಗೆ ಸಾಗುತ್ತವೆ.
ವಿದ್ಯುದ್ಧ್ರುವಗಳಲ್ಲಿ ವಿದ್ಯುತ್ಕಣಗಳು, ಅಣುಗಳು ಮತ್ತು ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳನ್ನು ಹಿಡಿದಿಟ್ಟುಕೊಳ್ಳುತ್ತವೆ ಅಥವಾ ಬಿಡುಗಡೆ ಮಾಡುತ್ತವೆ. ಅಂತಹ ಅಣುಗಳು, ಅವು ವಿದ್ಯುತ್ಕಣಗಳನ್ನು ಪಡೆಯುವ ಅಥವಾ ಕಳೆದುಕೊಳ್ಳುವ
ವಿದ್ಯುದಂಶವಾದ ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳಾಗಿ ವಿದ್ಯುದ್ವಿಭಾಜಕದೊಳಗೆ ಹೋಗುತ್ತವೆ. ಅಂತಹ ವಿದ್ಯುತ್ದಾವಿಷ್ಟ ಕಣಗಳು, ಅವು ವಿದ್ಯುತ್ಕಣಗಳನ್ನು ಪಡೆಯುವ ಅಥವಾ ಕಳೆದುಕೊಳ್ಳುವ ಅವಿದ್ಯುದಂಶವಾದ ಅಣುಗಳಾಗಿ ವಿದ್ಯುದ್ವಿಭಾಜಕದಿಂದ ಪ್ರತ್ಯೇಕಗೊಳ್ಳುತ್ತವೆ. ವಿದ್ಯುದಾವಿಷ್ಟ ಕಣಗಳಿಂದ ಅವಿದ್ಯುದಂಶವಾದ ಅಣುಗಳು ರಚನೆಯಾಗುವುದಕ್ಕೆ ವಿಸರ್ಜನೆಯಾಗುವುದು(ಡಿಸ್ಚಾರ್ಜಿಂಗ್) ಎಂದು ಕರೆಯುತ್ತಾರೆ.
ವಿದ್ಯುದ್ಧ್ರುವಗಳಲ್ಲಿ ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳು ಸ್ಥಳಾಂತರವನ್ನುಂಟುಮಾಡಲು ಶಕ್ತಿ ಅವಶ್ಯಕ ಮತ್ತು ಶಕ್ತಿ ವಿದ್ಯುದಾವಿಷ್ಟಕಣ ರೂಪದ ಸ್ಥಿತಿಯಲ್ಲಿ (ಅಯಾನಿಕ್ ಸ್ಥಿತಿ) ಬದಲಾವಣೆಯನ್ನುಂಟು ಮಾಡುತ್ತದೆ, ಇದು ಹೊರಗಿನ ಮೂಲ ವಿದ್ಯುತ್ ಸಾಮರ್ಥ್ಯವನ್ನು ಒದಗಿಸುತ್ತದೆ.
ವಿದ್ಯುದ್ಧ್ರುವಗಳಲ್ಲಿ ಉತ್ಕರ್ಷಣ ಮತ್ತು ಅಪಕರ್ಷಣ[ಬದಲಾಯಿಸಿ]
ನೋಡಿ ಉತ್ಕರ್ಷಣ - ಅಪಕರ್ಷಣ
ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳ ಉತ್ಕರ್ಷಣ ಅಥವಾ ಅನೋಡ್ನಲ್ಲಿ ತಟಸ್ಥ ಪರಮಾಣುಗಳು ಉಂಟಾಗುತ್ತವೆ ಮತ್ತು ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳ ಅಪಕರ್ಷಣ ಅಥವಾ ಕ್ಯಾಥೋಡ್ನಲ್ಲಿ ತಟಸ್ಥ ಪರಮಾಣುಗಳು ಉಂಟಾಗುತ್ತವೆ. ಉದಾಹರಣೆಗೆ, ಅನೋಡ್ನಲ್ಲಿ ಕಬ್ಬಿಣಯುಕ್ತ(ಫೆರಸ್) ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳಿಂದ ಕಬ್ಬಿಣದ (ಫೆರಿಕ್) ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳನ್ನು ಉತ್ಕರ್ಷಿಸಬಹುದು:
- Fe2+
aq → Fe3+
aq + e–
ಹಾಗೆಯೇ ಕ್ಯಾಥೋಡ್ನಲ್ಲಿಯೂ ಸಹ ಫೆರಿಕ್ಸಯನೈಡ್ ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳಿಂದ ಫೆರೋಸಯನೈಡ್ ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳನ್ನು ಮಾರ್ಪಾಡು ಮಾಡಬಹುದಾಗಿದೆ:
- Fe(CN)3-
6 + e– → Fe(CN)4-
6
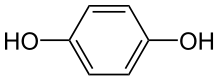
ತಟಸ್ಥ ಪರಮಾಣುಗಳು ವಿದ್ಯುದ್ಧ್ರುವವಾಗಿಯೂ ವರ್ತಿಸಬಲ್ಲವು. ಉದಾಹರಣೆಗೆ: ಕ್ಯಾಥೋಡ್ನಲ್ಲಿ ಹೈಡ್ರೋಕ್ವೀನಾನ್ ಅನ್ನು ಪಿ-ಬೆನ್ಜೋಕ್ವಿನಾನ್ ಆಗಿ ಮಾರ್ಪಾಡಿಸಬಹುದಾಗಿದೆ:
ಕೊನೆಯ ಉದಾಹರಣೆಯಲ್ಲಿ, H+ ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳು (ಹೈಡ್ರೋಜನ್ ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳು) ಸಹ ಪ್ರತಿಕ್ರಿಯೆಯ ಭಾಗವಾಗಿವೆ ಮತ್ತು ಇವು ದ್ರಾವಣದಲ್ಲಿ ಆಮ್ಲೀಯ ಅನ್ನು ಒದಗಿಸುತ್ತವೆ ಅಥವಾ ದ್ರಾವಕವೇ ಒದಗಿಸಿಕೊಳ್ಳುತ್ತದೆ (ನೀರು,ಮೆಥೆನಾಲ್ ಮುಂತಾದವುಗಳು). ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು H+ ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ, ಇವು ಆಮ್ಲೀಯ ದ್ರಾವಣಗಳಲ್ಲಿ ಸಮೃದ್ದವಾಗಿರುವುದು ಸಾಮಾನ್ಯ. ಆಲ್ಕಲೈನ್ ದ್ರಾವಣಗಳ ಪ್ರತಿಕ್ರಿಯೆಗಳು, OH- (ಹೈಡ್ರಾಕ್ಸೈಡ್ ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳು) ಅನ್ನು ಒಳಗೊಂಡಿರುವುದು ಸಾಮಾನ್ಯ.
ವಿದ್ಯುದ್ಧ್ರುವಗಳಾಗಿ ಅಥವಾ ದ್ರಾವಕವಾಗಿಯೂ (ಸಾಮಾನ್ಯವಾಗಿ ನೀರು) ಸಹ ಪದಾರ್ಥಗಳನ್ನು ಉತ್ಕರ್ಷಣೆಮಾಡಬಹುದು ಅಥವಾ ಮಾರ್ಪಡಿಸಬಹುದು. ವಿದ್ಯುದ್ವಿಭಜನೆಯೂ ಅನಿಲಗಳನ್ನು ಒಳಗೊಂಡಿದ್ದಾಗ ಇದು ಸಾಧ್ಯವಾಗುತ್ತದೆ.
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಅವಧಿಯಲ್ಲಿ ಶಕ್ತಿ ಬದಲಾಗುತ್ತದೆ.[ಬದಲಾಯಿಸಿ]
ವಿದ್ಯುಚ್ಛಕ್ತಿಯ ಮೊತ್ತವನ್ನು ಗಿಬ್ಸ್ ಮುಕ್ತ ಶಕ್ತಿ ಪ್ರತಿಕ್ರಿಯೆಯ ಜೊತೆಗೆ ವ್ಯವಸ್ಥೆಯಲ್ಲಿನ ನಷ್ಟಗಳ ಬದಲಾವಣೆಗೆ ಸಮವಾಗುವಷ್ಟು ಸೇರಿಸಲಾಗಿದೆ. ನಷ್ಟಗಳು (ಸಿದ್ದಾಂತದಲ್ಲಿ) ನಿರ್ದಿಷ್ಟವಾಗಿ ಶೋನ್ಯಕ್ಕೆ ಸಮೀಪವಿರಬಹುದು, ಅದರಿಂದ ಗರಿಷ್ಠ ಥರ್ಮೋಡೈನಮಿಕ್ ಸಾಮರ್ಥ್ಯ, ಎಥಾಲ್ಫಿ ಬದಲಾವಣೆಯನ್ನು ಪ್ರತಿಕ್ರಿಯೆಯ ಮಕ್ತ ಶಕ್ತಿಯ ಬದಲಾವಣೆಯಿಂದ ವಿಭಾಗಿಸಿರುವುದಕ್ಕೆ ಸಮನಾಗಿದೆ. ಹಲವು ಪ್ರಕ್ರಿಯೆಗಳಲ್ಲಿ, ಪ್ರತಿಕ್ರಿಯೆಯ ಎಥಾಲ್ಫಿ ಬದಲಾವಣೆಗಿಂತ ವಿದ್ಯುತ್ತಿನ ಪ್ರವೇಶವು ಹೆಚ್ಚಾಗಿದೆ, ಅದ್ದರಿಂದ ಶಕ್ತಿಯು ಉಷ್ಣದ ರೂಪದಲ್ಲಿ ಬಿಡುಗಡೆಗೊಳ್ಳುತ್ತದೆ. ಗರಿಷ್ಠ ಉಷ್ಣಾಂಶದಲ್ಲಿ ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಹಬೆಯೊಳಗೆ ಹೈಡ್ರೋಜನ್ ಮತ್ತು ಆಕ್ಸೀಜನ್ ಪ್ರತಿಯಾದದ್ದು ವಾಸ್ತವ.
ತಾಪವನ್ನು ಸುತ್ತುಮುತ್ತುಲುಗಳಲ್ಲಿ ಹೀರಿಕೊಳ್ಳಲಾಗಿದೆ, ಮತ್ತು ವಿದ್ಯುತ್ತಿನ ಪ್ರವೇಶಕ್ಕಿಂತ ಹೈಡ್ರೋಜನ್ ಉತ್ಪತ್ತಿಮಾಡಿದ ತಾಪಮಾನದ ಮೌಲ್ಯ ಹೆಚ್ಚಾಗಿದೆ.
ಸಂಬಂಧಿತ ತಂತ್ರಗಳು[ಬದಲಾಯಿಸಿ]
ವಿದ್ಯುದ್ವಿಭಜನೆಗೆ ಸಂಬಂಧಿಸಿದ ತಂತ್ರಗಳು ಹೀಗಿವೆ:
- ಜೆಲ್ ವಿದ್ಯುದ್ವಿಭಜನೆ, ಈ ವಿದ್ಯುದ್ವಿಭಜನೆಗೆ ಜೆಲ್ ದಾವಕವನ್ನು ಬಳಸಲಾಗುತ್ತದೆ. ಡಿಎನ್ಎ ಎಳೆಗಳಂತಹ ಪದಾರ್ಥಗಳನ್ನು ಅವುಗಳ ವಿದ್ಯುದಂಶದ ಆಧಾರ ಮೇಲೆ ಪ್ರತ್ಯೇಕಿಸಲು ಇದನ್ನು ಬಳಸುತ್ತಾರೆ.
- ಶ್ರೇಷ್ಠ ವಿದ್ಯುದ್ಧ್ರುವ ಸಾಮರ್ಥ್ಯ ವಿದ್ಯುತ್ತಿನ ಸಾಮರ್ಥ್ಯವನ್ನುಂಟು ಮಾಡಿ ಅದರಿಂದ ಉಪಯುಕ್ತ ಶಕ್ತಿಯನ್ನು ಹೊರತೆಗೆಯುತ್ತದೆ, ಇದರಲ್ಲಿನ ವ್ಯತ್ಯಾಸವನ್ನು ಹೈಡ್ರೋಜನ್ ಇಂಧನ ಕೋಶ ಒಳಗೊಂಡು ವಿದ್ಯುದ್ರಾಸಾಯನಿಕ ಕೋಶಗಳು ಬಳಸಿಕೊಳ್ಳುತ್ತವೆ. ಆದಾಗ್ಯೂ ವಿದ್ಯುದಾವಿಷ್ಟಕಣಗಳ ಹೊಂದಾಣಿಕೆ, ವಿದ್ಯುದ್ಧ್ರುವಗಳು,ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಮೂಲಕ ಸಂಬಂಧಿದಿದಂತೆ, ವಿದ್ಯುದ್ವಿಭಜನೆ ಮತ್ತು ಕಾರ್ಯಕ್ರಿಯೆಯ ವಿದ್ಯುದ್ರಾಸಾಯನಿಕ ಕೋಶಗಳು ಸ್ವಲ್ಪ ಮಟ್ಟಿಗೆ ಭಿನ್ನ. ರಾಸಾಯನಿಕ ಕೋಶಗಳು "ಹಿಮ್ಮುಖವಾಗಿ ವಿದ್ಯುದ್ವಿಭಜನೆ" ಮಾಡುವ ಕಲ್ಪನೆಯ ಮಾದರಿಯನ್ನೇ ಹೊಂದಿರಲಿಲ್ಲ .
ಫ್ಯಾರಡೇಯ ವಿದ್ಯುದ್ವಿಭಜನೆಯ ನಿಯಮಗಳು[ಬದಲಾಯಿಸಿ]
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಮೊದಲನೆ ನಿಯಮ[ಬದಲಾಯಿಸಿ]
1832ರಲ್ಲಿ, ಮೈಕಲ್ ಫ್ಯಾರಡೇ ಪಥದೊಳಗೆ ಕಳುಹಿಸಿದ ವಿದ್ಯುದಾಂಶ ಪ್ರಮಾಣದ ಅನುಪಾತ ಕರಗಿದ ಅಥವಾ ಕರಗುವ ಲವಣದೊಳಗೆ ವಿದ್ಯುತ್ಪ್ರವಾಹವನ್ನು ಹರಿಸುವುದರ ಮೂಲಕ ಮೂಲವಸ್ತುಗಳ ಪ್ರಮಾಣವನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗುತ್ತದೆ ಎಂದು ವರದಿ ಮಾಡಿದರು. ಇದು ವಿದ್ಯುದ್ವಭಜನೆಯ ಮೊದಲನೆ ನಿಯಮದ ಮೂಲತತ್ವವಾಗಿದೆ:
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಎರಡನೆ ನಿಯಮ[ಬದಲಾಯಿಸಿ]
ಫ್ಯಾರಡೇ, ಸರಿಯಾಗಿ ಅಗತ್ಯವಾದ ಭಾಗಾಂಕವನ್ನು ಅನ್ವಯಿಕೆ ಮಾಡಿದಾಗ ಪ್ರತ್ಯೇಕಸಿದ ಮೂಲ ವಸ್ತುಗಳ ಪರಿಣಾಮದ ದ್ರವ್ಯರಾಶಿ ಮೂಲವಸ್ತುಗಳ ಪರಮಾಣುಗಳ ದ್ರವ್ಯರಾಶಿಗಳಿಗೆ ನೇರ ಅನುಪಾತದಲ್ಲಿರುತ್ತವೆ ಎನ್ನುವುದನ್ನು ಕೂಡ ಕಂಡುಹಿಡಿದರು.
ಅದಕ್ಕೆ ಇದು, ಪ್ರತ್ಯೇಕಿಸಿದ ಕಣಗಳ ಭೌತವಸ್ತು ಮೂಲವಸ್ತುಗಳ ಪರಮಾಣುಗಳ ಭಾಗಳಾಗಿವೆ ಎನ್ನುವ ದೃಢವಾದ ಪುರಾವೆಯನ್ನು ಒದಗಿಸುತ್ತದೆ.
ಕೈಗಾರಿಕಾ ಉದ್ಯಮದಲ್ಲಿ ಬಳೆಯುವಿಕೆಗಳು[ಬದಲಾಯಿಸಿ]

- ಅಲ್ಯೂಮಿನಿಯಂ,ಲಿಥಿಯಂ, ಸೋಡಿಯಂ, ಪೋಟ್ಯಾಶಿಯಂ, ಮೆಗ್ನೀಶಿಯಂಗಳ ಉತ್ಪಾದನೆ.
ಕೌಲೊಮೆಟ್ರಿಕ್ ತಂತ್ರಗಳನ್ನು ವಿದ್ಯುದ್ವಿಭಜನೆ ಮಾಡಲು ಬೇಕಾಗುವ ವಿದ್ಯುತ್ ಮೊತ್ತವನ್ನು ಅಳೆದು,ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಸಂದರ್ಭದಲ್ಲಿ ಪರಿವರ್ತಿಸಿದ ಭೌತವಸ್ತುವಿನ ಮೊತ್ತವನ್ನು ಕಂಡುಹಿಡಿಯಲು ಬಳಸಬಹುದು.
- ಕ್ಲೋರಿನ್ ಮತ್ತುಸೋಡಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್ ಉತ್ಪಾದನೆ.
- ಸೋಡಿಯಂ ಕ್ಲೋರೇಟ್ ಮತ್ತು ಪೊಟ್ಯಾಶಿಯಂ ಕ್ಲೋರೇಟ್ ಉತ್ಪಾದನೆ.
- ಟ್ರೈಫ್ಲೋರೊಸಿಟಿಕ್ ಆಮ್ಲೀಯದಂತಹ ಪೆರ್ಫ್ಲೋರಿನೇಟೆಡ್ ಜೈವಿಕ ಸಂಯುಕ್ತಗಳ ಉತ್ಪಾದನೆ.
- ವಿದ್ಯುದ್ವಿಭಾಜಕ ತಾಮ್ರದಿಂದ ಕ್ಯಾಥೋಡ್ಮತ್ತು ಸಂಸ್ಕರಿಸಿದ ಕೀಳು ಗುಣಮಟ್ಟದ ಶುದ್ಧ ತಾಮ್ರದಿಂದ ಅನೋಡ್ ಉತ್ಪಾದನೆ.
ವಿದ್ಯುದ್ವಿಭಜನೆ ಹಲವು ಬೇರೆರೀತಿಯ ಬಳಕೆಗಳನ್ನು ಹೊಂದಿದೆ:
- ವಿದ್ಯುನ್ಲೋಹೋದ್ಧರಣ ಎಂದರೆ,ವಿದ್ಯುದ್ವಿಭಜನೆಯನ್ನು ಬಳಸಿ, ಲೋಹದ ಧಾತುಗಳಿಂದ ಲೋಹಗಳ ಅಪಕರ್ಷಣಮಾಡಿ ಪರಿಶುದ್ಧ ರೂಪದ ಲೋಹವನ್ನು ಪಡೆಯುವುದು, ಈ ವಿಧಾನ. ಉದಾಹರಣೆಗೆ, ಸೋಡಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್ನ ದ್ರವ ರೂಪವು ವಿದ್ಯುದ್ವಿಭಜನೆಯಿಂದ ಸೋಡಿಯಂ ಮತ್ತು ಆಕ್ಸೀಜನ್ ಆಗಿ ಪ್ರತ್ಯೇಕಗೊಂಡಿತು, ಇವೆರಡೂ ಉನ್ನತ ರಾಸಾಯನಿಕ ಬಳಕೆಗಳು.
(ಅದೇ ಸಮಯದಲ್ಲಿ ನೀರು ಉತ್ಪತ್ತಿಯಾಗಿದೆ.)
- ಅನೋಡಿಕರಣ ಎಂದರೆ ವಿದ್ಯುದ್ವಿಭಜನೆಯ ವಿಧಾನ ಇದು ಲೋಹದ ಮೇಲ್ಪದರದ ಸವೆತವನ್ನು ತಡೆಯುವಂತೆ ಮಾಡುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ಈ ವಿಧಾನದಿಂದ ನೀರಿನಲ್ಲಿನ ಆಮ್ಲಜನಕದಿಂದ ಹಡಗುಗಳಿಗೆ ತುಕ್ಕು ಹಿಡಿಯುವುದನ್ನು ತಡೆಗಟ್ಟಿ ಹಡಗುಗಳನ್ನು ತುಕ್ಕು ಹಿಡಿಯುವುದರಿಂದ ರಕ್ಷಿಸಬಹುದು. ಈ ವಿಧಾನವನ್ನು ಅಲಂಕಾರಿಕ ವಸ್ತುಗಳಾ ಮೇಲ್ಪದರಗಳಲ್ಲಿಯೂ ಬಳಸುತ್ತಾರೆ.
- ವಿದ್ಯುತ್ಕೋಶವು ವಿದ್ಯುದ್ವಿಭಜನೆಗೆ ಹಿಮ್ಮುಖ ವಿಧಾನವಾಗಿ ಕೆಲಸ ಮಾಡುತ್ತದೆ. ಹಂಫ್ರಿ ಡೇವಿ ಲಿಥಿಯಂ ವಿದ್ಯುದ್ವಿಭಾಜಕವಾಗಿ ವರ್ತಿಸುತ್ತದೆ ಮತ್ತು ಇದು ವಿದ್ಯುತ್ಶಕ್ತಿಯನ್ನು ಒದಗಿಸುತ್ತದೆ. [ಸೂಕ್ತ ಉಲ್ಲೇಖನ ಬೇಕು]
- ಬಾಹ್ಯಾಕಾಶ ನೌಕೆ ಮತ್ತು ನ್ಯೂಕ್ಲೀಯರ್ ಜಲಾಂತರಗಳಿಗಾಗಿ ಆಮ್ಲಜನಕ ಉತ್ಪತ್ತಿ.
- ಲೋಹಗಳನ್ನು ಬಲಪಡಿಸಲು ಅವುಗಳಿಗೆ ಲೇಪನಮಾಡಲಾಗುತ್ತದೆ ಈ ವಿಧಾನಕ್ಕೆ ವಿದ್ಯುಲ್ಲೇಪನವನ್ನು ಬಳಸಲಾಗುತ್ತದೆ. ಹಲವು ಕೈಗಾರಿಕೆಗಳಲ್ಲಿ ಕಾರ್ಯಾತ್ಮಕ ಅಥವಾ ಅಲಂಕಾರಿಕ ಉದ್ದೇಶಗಳಿಗಾಗಿ,
ವಾಹನಗಳ ದೇಹಾಕೃತಿಗಳಲ್ಲಿ ಮತ್ತು ನಿಕ್ಕಲ್ ಬಿಲ್ಲೆಗಳಲ್ಲಿ ವಿದ್ಯುಲ್ಲೇಪನವನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.
- ಇಂಧನಕ್ಕಾಗಿ ಹೈಡ್ರೋಜನ್ ಉತ್ಪಪಾದನೆ ಮಾಡಲಾಗುತ್ತದೆ,ಇದನ್ನು ಅಗ್ಗದ ವಿದ್ಯುಚ್ಛಕ್ತಿ ಉತ್ಪನ್ನವಾಗಿ ಬಳಸಿಕೊಳ್ಳಲಾಗುತ್ತದೆ.
- ಸಲಕರಣೆಗಳು ಅಥವಾ ಖಾಯಂ ಗುರುತು ಅಥವಾ ಚಿಹ್ನೆಯೊಂದಿನ ಚೂರಿಗಳಂತಹ ಲೋಹದ ಮೇಲ್ಪದರಗಳನ್ನು ವಿದ್ಯುದ್ವಿಭಾಜಕವಾಗಿ ಕೊರೆಯಾಗುತ್ತದೆ.
ಹಳೆಯ ಉಪಕರಣಗಳ ಸಂರಕ್ಷಣೆ ಮತ್ತು ಶುದ್ಧಿಕರಣದಲ್ಲಿಯೂ ಕೂಡ ವಿದ್ಯುದ್ವಿಭಜನೆಯನ್ನು ಬಳಸುತ್ತಾರೆ. ಏಕೆಂದರೆ ಈ ವಿಧಾನವು ಲೋಹದ ಕಣಗಳಿಂದ ಅಲೋಹ ಕಣಗಳನ್ನು ಪ್ರತ್ಯೇಕಗೊಳಿಸುತ್ತದೆ ಮತ್ತು ಇದು ಹಳೆ ಬಿಲ್ಲೆಗಳು ಮತ್ತು ದೊಡ್ದದಾದ ವಸ್ತುಗಳನ್ನು ಕೂಡ ಶುದ್ಧಮಾಡಲು ಅಧಿಕವಾಗಿ ಬಳಸಬಹುದು.
ದ್ರಾವಣ ವಿದ್ಯುದ್ವಿಭಾಜಕದಲ್ಲಿ ಅರೆ-ಪ್ರತಿಕ್ರಿಯೆಗಳ ಪೈಪೂಟಿ[ಬದಲಾಯಿಸಿ]
ನಿಷ್ಕ್ರಿಯ ಪ್ಲಾಟಿನಂ ವಿದ್ಯುದ್ಧ್ರುವಗಳನ್ನು ಹೊಂದಿರುವ ಕೋಶವನ್ನು ಬಳಸಿ, ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಜಲ ದ್ರಾವಕಗಳ ಕೆಲವು ಲವಣಗಳು ಧನ ಅಯಾನುಗಳ ಅಪಕರ್ಷಣಕ್ಕೆ ಪರಿಣಮಿಸುತ್ತವೆ (ಉ.ದಾ.ಲೋಹದ ರಾಶಿ ಸಂಚಯಿಸಲು ಬಿಡುವುದರ ಜೊತೆಗೆ ಉ.ದಾ.ಗಂಧಕ ಲವಣಗಳು) ಮತ್ತು ಋಣ ಅಯಾನುಗಳ ಉತ್ಕರ್ಷಣ (ಉ.ದಾ.ಬ್ರೋಮಿನ್ ಜೊತೆಗೆ ಬ್ರೋಮೈಡ್ ವಿಕಾಸ) ಆದರೂ ಲವಣಗಳ ಕೆಲ ಲೋಹಗಳು (ಉ.ದಾ. ಸೋಡಿಯಂ) ಹೈಡ್ರೋಜನ್ ಕ್ಯಾಥೋಡ್ನಲ್ಲಿ ಉತ್ಪತ್ತಿಯಾಗುತ್ತದೆ ಮತ್ತು ಲವಣಗಳು ಕೆಲ ಋಣ ಅಯಾನುಗಳನ್ನು ಹೊಂದಿವೆ (ಉ.ದಾ.ಸಲ್ಫೆಟ್ (SO42−)) ಆಮ್ಲಜನಕ ಕ್ಯಾಥೋಡ್ನಲ್ಲಿ ಉತ್ಪತ್ತಿಯಾಗುತ್ತದೆ, ಮತ್ತು ಎರಡೂ ಕ್ರಿಯೆಗಳಲ್ಲಿ ಈ ರೀತಿ ಯಾಕೆಂದರೆ ಹೈಡ್ರೋಜನ್ ಉತ್ಪತ್ತಿಸಲು ನೀರು ಕಡಿಮೆಗೊಳಿಸುವುದು ಅಥವಾ ಆಮ್ಲಜನಕ ಉತ್ಪತ್ತಿಸಲು ಉತ್ಕರ್ಷಣ ಮಾಡುವುದು. ಮೂಲತತ್ವದಲ್ಲಿ ವಿದ್ಯುದ್ವಿಜನೀಯ ಕ್ಯಾಥೋಡ್ ಮತ್ತು ಅನೋಡ್ಗಳಲ್ಲಿನ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗಾಗಿ ಶ್ರೇಷ್ಠ ವಿದ್ಯುದ್ಧ್ರುವ ಸಾಮರ್ಥ್ಯದಿಂದ ಪಡೆಯಬಹುದಾದ ಲವಣ ದ್ರಾವಣದ ವಿದ್ಯುದ್ವಿಭಜನೆಗೆ ಬೇಕಾಗುವ ವಿದ್ಯುತ್ ವಿಭವಾಂತರದ ಪ್ರಮಾಣ. ಶ್ರೇಷ್ಠ ವಿದ್ಯುದ್ಧ್ರುವ ಸಾಮರ್ಥ್ಯ ನೇರವಾಗಿ ಗಿಬ್ಸ್ ಮುಕ್ತ ಶಕ್ತಿಗೆ ಸಂಬಂಧಿಸುತ್ತದೆ,ΔG ಇದು ಪ್ರತಿ ವಿದ್ಯುದ್ಧ್ರುವಗಳಲ್ಲಿನ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಹಾಗೂ ವಿದ್ಯುದ್ವಾರದ ಉಲ್ಲೇಖದೊಂದಿಗೆ ವಿದ್ಯುತ್ ಪ್ರವಾಹ ಹರಿಯುತ್ತಿಲ್ಲವೆಂದು ತೋರಿಸುತ್ತದೆ. ಶ್ರೇಷ್ಠ ವಿದ್ಯುದ್ಧ್ರುವ ಸಾಮರ್ಥ್ಯಗಳ ಕೋಷ್ಠಕದಿಂದ ತೆಗೆದುಕೊಂಡಿರುವ ಸಂಗ್ರಹವನ್ನು ಈ ಕೆಳಗೆ ತೋರಿಸಲಾಗಿದೆ.
| ಅರೆ-ಪ್ರತಿಕ್ರಿಯೆ | E° (V) | ಉಲ್ಲೇಖ. |
|---|---|---|
| Na+ + e − |
-2.71 | [೧] |
| Zn2+ + 2e − |
-0.7618 | [೨] |
| 2H+ + 2e − |
≡ 0 | |
| Br2(aq ) + 2e − |
+1.0873 | [೨] |
| O2(g ) + 4H+ + 4e − |
+1.23 | [೧] |
| Cl2(g ) + 2e − |
+1.36 | [೧] |
| S 2O2– 8 + 2e − 4 |
+2.07 | [೧] |
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ರೀತಿಯಲ್ಲಿ ಹೇಳುವುದಾದರೆ, ಈ ಕೋಷ್ಠಕವನ್ನು ಕೆಳಗಿನಂತೆ ವಿವವರಿಸಿ ಹೇಳಲಾಗಿದೆ.
- ಸಮೀಪ ಕೋಷ್ಠದ ಮೇಲ್ಭಾಗದಲ್ಲಿರುವ ಉತ್ಕರ್ಷಣೆಯ ಬಿಲ್ಲೆಗಳನ್ನು(ಆಗಾಗ ಧನ ಅಯಾನು)ಮಾರ್ಪಡಿಸುವುದಕ್ಕಿಂತ ಉಕರ್ಷಣೆಯ ಬಿಲ್ಲೆಗಳನ್ನು ಮತ್ತಷ್ಟು ಕೆಳಗಿಳಿಸುವುದು ಹೆಚ್ಚು ಕಷ್ಟ. ಉದಾಹರಣೆಗೆ ಸೋಡಿಯಂ ಅಯಾನ್ನಿಂದ ಸೋಡಿಯಂ ಲೋಹವಾಗಿ ಮಾರ್ಪಡಿಸುವುದಕ್ಕಿಂತ ಗಂಧಕ ಅಯಾನ್ನಿಂದ ಗಂಧಕ ಲೋಹವಾಗಿ ಮಾರ್ಪಾಡಿಸುವುದು ಹೆಚ್ಚು ಕಷ್ಟ.
- ಕೋಷ್ಠದ ಕೆಳಭಾಗದ ಸಮೀಪದಲ್ಲಿರುವ ಬಿಲ್ಲೆಗಳನ್ನು(ಆಗಾಗ ಋಣ ಅಯಾನು)ಉತ್ಕರ್ಷಣೆ ಮಾಡುವುದಕ್ಕಿಂತ ಬಿಲ್ಲೆಗಳನ್ನು ಮತ್ತಷ್ಟು ಎತ್ತರಕ್ಕೆ ಮಾರ್ಪಾಡಿಸುವುದು ಹೆಚ್ಚು ಕಷ್ಟ.
ಉದಾಹರಣೆಗೆ ಸಲ್ಫೆಟ್ ಅಯಾನುಗಳನ್ನು ಉತ್ಕರ್ಷಿಸುವುದಕ್ಕಿಂತ ಬ್ರೊಮೈಡ್ ಅಯಾನುಗಳನ್ನು ಉತ್ಕರ್ಷಿಸುವುದು ಹೆಚ್ಚು ಕಷ್ಟ.
ನೆರ್ನ್ಸ್ಟ್ ಸಮೀಕರಣ ಬಳಸಿ ಅಯಾನುಗಳ, ಉಷ್ಣತೆಯ ಮತ್ತು ಒಳಗೊಂಡಿರುವ ಎಲೆಕ್ಚ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯ ಒಂದು ನಿರ್ದಿಷ್ಟವಾದ ಸಾಂದ್ರತೆಗೆ ವಿದ್ಯುದ್ಧ್ರುವ ವಿಭವವನ್ನು ಎಣಿಕೆಮಾಡಲು ಸಾಧ್ಯ. ಶುದ್ಧ ನೀರಿಗೆ (pH 7):
- ಅಪಕರ್ಷಣ ಉತ್ಪಾದಿಸುವ ಜಲಜನಕಕ್ಕೆ ವಿದ್ಯುದ್ಧ್ರುವ ವಿಭವ −0.41 V
- ಉತ್ಕರ್ಷಣ ಉತ್ಪಾದಿಸುವ ಅಮ್ಲಜನಕಕ್ಕೆ ವಿದ್ಯುದ್ಧ್ರುವ ವಿಭವ +0.82 V.
IM ಜಿಂಕ್ ಬ್ರೋಮೈಡ್, ZnBr2ಗೆ −0.76 V ಅನ್ನು Zn ಮೆಟಲ್ ಮತ್ತು +1.10 V ಪ್ರಮಾಣದಲ್ಲಿ ಆಕ್ಸಿಡೇಷನ್ ಆದಾಗ ಬ್ರೋಮಿನ್ ಉತ್ಪಾದನೆ ಆಗುತ್ತದೆ ಎಂಬುದು ಹೋಲಿಕೆ ಮಾಡಬಹುದಾದ ಅಂಕೆಗಳಾಗಿವೆ. ಈ ಅಂಕಿಅಂಶಗಳಿಂದ ತಿಳಿದು ಬರುವ ವಿಷಯವೆಂದರೆ ಜಲಜನಕವನ್ನು ಕ್ಯಾಥೋಡ್ನಲ್ಲಿ ಉತ್ಪತ್ತಿ ಮಾಡಬಹುದು ಮತ್ತು ಆಮ್ಲಜನಕವನ್ನು ನೀರನ್ನು ಎಲೆಕ್ಟ್ರೋಲಿಸಿಸ್ ಮಾಡುವ ಮೂಲಕ ಆಯ್ನೋಡ್ನಲ್ಲಿ ಉತ್ಪತ್ತಿ ಮಾಡಬಹುದು. ಇದರಲ್ಲಿ ಪ್ರಾಯೋಗಿಕವಾಗಿ ಜಿಂಕ್ ಲೋಹವನ್ನು ಹಾಕುವ ಮೂಲಕ ಬ್ರೋಮೈಡ್ ಅನ್ನು ಉತ್ಪತ್ತಿ ಮಾಡಬಹುದು.[೩] ವಿವರವೇನೆಂದರೆ ಈ ಲೆಕ್ಕಾದಾರಿತ ಸಾಮರ್ಥ್ಯವು ಥರ್ಮೋಡೈನಾಮಿಕ್ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಕುರಿತಾದುದು ಮಾತ್ರವಾಗಿದೆ. ಸಾಮಾನ್ಯವಾಗಿ ರೂಡಿಯಲ್ಲಿ ಇನ್ನೀತರ ಅಂಶಗಳೂ ಕೂಡ ಸಂಬಂಧಪಡುತ್ತವೆ, ಅವುಗಳಲ್ಲಿ ಕೆಲವು ಪ್ರತಿಕ್ರಿಯೆಗಳ ಹಂತಗಳೂ ಕೂಡ ಒಳಗೊಂಡಿರುತ್ತವೆ. ಈ ಎಲ್ಲ ಅಂಶಗಳನ್ನು ಒಳಗೊಂಡಂತೆ ಹೆಚ್ಚಿನ ಅಂಶಗಳು ಹೆಚ್ಚಿನ ಸತ್ವವನ್ನು ಕಡಿಮೆಗೊಳಿಸುವಿಕೆ ಮತ್ತು ನೀರಿನ ಆಕ್ಸಿಡೀಕರಣ ಅಗತ್ಯವಿದೆ ಎಂಬುದನ್ನು ತಿಳಿಯಲಾಗಿದೆ. ಅಲ್ಲದೆ ಇವು ಹೆಚ್ಚಾಗಿ ಹೆಚ್ಚಿನ ಸತ್ವಹೊಂದಿರುವಂವುಗಳಾಗಿವೆ. ಪ್ರಾಯೋಗಿಕವಾಗಿ ಹೆಚ್ಚಿನ ಸತ್ವ ಒಳಗೊಳ್ಳುವಿಕೆಯು ಹೆಚ್ಚಾಗಿ ಜೀವಕೋಶದ ರಚನೆ ಹಾಗೂ ಎಲೆಕ್ಟ್ರೋಡ್ಗಳ ಗುಣಗಳನ್ನು ಅವಲಂಭಿಸಿರುತ್ತದೆ ಎಂಬುದನ್ನು ಪ್ರಾಯೋಗಿಕವಾಗಿ ತಿಳಿಯಲಾಗಿದೆ.
ತಟಸ್ಥ (pH 7) ಎಲೆಕ್ಟ್ರೋಲೈಸಿಸ್ನ ಸೋಡಿಯಂ ಕ್ಲೊರೈಡ್ಗೆ, ಸೋಡಿಯಂ ಅಯಾನುವಿನ ಅಪಕರ್ಷಣ ಥರ್ಮೊಡೈನಾಮಿಕ್ವಾಗಿ ತುಂಬಾ ಕಷ್ಟ ಮತ್ತು ಹೈಡ್ರೊಕ್ಸೈಡ್ ಅಯಾನುಗಳನ್ನು ದ್ರಾವಣದಲ್ಲಿ ಉಳಿಸಿ ಜಲಜನಕವನ್ನು ಉತ್ಪತ್ತಿಮಾಡಿ ನೀರು ಅಪಕರ್ಷಿಸುತ್ತದೆ. ಕ್ಲೋರಿನ್ಗೆ ಕ್ಲೊರೈಡ್ನ ಉತ್ಕರ್ಷಣಕ್ಕೆ ಅಧಿಕ ವಿಭವವು ಅಮ್ಲಜನಕಕ್ಕೆ ನೀರಿನ ಉತ್ಕರ್ಷಣಕ್ಕೆ ಅಧಿಕ ವಿಭವಕ್ಕಿಂತ ಕಡಿಮೆಯಾಗಿರುವುದರಿಂದ ಆನೋಡ್ನಲ್ಲಿ ನೀರಿನ ಉತ್ಕರ್ಷಣಕ್ಕಿಂತ ಕ್ಲೊರೀನ್ನ ಉತ್ಕರ್ಷಣವನ್ನು ಗಮನಿಸಿದೆ. ಹೈಡ್ರೊಕ್ಸೈಡ್ ಅಯಾನುಗಳು ಮತ್ತು ಕರಗಿರುವ [[ಕ್ಲೋರಿನ್ ಅನಿಲ ಅಷ್ಟೇ ಅಲ್ಲದೆ ಹೈಪೊಕ್ಲೊರಸ್ ಅಮ್ಲ|ಕ್ಲೋರಿನ್ [[ಅನಿಲ ಅಷ್ಟೇ ಅಲ್ಲದೆ ಹೈಪೊಕ್ಲೊರಸ್ ಅಮ್ಲ]]]]ವನ್ನು ರಚಿಸಲು ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ. ಈ ಪ್ರಕ್ರಿಯೆಯಿಂದ ಉಂಟಾದ ನೀರಿನ ದ್ರಾವಣಗಳನ್ನು ಎಲೆಕ್ಟ್ರೊಲೈಜ್ಡ್ ನೀರು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಅದನ್ನು ಮತ್ತು ಸ್ವಚ್ಚಗೊಳಿಸುವ ಪ್ರತಿನಿಧಿಗಳಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ.
ನೀರಿನ ವಿದ್ಯುದ್ವಿಭಜನೆ[ಬದಲಾಯಿಸಿ]
ನೀರಿನ ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಒಂದು ಮುಖ್ಯ ಉಪಯೋಗವೆಂದರೆ ಜಲಜನಕದ ಉತ್ಪಾದನೆ.
- 2 H2O(l) → 2 H2(g) + O2(g); E0 = +1.229 V
ಜಲಜನಕವನ್ನು ದಹನದ ಮೂಲಕ ಅಂತರ್ದಹನ ಯಂತ್ರಗಳ ಅಥವಾ ಜಲಜನಕ ಇಂಧನ ಕೋಶಗಳ ಮೂಲಕ ಎಲೆಕ್ಟ್ರಿಕ್ ಮೋಟಾರುಗಳ ಶಕ್ತಿ ಒದಗಿಸಲು ಇಂಧನವಾಗಿ ಬಳಸಲು ಸಾಧ್ಯ (ಜಲಜನಕ ವಾಹನಗಳು ನೋಡಿ). ಪ್ರಪಂಚದ ಆರ್ಥಿಕ ಸ್ಥಿತಿಗಳನ್ನು ಪ್ರಸ್ತುತದಿಂದ ಶಕ್ತಿಗಾಗಿ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ಮೇಲೆ ಬಹುಮಟ್ಟಿಗೆ ಸಂಪೂರ್ಣ ಅವಲಂಬನೆಯ ಸ್ಥಿತಿಗೆ ವರ್ಗಾಯಿಸಲು ಒಂದು ದಾರಿಯ ಹಾಗೆ ಇದನ್ನು ಸೂಚಿಸಲಾಗಿದೆ (ಜಲಜನಕ ಆರ್ಥಿಕ ಸ್ಥಿತಿ ನೋಡಿ ).
ನೀರಿನ ಶಕ್ತಿ ದಕ್ಷತೆಯ ವಿದ್ಯುದ್ವಿಭಜನೆ ವ್ಯಾಪಕವಾಗಿ ಬದಲಾಗುತ್ತದೆ. ಈ ಸಾಮರ್ಥ್ಯವು ಜಲಜನಕದಲ್ಲೇ ಇರುವ ವಿದ್ಯುತ್ಕಾಂತೀಯ ಶಕ್ತಿಯ ಪ್ರಮಾಣವನ್ನು ತಿಳಿಸುತ್ತದೆ. ವಿದ್ಯುತ್ತಿನ ಶಕ್ತಿಯ ಕೆಲವುಗಳನ್ನು ಉಷ್ಣತೆಗೆ ಮಾರ್ಪಡಿಸಲಾಗಿದೆ, ಅದು ಒಂದು ಅನುಪಯುಕ್ತ ಉಪ ಉತ್ಪನ್ನ. ಕೆಲವವು ವರದಿಗಳು 50% ಮತ್ತು 70%[೧] ರ ನಡುವಿನ ದಕ್ಷತೆಗಳನ್ನು ಉಲ್ಲೇಖಿಸುತ್ತವೆ. ಈ ದಕ್ಷತೆಯು ಜಲಜನಕದ ಕನಿಷ್ಟ ತಾಪನ ಮೌಲ್ಯದ ಮೇಲೆ ಆಧಾರವಾಗಿದೆ. ಜಲಜನಕದ ಕನಿಷ್ಟ ತಾಪನ ಮೌಲ್ಯವು ಜಲಜನಕವನ್ನು ಕಡಿಮೆ ತಾಪಮಾನದಲ್ಲಿ ಕುದಿಸಿದಾಗ ಅಲ್ಲದೆ ಜಲಜನಕ ಆವಿಯಾಗುವ ಕೆಳಹಂತದ ಉಷ್ಣಾಂಶವನ್ನು ಅತ್ಯಂತ ಕಡಿಮೆ ತಾಪಮಾನ ಮೌಲ್ಯವಾಗಿದೆ. ದಕ್ಷತೆಯು ಒಂದು ಹೆಚ್ಚು ಖಚಿತವಾದ ವ್ಯಾಖ್ಯಾನೆಗಿಂತ ಕಡಿಮೆಯಿರುವ ಕಾರಣ, ಇದು ಜಲಜನಕದ ಒಳಗಿನ ಶಕ್ತಿಯ ಒಟ್ಟು ಮೊತ್ತವನ್ನು ಪ್ರತಿನಿಧಿಸುವುದಿಲ್ಲ. ಇತರೆ ವರದಿಗಳು ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಸೈದ್ಧಾಂತಿಕ ಗರಿಷ್ಟ ದಕ್ಷತೆಯು 80% ಮತ್ತು 94%ರ ನಡುವೆ ಇರುವುದಾಗಿ ಉಲ್ಲೇಖಿಸುತ್ತಾರೆ.[೨] Archived 2008-02-16 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ. . ಸೈದ್ಧಾಂತಿಕ ಗರಿಷ್ಟವು ಅಮ್ಲಜನಕ ಮತ್ತು ಜಲಜನಕ ಎರಡರ ಮೂಲಕ ಹೀರಿಕೊಂಡ ಶಕ್ತಿಯ ಒಟ್ಟು ಮೊತ್ತವನ್ನು ಪರಿಗಣಿಸುತ್ತದೆ. ಈ ಮೌಲ್ಯಗಳು ವಿದ್ಯುತ್ತಿನ ಶಕ್ತಿಯನ್ನು ಜಲಜನಕದ ರಾಸಾಯಿನಿಕ ಶಕ್ತಿಗೆ ಪರಿವರ್ತಿಸುವ ದಕ್ಷತೆಗೆ ಮಾತ್ರ ನಿರ್ದೇಸಿಸುತ್ತವೆ. ವಿದ್ಯುಚ್ಛಕ್ತಿಯನ್ನು ಉತ್ಪಾದಿಸುವಾಗ ವ್ಯಯವಾದ ಶಕ್ತಿ ಒಳಗೊಂಡಿಲ್ಲ. ಉದಾಹರಣೆಗೆ, ಪರಮಾಣು ಪ್ರತಿಕ್ರಿಯೆಗಳ ತಾಪವನ್ನು ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಮೂಲಕ ಜಲಜನಕವಾಗಿ ಪರಿವರ್ತಿಸುವ ಒಂದು ಶಕ್ತಿಕೇಂದ್ರವನ್ನು ಪರಿಗಣಿಸುವಾಗ, ಒಟ್ಟು ದಕ್ಷತೆಯು ಹೆಚ್ಚಿನ ಪಕ್ಷ 25% ಮತ್ತು 40%ರ ನಡುವೆಯಾಗಿರುತ್ತದೆ.[೩]
ಸಮೀಪದ ಅವಧಿಯಲ್ಲಿ $5.55 ಮತ್ತು ದೀರ್ಘ ಅವಧಿಯಲ್ಲಿ $2.27ರ ನಡುವೆ ಒಂದು ಕೆಜಿ ಜಲಜನಕವನ್ನು ಗಾಳಿ ಶಕ್ತಿಯ ವಿದ್ಯುದ್ವಿಭನೆಯಿಂದ ಉತ್ಪಾದಿಸಲು ಸಾಧ್ಯ ಎಂದು NREL ಪತ್ತೆ ಹಚ್ಚಿದೆ.[೪]
ಪ್ರಪಂಚದೆಲ್ಲೆಡೆ ಸುಮಾರು ಶೇಕಡ ನಾಲ್ಕರಷ್ಟು ಜಲಜನಕ ಅನಿಲವು ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಮೂಲಕ ಸೃಷ್ಟಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ಸಾಮಾನ್ಯವಾಗಿ ಸ್ಥಳದಲ್ಲೇ ಉಯೋಗಿಸಲಾಗುತ್ತದೆ. ಹಾಬೆರ್ ಪ್ರಕ್ರಿಯೆಯ ಮೂಲಕ ರಾಸಾಯನಿಕ ಗೊಬ್ಬರಕ್ಕೆ ಅಮೋನಿಯಾದ ಸೃಷ್ಟಿಗಾಗಿ, ಮತ್ತು ಹೈಡ್ರೊಕ್ರಾಕಿಂಗ್ ಮೂಲಕ ಸಮೃದ್ಧವಾದ ಪೆಟ್ರೋಲಿಯಂ ಆಕರಗಳನ್ನು ಲಘು ಭಿನ್ನರಾಶಿಗೆ ಪರಿವರ್ತಿಸಲು ಜಲಜನಕವನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.
ಪ್ರಯೋಗ ನಡೆಸುವವರು[ಬದಲಾಯಿಸಿ]
ವಿದ್ಯುದ್ವಿಭಜನೆ ವೈಜ್ಞಾನಿಕ ಪ್ರಥಮಾನ್ವೇಷಕರನ್ನು ಈ ಕೆಳಗೆ ಹೆಸರಿಸಲಾಗಿದೆ:
ಪೌಲ್ ಹೆರೌಲ್ಟ್]]
ವಿದ್ಯುದುತ್ಪನ್ನಕಗಳ ಪ್ರಥಮಾನ್ವೇಷಕರು:
ತೀರ ಇತ್ತೀಚೆಗಷ್ಟೇ, ಫ್ಲೆಯಿಸ್ಕ್ಯಾಮನ್ ಮತ್ತು ಪೊನ್ಸ್ ಅವರ ಪ್ರಸಿದ್ದ ಪ್ರಯೋಗ ಗಡಸು ನೀರಿನ ವಿದ್ಯುದ್ವಿಭಜನೆಯನ್ನು ಪ್ರದರ್ಶಿಸಿದ್ದರು, ಈ ಪ್ರಯೋಗದ ಪರಿಣಾಮದಲ್ಲಿ ಅಸಂಬದ್ಧ ಉಷ್ಣ ಉಂಟಾಗಿ ಶೈತ್ಯದ ಮಿಳನದ ವಿಫಲ ಸಾಧನೆ.
ಇವನ್ನೂ ಗಮನಿಸಿ[ಬದಲಾಯಿಸಿ]
- [[
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಫ್ಯಾರಡೇ ನಿಯಮಗಳು]]
ಆಕರಗಳು[ಬದಲಾಯಿಸಿ]
- ↑ ೧.೦ ೧.೧ ೧.೨ ೧.೩ ಪೀಟರ್ ಆಯ್ಟ್ಕಿನ್ಸ್(1997). ಫಿಸಿಕಲ್ ಕೆಮಿಸ್ಟ್ರಿ , 6ಥ್ ಎಡಿಷನ್ (ಡಬ್ಲ್ಯೂ .ಎಚ್.ಫ್ರೀಮ್ಯಾನ್ ಆಯ್೦ಡ್ ಕಂಪನಿ, ನ್ಯೂಯಾರ್ಕ್).
- ↑ ೨.೦ ೨.೧ ವನ್ಯಾಸೆಕ್,ಪೆಟ್ರ್(2007). "ಎಲ್ಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸೀರೀಸ್" Archived 2017-07-24 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ.,ಇನ್ ಹ್ಯಾಂಡ್ಬುಕ್ ಆಫ್ ಕೆಮಿಸ್ಟ್ರಿ ಆಯ್೦ಡ್ ಫಿಸಿಕ್ಸ್:88th ಎಡಿಷನ್ Archived 2017-07-24 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ. (ಕೆಮಿಕಲ್ ರಬ್ಬರ್ ಕಂಪನಿ).
- ↑ ಎ.ಇ.ವೊಗೆಲ್, ಎ ತೆಕ್ಸ್ಟ್ಬುಕ್ ಆಫ್ ಕ್ವಾಂಟಿಟೇಟಿವ್ ಇನ್ ಆರ್ಗ್ಯಾನಿಕ್ ಅನಾಲೆಸಿಸ್,ಲಾಗ್ಮನ್ಸ್,ಗ್ರೀನ್ ಆಯ್೦ಡ್ ಕೋ
- ↑ Levene, J. (March 2006). "Wind Energy and Production of Hydrogen and Electricity - Opportunities for Renewable Hydrogen - Preprint" (PDF). National Renewable Energy Laboratory. Retrieved 2008-10-20.
{{cite web}}: Unknown parameter|coauthors=ignored (|author=suggested) (help)
- Pages with script errors
- ವೆಬ್ ಆರ್ಕೈವ್ ಟೆಂಪ್ಲೇಟಿನ ವೇಬ್ಯಾಕ್ ಕೊಂಡಿಗಳು
- CS1 errors: unsupported parameter
- Articles with hatnote templates targeting a nonexistent page
- Articles with unsourced statements from March 2009
- Articles with invalid date parameter in template
- Pages using div col with unknown parameters
- Commons link is on Wikidata
- ರಾಸಾಯನಿಕ ವಿಧಾನಗಳು
- ರಾಸಾಯನಿಕ ಲೇಖನಗಳು ಪರಿಣಿತ ಗಮನವನ್ನು ಹರಿಸಬೇಕು
- ವಿದ್ಯುತ್ರಸಾಯನಶಾಸ್ತ್ರ
- ವಿದ್ಯುದ್ವಿಚ್ಛೇದನ
- ಹೈಡ್ರೋಜನ್ ಉತ್ಪತ್ತಿ
- ಕೈಗಾರಿಕಾ ವಿಧಾನಗಳು
- ರಸಾಯನಶಾಸ್ತ್ರ