ಯೂರಿಯಾ
| |||
| |||
| ಹೆಸರುಗಳು | |||
|---|---|---|---|
| ಐಯುಪಿಎಸಿ ಹೆಸರು
ಡೈಮಿನೊಮೆಥನಾಲ್ (ಕಾರ್ಬನಿಕ ಸಂಯುಕ್ತವಾಗಿ), ಕಾರ್ಬೊನಿಲ್ ಡೈಮೈಡು (ಅಕಾರ್ಬನಿಕ ಸಂಯುಕ್ತವಾಗಿ)
| |||
| Other names
ಕಾರ್ಬಮೈಡು, ಕಾರ್ಬೊನಿಲ್ ಡೈಮೈನು, ಡೈಮಿನೊಮೆಥನೋನ್
| |||
| Identifiers | |||
3D model (JSmol)
|
|||
| ChemSpider | |||
| ECHA InfoCard | 100.000.286 | ||
| E number | E927b (glazing agents, ...) | ||
PubChem CID
|
|||
| RTECS number | YR6250000 | ||
| |||
| ಗುಣಗಳು | |||
| ಆಣ್ವಿಕ ಸೂತ್ರ | CH4N2O | ||
| ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ | ೬೦.೦೬ g mol−1 | ||
| Appearance | White solid | ||
| ಸಾಂದ್ರತೆ | 1.32 g/cm3 | ||
| ಕರಗು ಬಿಂದು |
132.7–135 °C | ||
| ಕರಗುವಿಕೆ ನೀರಿನಲ್ಲಿ | 108 g/100 ml (20 °C) 167 g/100 ml (40 °C) 251 g/100 ml (60 °C) 400 g/100 ml (80 °C) 733 g/100 ml (100 °C) | ||
| ಪ್ರತ್ಯಾಮ್ಲತೆ (pKb) | pKBH+ = 0.18[೧] | ||
| ರಚನೆ | |||
| ದ್ವಿಧ್ರುವ ಚಲನೆ | 4.56 D | ||
| Hazards | |||
| ಚಿಮ್ಮು ಬಿಂದು (ಫ್ಲಾಶ್ ಪಾಯಿಂಟ್) |
|||
| ಸಂಬಂಧಿತ ಸಂಯುಕ್ತಗಳು | |||
Related
|
|||
Related compounds
|
|||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). > | |||
| Infobox references | |||
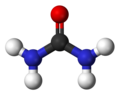
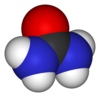
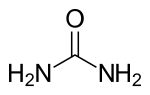
ಯೂರಿಯಾ ಅಥವಾ ‘ಕಾರ್ಬಮೈಡ್’ ಎಂಬುದು (NH2)2CO ರಾಸಾಯನಿಕ ಸೂತ್ರವನ್ನು ಹೊಂದಿರುವ ಕಾರ್ಬನಿಕ ಸಂಯುಕ್ತವಾಗಿದೆ. ಈ ಅಣು ಕಾರ್ಬನಿಲ್ (-CO-) ಕ್ರಿಯಾತ್ಮಕ ಗುಂಪು ಗಳಿಂದ ಬಂಧಿಸಲ್ಪಟ್ಟಿರುವ ಎರಡು ಅಮೀನ್ (-NH2) ಶೇಷಗಳನ್ನು ಹೊಂದಿದೆ.
ಯೂರಿಯಾ ಪ್ರಾಣಿಗಳಲ್ಲಿರುವ ಸಾರಜನಕ ಸಂಯುಕ್ತಗಳ ಮತ್ತು ಸಸ್ತನಿಗಳ ಮೂತ್ರದಲ್ಲಿರುವ ಪ್ರಮುಖ ಸಾರಜನಕದ ಚಯಾಪಚಯ ಕ್ರಿಯೆಯಲ್ಲಿ ಪ್ರಮುಖ ಪಾತ್ರವನ್ನು ನಿರ್ವಹಿಸುತ್ತದೆ . ಘನರೂಪದಲ್ಲಿದ್ದು ,ವರ್ಣರಹಿತ, ವಾಸನೆರಹಿತವಾಗಿರುವ ( ಆದರೂ ಗಾಳಿಯಲ್ಲಿ ನೀರಿನ ಆವಿಯಾಗುವುದೂ ಸೇರಿದಂತೆ ನೀರಿನಲ್ಲಿ ಅಮೋನಿಯ ತೀವ್ರವಾದ ವಾಸನೆ ಹೊಂದಿರುತ್ತದೆ.)ಅಮ್ಲೀಯವು ಅಲ್ಲದ ಕ್ಷಾರೀಯವು ಅಲ್ಲದ , ನೀರಿನಲ್ಲಿ ಚೆನ್ನಾಗಿ ಕರಗಬಲ್ಲ ಹಾಗು ತುಲನಾತ್ಮಕವಾಗಿ ವಿಷಮಯವಲ್ಲದ ಯೂರಿಯಾವನ್ನು ಅನುಕೂಲಕರವಾದ ಸಾರಜನಕ ಮೂಲವಾಗಿ ಗೊಬ್ಬರಗಳಲ್ಲಿ ಹೆಚ್ಚು ಬಳಸಲಾಗುತ್ತದೆ. ಅಷ್ಟೇ ಅಲ್ಲದೆ ಯೂರಿಯಾ ರಾಸಾಯನಿಕ ಉದ್ಯಮಗಳಿಗೆ ಅತಿ ಮುಖ್ಯವಾದ ಕಚ್ಚಾ ವಸ್ತುವಾಗಿದೆ. 1828 ರಲ್ಲಿ ಫ್ರೆಡ್ರಿಕ್ ವೊಲರ್ ನ ಕಾರ್ಬನಿಕ ಸಂಯುಕ್ತಗಳ ಸಂಶ್ಲೇಷಣೆಯ ಅಕಾರ್ಬನಿಕ ಪೂರ್ವವರ್ತಿ ರಾಸಾಯನಶಾಸ್ತ್ರದ ಅಭಿವೃದ್ದಿಯ ಪ್ರಮುಖ ಮೈಲಿಗಲ್ಲಾಗಿದೆ.
ಯೂರಿಯಾ ಮತ್ತು ಕಾರ್ಬಮೈಡ್ ಎಂಬ ಪದವನ್ನು ಎರಡು ಕಾರ್ಬನಿಕ ಅಮೀನ್ ಶೇಷಗಳನ್ನು ಹೊಂದಿರುವಂತಹ ಕಾರ್ಬೊನಿಲ್ ಗುಂಪು ಎಂದು ಕರೆಯಲಾಗುವ RR'N-CO-NRR' ಕ್ರಿಯಾತ್ಮಕ ಗುಂಪುಗಳೊಡನೆ ಹಂಚಿಕೊಳ್ಳುವ ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳ ವರ್ಗಗಳಿಗೂ ಬಳಸಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ ಕಾರ್ಬಮೈಡ್ ಪೆರಾಕ್ಸೈಡ್ , ಅಲಾನ್ ಟಾಯ್ನ್ , ಹೈಡನ್ ಟಾಯ್ನ್ ಗಳನ್ನು ಒಳಗೊಂಡಿದೆ. ಯೂರಿಯಾ ಬೈಯೂರೆಟ್ಸ್ ನ ಜೊತೆ ಅತ್ಯಂತ ನಿಕಟವಾಗಿದೆ. ಅಲ್ಲದೇ ಅಮೈಡ್ಸ್ , ಕಾರ್ಬಮೇಟ್ಸ್ , ಡೀಮೈಡ್ಸ್, ಕಾರ್ಬೊಡಿಮೈಡ್ಸ, ತಿಯೋಕಾರ್ಬಮೈಡ್ಸ್ ನ ರಚನೆಗಳಿಗೆ ಸಂಬಂಧಿಸಿದೆ.
ಇತಿಹಾಸ[ಬದಲಾಯಿಸಿ]
ಯೂರಿಯಾವನ್ನು ಮೊದಲು ಹಿಲೈರ್ ರೊಯೆಲ್ ಎಂಬ ಫ್ರೆಂಚ್ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞ 1773ರಲ್ಲಿ ಮೂತ್ರದಲ್ಲಿ ಕಂಡುಹಿಡಿದನು. ಫೆಡ್ರಿಕ್ ವೊಲರ್ ಎಂಬ ಜರ್ಮನ್ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞ 1828ರಲ್ಲಿ ಸಿಲ್ವರ್ ಐಸೊಸೈನೆಟ್ ಅನ್ನು ಅಮೋನಿಯಮ್ ಕ್ಲೋರೈಡ್ ನ ಜೊತೆ ಸೇರಿಸಿ ಅಮೋನಿಯಮ್ ಸೈನೇಟ್ ತಯಾರಿಸುವ ವಿಫಲ ಪ್ರಯತ್ನದಲ್ಲಿ ಯೂರಿಯಾವನ್ನು ಪಡೆದುಕೊಂಡನು.[೨]
- AgNCO + NH4Cl → (NH2)2CO + AgCl
ಸಜೀವ ಜೀವಿಗಳ ಪಾತ್ರವಿಲ್ಲದೆಯೇ ಇದೇ ಮೊದಲನೆ ಬಾರಿಗೆ ಕಾರ್ಬನಿಕ ಸಂಯುಕ್ತ ಕಾರ್ಬನಿಕ ಅಲ್ಲದ ವಸ್ತುಗಳಿಂದ ಸಂಶ್ಲೇಷಿಸಲ್ಪಟ್ಟಿದೆ. ಈ ಪ್ರಯೋಗದ ಖಚಿತವಾದ ಫಲಿತಾಂಶ ಜೀವತತ್ವವಾದದ ಮೇಲೆ ಅಪನಂಬಿಕೆಯನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ: ಸಜೀವಿಗಳ ರಾಸಾಯನಿಕ ಸಿದ್ಧಾಂತವು ನಿರ್ಜೀವಿಗಳ ವಿಷಯದಲ್ಲಿ ಸಂಪೂರ್ಣವಾಗಿ ಭಿನ್ನವಾಗಿದೆ. ಕಾರ್ಬನಿಕ ರಾಸಾಯನಶಾಸ್ತ್ರದ ಅಭಿವೃದ್ಧಿಗೆ ಈ ಒಳನೋಟ ಬಹು ಮುಖ್ಯವಾಗಿದೆ. ವೊಲರ್ ನ ಸಂಶೋಧನೆ ತಕ್ಷಣವೇ ಅವನನ್ನು ಬರ್ಜಿಲಿಯಸ್ ನ ಮೇಲೆ ವಿಜಯ ಸಾಧಿಸಿದೆನೆಂದು ಬರೆಯಲು ಪ್ರಚೋದಿಸಿತು: "ಮನುಷ್ಯರ ಅಥವಾ ನಾಯಿಯ ಮೂತ್ರ ಪಿಂಡವನ್ನು ಉಪಯೋಗಿಸದೆ ನಾನು ಯೂರಿಯಾ ತಯಾರಿಸಬಲ್ಲೆನೆಂದು ನಾನು ನಿನಗೆ ಖಚಿತವಾಗಿ ಹೇಳಬೇಕು". ಅಮೋನಿಯಮ್ ಸೈನೇಟ್ ಯೂರಿಯಾವಾಗಿದೆ." ಈ ಸಂಶೋಧನೆಗಾಗಿ ವೊಲರ್ ನನ್ನು ಹಲವರು ಕಾರ್ಬನಿಕ್ ರಾಸಾಯನಶಾಸ್ತ್ರದ ಪಿತಾಮಹನೆಂದು ಪರಿಗಣಿಸಿದರು.
ಶರೀರ ವಿಜ್ಞಾನ[ಬದಲಾಯಿಸಿ]
ಯೂರಿಯಾವು ಯೂರಿಯಾಚಕ್ರದ ಭಾಗವಾದ ಅನೇಕ ಜೀವಿಗಳ ದೇಹದಲ್ಲಿ ಹಾಗು ಅಮಿನೊಆಮ್ಲಕ್ಕೆ ಆಮ್ಲಜನಕ ಸೇರಿಸಿ ಅಥವಾ ಅಮೋನಿಯ ದಿಂದಲೂ ಸಹ ಸಂಯೋಜಿಸಲ್ಪಟ್ಟಿರುತ್ತದೆ . ಈ ಚಕ್ರದಲ್ಲಿ ಅಮಿನೊ ಗುಂಪುಗಳನ್ನು ಅಮೋನಿಯ ರಚಿಸಿದೆ, ಹಾಗು L-ಅರ್ನಿತಿನ್ ಸಿಟ್ರುಲಿನ್ ,L-ಅರ್ಜಿನ್ ನಿನೊಸೊಯೇಟ್ ಮತ್ತು L-ಅರ್ಜಿನೈನ್ ಮಧ್ಯಂತರವಾದಾಗ L-ಆಸ್ಪರ್ಟೆಟ್ ಯೂರಿಯಾವಾಗಿ ಬದಲಾಗುತ್ತದೆ. ಯೂರಿಯಾ ಉತ್ಪಾದನೆಯು ಲಿವರ್ನಲ್ಲಿ ಉಂಟಾಗುತ್ತದೆ, ಹಾಗು N-ಅಸಿಟೈಲ್ ಗ್ಲುಟ್ ಮೆಟ್ನಿಂದ ನಿಯಂತ್ರಿಸಲ್ಪಡುತ್ತದೆ . ಯೂರಿಯಾ ರಕ್ತದಲ್ಲಿ ಬೆರೆತುಹೋಗಿದೆ. (ಈ ಉಲ್ಲೇಖನ ಮಟ್ಟ ದಲ್ಲಿ of 2.5 to 7.5 mmol/liter)ಹಾಗು ಇದು ಮೂತ್ರದ ಒಂದು ಅಂಶದಂತೆ ಮೂತ್ರಪಿಂಡದಿಂದ ಹೊರಹಾಕಲ್ಪಡುತ್ತದೆ. ಇದರ ಜೊತೆಯಲ್ಲಿ , ಸ್ವಲ್ಪ ಪ್ರಮಾಣದ ಯೂರಿಯಾ ( ಉಪ್ಪು ಮತ್ತು ನೀರಿನ ಜೊತೆಯಲ್ಲಿ ) ಬೆವರಿನ ಹನಿಗಳ ಮೂಲಕ ಹೊರಹಾಕಲ್ಪಡುತ್ತದೆ .
|
| |
|
| |
ಜೀರ್ಣಿಸಿಕೊಳ್ಳಲಾಗದಂತಹ ಆಹಾರಗಳಿಂದ ಪಡೆಯುವಂತಹ ಅಮಿನೊ ಆಮ್ಲವನ್ನು ಪ್ರೋಟೀನ್ ಮತ್ತು ಇತರ ಜೈವಿಕ ವಸ್ತುಗಳನ್ನು ಸಂಶ್ಲೇಷಿಸಲು ಬಳಸದ ಕಾರಣ ಅದನ್ನು ದೇಹವು ಆಕ್ಸಿಡೀಕರಿಸಿ ಯೂರಿಯ ಮತ್ತು ಇಂಗಾಲದ ಡೈ ಆಕ್ಸೈಡ್ ಅನ್ನು ಶಕ್ತಿಯ ಪರ್ಯಾಯ ರೂಪವಾಗಿಸುತ್ತವೆ. [೩] ಆಕ್ಸಿಡೀಕರಣದ ಪ್ರತಿಕ್ರಿಯಾಸರಣಿಯು ಟ್ರಾನ್ಸ್ ಮೈನ್ಸ್ ನಿಂದ ಅಮಿನೊ ಗುಂಪನ್ನು ತೆಗೆದುಹಾಕುವ ಮೂಲಕ ಪ್ರಾರಂಭವಾಗುತ್ತದೆ,ಆಗ ಅಮಿನೊ ಗುಂಪು ಯೂರಿಯಾಚಕ್ರಕ್ಕೆ ಹೋಗಿ ಬೀಳುತ್ತದೆ.
ಅಮೋನಿಯ (NH3) ಸಾರಜನಕಯುಕ್ತ ಸಂಯುಕ್ತಗಳ ಚಯಾಪಚಯ ಕ್ರಿಯೆಯ ಮತ್ತೊಂದು ಸಾಮಾನ್ಯ ಉತ್ಪನ್ನವಾಗಿದೆ. ಅಮೋನಿಯ ಪರಮಾಣಗಳು ಯೂರಿಯಾಗಳಿಗಿಂತ ಗಾತ್ರದಲ್ಲಿ ಸಣ್ಣದಾಗಿರುತ್ತವೆ; ಅಲ್ಲದೇ ಹೆಚ್ಚು ಕರಗಬಲ್ಲವು ಮತ್ತು ಸರಾಗವಾಗಿ ಚಲಿಸಬಲ್ಲವು. ಸಂಚಯಿಸಲು ಅವಕಾಶ ನೀಡಿದಲ್ಲಿ ಅಮೋನೀಯ ಜೀವಕೋಶಗಳಲ್ಲಿ ವಿಷದ ಮಟ್ಟದವರೆಗೆ pH ಪ್ರಮಾಣವನ್ನು ಹೆಚ್ಚಿಸಿರುತ್ತಿತ್ತು. ಈ ಸಂಶ್ಲೇಷಣೆಯು ಮೂಲ ಶಕ್ತಿಯನ್ನು ಒಳಗೊಂಡಿದ್ದರೂ ಕೂಡ ಹಲವು ಜೀವಿಗಳು ಅಮೋನಿಯವನ್ನು ಯೂರಿಯಾವಾಗಿ ಬದಲಾಯಿಸುತ್ತವೆ. ವಾಸ್ತವವಾಗಿ ಅಮ್ಲೀಯವೂ ಅಲ್ಲದ ಪ್ರತ್ಯಾಮ್ಲೀಯವೂ ಅಲ್ಲದ ತಟಸ್ಥ ಸ್ಥಿಯಲ್ಲಿದ್ದು , ನೀರಿನಲ್ಲಿ ಚೆನ್ನಾಗಿ ಕರಗಬಲ್ಲ ಯೂರಿಯಾ ದೇಹದಲ್ಲಿರುವಂತಹ ಸಾರಜನಕವನ್ನು ಸಾಗಿಸುವಂತಹ ಹಾಗು ಹೆಚ್ಚಾಗಿರುವ ಸಾರಜನಕವನ್ನು ದೇಹದಿಂದ ಹೊರಹಾಕುವಂತಹ ಉತ್ತಮ ಸಾಧನವಾಗಿದೆ.
ನೀರಿನ ಪರಮಾಣುಗಳು ಅಮೋನಿಯ ಮತ್ತು ಕಾರ್ಬೊನೆಟ್ ಅನಿಯನ್ಅನ್ನು ಉತ್ಪಾದಿಸುವುದರಿಂದ ನೀರಿನಲ್ಲಿ ಆಮೀನ್ ಗುಂಪು ನಿಧಾನವಾಗಿ ಸ್ಥಳಾಂತರಣಕ್ಕೆ ಒಳಪಡುತ್ತದೆ. ಈ ಕಾರಣದಿಂದ ಕೆಟ್ಟುಹೋಗಿರುವ ಹಳೆಯ ಮೂತ್ರ ತಾಜಾ ಮೂತ್ರಕ್ಕಿಂತ ಹೆಚ್ಚು ದುರ್ವಾಸನೆ ಹೊಂದಿರುತ್ತದೆ .
ಮಾನವರಲ್ಲಿ[ಬದಲಾಯಿಸಿ]
ಮೂತ್ರಪಿಂಡಗಳ ಮೂಲಕ ಯೂರಿಯಾವನ್ನು ನಿರ್ವಹಣೆಮಾಡುವುದು ಮಾನವನ ಚಯಾಪಚಯ ಕ್ರಿಯೆಯ ಒಂದು ಪ್ರಮುಖ ಅಂಶವಾಗಿದೆ. ನಿರುಪಯುಕ್ತ ಸಾರಜನಕವನ್ನು ಸಾಗಿಸುವುದರ ಜೊತೆಗೆ ಯೂರಿಯಾ ನೆಫ್ರೊನ್ ಗಳ ವಿರುದ್ಧ ವಿದ್ಯುತ್ ವಿನಿಮಯ ವ್ಯವಸ್ಥೆಯಲ್ಲಿಯು ಪ್ರಮುಖ ಪಾತ್ರವನ್ನು ನಿರ್ವಹಿಸುತ್ತದೆ. ಇದು ನೀರನ್ನು ಹಾಗು ಮೂತ್ರದಿಂದ ಹೊರಹಾಕಲ್ಪಟ್ಟ ಅಯಾನಗಳನ್ನು ಪುನಃ ಹೀರಿಕೊಳ್ಳಲು ಅವಕಾಶವನ್ನು ನೀಡುತ್ತದೆ. ಯೂರಿಯಾ ನೆಫ್ರಾನ್ ಗಳ ಆಂತರಿಕ ಮಜ್ಜೆಯ ಸಂಗ್ರಹಣಾ ನಾಳದಲ್ಲಿ ಹೀರಿಕೊಳ್ಳುತ್ತದೆ, ಈ ರೀತಿಯಾಗಿ ಮಜ್ಜೆಯ ಇಂಟರ್ಸ್ಟಿಟಿಯಂ ನ ಆಸ್ಮೊಲಾರಿಟಿಯನ್ನು ಹೆಚ್ಚಿಸುತ್ತದೆ. ಇದು ಹೆನ್ಲೆ ಕುಣಿಕೆಯ ಸಣ್ಣದಾಗಿ ಏರಿದ ಅಂಗಾಂಗವನ್ನು ಸುತ್ತುವರೆಯುವುದರ ಜೊತೆಗೆ ನೀರಿನ ಹೀರಿಕೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ. ಯೂರಿಯಾ ಸಾಗಿಸುವ ಸಾಧನ2 ರ ಕಾರ್ಯದಿಂದ ಕೆಲವು ಪುನಃ ಹೀರಿಕೊಳ್ಳಲ್ಪಟ್ಟಂತಹ ಯೂರಿಯಾ ಅಂತಿಮವಾಗಿ ಅಂಗಗಳ ತೆಳುವಾದ ಹಿಮ್ಮುಕ ಕೊಳವೆಗೆ ಶೇಖರಿಸಲ್ಪಟ್ಟ ನಾಳಗಳಿಂದ ಹಾಗು ಹೊರಹಾಕಲ್ಪಟ್ಟ ಮೂತ್ರದ ಮೂಲಕ ಹಿಂದಕ್ಕೆ ಹರಿಯಲ್ಪಡುತ್ತದೆ.
ಮೂತ್ರವರ್ಧಕ ಹಾರ್ಮೋನ್ ಗಳಿಂದ ನಿಯಂತ್ರಿಸಲ್ಪಡುವಂತಹ ಈ ಯಾಂತ್ರಿಕ ವ್ಯವಸ್ಥೆ ದೇಹಕ್ಕೆ ಹೈಪರೊಸೊಮೊಟಿಕ್ ಮೂತ್ರವನ್ನು ಉತ್ಪಾದಿಸಲು ಅವಕಾಶ ನೀಡುತ್ತದೆ. ಇದು ರಕ್ತ ಪ್ಲಾಸ್ಮ ಗಿಂತ ವಿಭಜಿಸಲ್ಪಟ್ಟಂತಹ ವಸ್ತುಗಳ ಹೆಚ್ಚು ಸಾಂದ್ರೀಕರಣ ಒಳಗೊಂಡಿರುತ್ತದೆ. ಈ ಯಾಂತ್ರಿಕ ವ್ಯವಸ್ಥೆ ರಕ್ತದ ಒತ್ತಡವನ್ನು ಹಾಗು ರಕ್ತ ಪ್ಲಾಸ್ಮದಲ್ಲಿ ಸೋಡಿಯಂ ಅಯಾನಿನ ಸರಿಯಾದ ಸಾಂದ್ರೀಕರಣವನ್ನು ನಿರ್ವಹಿಸಲು ಬೇಕಾದ ನೀರಿನ ಕೊರತೆಯನ್ನು ತಡೆಗಟ್ಟಲು ಬಹುಮುಖ್ಯವಾಗಿದೆ.
ಇತರ ಜಾತಿ(ಸಜೀವಿಗಳ ವರ್ಗೀಕರಣದಲ್ಲಿ ಸಂತಾನೋತ್ಪತ್ತಿ ಸಾಧ್ಯವಿರುವ ಗುಂಪು)ಗಳಲ್ಲಿ[ಬದಲಾಯಿಸಿ]
ನೀರಿನಲ್ಲಿ ಇರುವಂತಹ ಜೀವಿಗಳು ವಿಷಯುಕ್ತ ಅಮೋನಿಯವನ್ನು ಯೂರಿಯಾವಾಗಿ ಅಥವಾ ಮೂತ್ರಾ ಮ್ಲವಾಗಿ ಬದಲಾಯಿಸುತ್ತವೆ. ಆಗ ಜಲಜೀವಿ ವ್ಯವಸ್ಥೆಯ ಸಾಮಾನ್ಯ ಭಾಗವಾಗಿರುವ ಉಪಯುಕ್ತವಲ್ಲದ ಸಾರಜನಕವೇ ಅಮೋನಿಯವಾಗುತ್ತದೆ. ಯೂರಿಯಾವು ಸಸ್ತನಿಗಳಮೂತ್ರದಲ್ಲಿ ಉಭಯಚರಜೀವಿಗಳಲ್ಲಿ ಹಾಗು ಕೆಲವು ಮೀನುಗಳಲ್ಲಿ ಸಿಗುತ್ತದೆ ಪಕ್ಷಿಗಳು ಮತ್ತು ಸರಟವರ್ಗದ (ಸಮುದ್ರ ಮೀನುಗಳ ವರ್ಗ)ಸರೀಸೃಪಗಳು ವಿಭಿನ್ನವಾದ ಸಾರಜನಕ ಚಯಾಪಚಯ ಕ್ರಿಯೆಯನ್ನು ಹೊಂದಿವೆ. ಇದು ಕಡಿಮೆ ಪ್ರಮಾಣದ ನೀರನ್ನು ತೆಗೆದುಕೊಂಡು ಸಾರಜನಕವನ್ನು ಮೂತ್ರ ಆಮ್ಲದ ರೂಪದಲ್ಲಿ ಹೊರಹಾಕಲ್ಪಡುವಂತೆ ಮಾಡುತ್ತದೆ . ಉಭಯಚರ ಜೀವಿಗಳು ಅಮೋನಿಯವನ್ನು ಹೊರಹಾಕುತ್ತವೆ, ಆದರೆ ರೂಪಾಂತರದ ಸಂದರ್ಭದಲ್ಲಿ ಮೂತ್ರ ಉತ್ಪಾದನೆಯಾಗಿ ಬದಲಾಗುತ್ತವೆ, ಎಂಬುದು ಗಮನಿಸಬೇಕಾದ ಅಂಶವಾಗಿದೆ. ಮೇಲೆ ಮಾಡಿರುವಂತಹ ಸಾಮಾನ್ಯೀಕರಣವನ್ನು ಹೊರತುಪಡಿಸಿ ಯೂರಿಯಾ ಪ್ರತಿಕ್ರಿಯಾಸರಣಿ ಕೇವಲ ಸಸ್ತನಿಗಳಲ್ಲಿ ಕಾಣುತ್ತದಲ್ಲದೇ ಉಭಯಚರಜೀವಿಗಳಲ್ಲಿ ಮಾತ್ರವಲ್ಲದೇ ಅನೇಕ ಇತರ ಜೀವಿಗಳಲ್ಲಿ ದೊರೆಯುತ್ತದೆ. ಉದಾಹರಣೆ: ಪಕ್ಷಿಗಳಲ್ಲಿ, ಅಕಶೇರುಕಗಳಲ್ಲಿ , ಕೀಟಗಳಲ್ಲಿ , ಸಸ್ಯಗಳಲ್ಲಿ , ಕ್ವಿಣಗಳಲ್ಲಿ , ಶೀಲಿಂದ್ರಗಳಲ್ಲಿ ಹಾಗು ಸೂಕ್ಷ್ಮಾಣು ಜೀವಿಗಳಲ್ಲೂ ಕೂಡ ಇರುತ್ತದೆ. . [ಸೂಕ್ತ ಉಲ್ಲೇಖನ ಬೇಕು]
ಬಳಕೆಗಳು (ಉಪಯೋಗಗಳು)[ಬದಲಾಯಿಸಿ]
ಕೃಷಿ[ಬದಲಾಯಿಸಿ]
ಪ್ರಂಪಚದ ಉತ್ಪಾದನೆಯ 90% ರಷ್ಟು ಯೂರಿಯಾವನ್ನು ಸಾರಜನಕ ಬಿಡುಗಡೆ ಮಾಡುವ ಗೊಬ್ಬರದಂತೆ ಉಪಯೋಗಿಸಲು ಬಳಸಲಾಗುತ್ತದೆ . ಸಾಮಾನ್ಯ ಬಳಕೆಯ ಎಲ್ಲಾ ಘನರೂಪದ ಸಾರಜನಕಯುಕ್ತ ಗೊಬ್ಬರಗಳಲ್ಲಿ ಯೂರಿಯಾವು ಅತ್ಯಂತ ಹೆಚ್ಚು ಸಾರಜನಕದ ಘಟಕವನ್ನು ಹೊಂದಿರುತ್ತದೆ (46.7%). ಆದ್ದರಿಂದ , ಇದು ಸಾರಜನಕ ಪೌಷ್ಟಿಕದ ಪ್ರತಿ ಘಟಕದ ಸಾಗಾಣೆಗೆ ಅತ್ಯಂತ ಕಡಿಮೆ ಬೆಲೆಯನ್ನು ಹೊಂದಿದೆ.
ಮಣ್ಣಿನಲ್ಲಿ ಇದು ನೀರಿನ ನೆರವಿನಿಂದ ಅಮೋನಿಯ ಮತ್ತು ಇಂಗಾಲದ ಡೈ ಆಕ್ಸೈಡ್ ಅನ್ನು ವಿಭಜಿಸುತ್ತದೆ. ಅಮೋನಿಯಯವು ಮಣ್ಣಿನಲ್ಲಿ ಬ್ಯಾಕ್ಟೀರಿಯಾಗಳಿಂದ ನೈಟ್ರೀಕ್ ಆಮ್ಲಗಳಿಗಾಗಿ ಆಕ್ಸಿಡೀಕರಿಸಲ್ಪಡುತ್ತದೆ. ಇದನ್ನು ಸಸ್ಯಗಳು ಹೀರಿಕೊಳ್ಳುತವೆ. ಯೂರಿಯಾ ಬಹುಘಟಕಗಳ ಹಲವು ಗಟ್ಟಿಯಾದ ಗೊಬ್ಬರದ ಸೂತ್ರರೂಪಗಳಲ್ಲಿ ಕೂಡ ಬಳಸಲಾಗುತ್ತದೆ. ಯೂರಿಯಾಾ ನೀರಿನಲ್ಲಿ ಚೆನ್ನಾಗಿ ಕರಗಬಲ್ಲದು; ಆದ್ದರಿಂದ ಇದು ಗೊಬ್ಬರಗಳ ದ್ರಾವಣದಲ್ಲಿ(ಅಮೋನಿಯಮ್ ನೈಟ್ರೇಟ್:UAN ಜೊತೆಯಲ್ಲಿ ) ಬಳಸಲು ಕೂಡ ಸೂಕ್ತವಾಗಿದೆ. ಉದಾಹರಣೆಗೆ ಗಿಡದ ಎಲೆಗಳಿಗೆ ಒದಗಿಸುವ ಮೇವು ಆಗಿರುತ್ತದೆ. ಗೊಬ್ಬರಗಳ ಉಪಯೋಗ, ಯಾಂತ್ರಿಕ ಬಳಕೆಗಳಿಗೆ ಲಾಭವಾಗುವಂತಹ ಸಂಕುಚಿತ ಸೂಕ್ಷ್ಮ ಭಾಗಗಳ ವಿಭಜನೆಯನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಇಲ್ಲಿ ಪ್ರಿಲ್ ಗಳನ್ನು ಸಣ್ಣ ಕಣಗಳು ಬಯಸುತ್ತವೆ .
ಸಂಶ್ಲೇಷಣ ಯೂರಿಯಾದ ಸಾಮಾನ್ಯ ಅಶುದ್ಧತೆ ಬೈಯುರೆಟ್ ಆಗಿದ್ದು, ಇದು ಸಸ್ಯಗಳ ಬೆಳವಣಿಗೆಯನ್ನು ಕುಠಿತಗೊಳಿಸುತ್ತದೆ.
ಯೂರಿಯಾವನ್ನು ಸಾಮಾನ್ಯವಾಗಿ 40 ರಿಂದ 300 kg/ha ಪ್ರಮಾಣದ ವರೆಗು ಹರಡಲಾಗುತ್ತದೆ.ಈ ಪ್ರಮಾಣಗಲಲ್ಲಿ ವ್ಯತ್ಯಾಸವಿರುತ್ತದೆ. ಪ್ರತ್ಯೇಕಿಸಲ್ಪಡುವ ಕಾರಣ ಸಣ್ಣ ಬಳಕೆಗೆಳು ಕಡಿಮೆ ನಷ್ಟವನ್ನು ಅನುಭವಿಸುತ್ತವೆ. ಬೇಸಿಗೆ ಕಾಲದಲ್ಲಿ ಸ್ವಲ್ಪ ಸಮಯ ಮೊದಲಷ್ಟೇ ಯೂರಿಯಾವನ್ನು ಹರಡಲಾಗುತ್ತದೆ, ಅಥವಾ ಬಾಷ್ಪೀಕರಣದಿಂದ ಉಂಟಾಗುವ ಹಾನಿಯನ್ನು ತಡೆಗಟ್ಟಲು ಮಳೆಯ ಸಂದರ್ಭದಲ್ಲಿ ಹರಡಲಾಗುತ್ತದೆ.( ವಾತಾವರಣವು ಅಮೋನಿಯ ಅನಿಲವನ್ನು ಹೊಂದಿದ್ದಾಗ ಸಾರಜನಕ ನಷ್ಟವಾಗುವ ಕ್ರಿಯೆ ) . ಯೂರಿಯಾ ಇತರ ಗೊಬ್ಬರಗಳೊಡನೆ ಹೊಂದಿಕೊಳ್ಳುವುದಿಲ್ಲ .
ಅತ್ಯಂತ ಹೆಚ್ಚು ಸಾರಜನಕದ ಸಾರ ಹೊಂದಿರುವ ಯೂರಿಯಾವನ್ನು ಸಮಮಟ್ಟದಲ್ಲಿ ಹರಡುವುದು ಅತಿ ಮುಖ್ಯವಾಗಿದೆ. ಅದನ್ನು ಹರಡಲು ಬಳಸುವಂತಹ ಸಲಕರಣೆಯ ಮಾಪನಾಂಕವನ್ನು ಸರಿಯಾಗಿ ನಿರ್ಣಯಿಸಬೇಕು. ಅದಲ್ಲದೇ ಅದನ್ನು ಬಳಸಬೇಕು . ಬೀಜಗಳು ಮೊಳಕೆಯೊಡೆಯ ಬಹುದಾದ ಅಪಾಯದ ಕಾರಣ ಕೂರಿಗೆಯನ್ನು ಬೀಜಗಳಿಂದ ದೂರವಿರಿಸಬೇಕು. . ಯೂರಿಯಾವನ್ನು ನೀರಿನಲ್ಲಿ ಕರಗಿಸಿ ಸಿಂಪಡಿಸಲಾಗುತ್ತದೆ. ಅಥವಾ ನೀರಾವರಿ ವಿಧಾನದ ಮೂಲಕ ಹಾಕಲಾಗುತ್ತದೆ.
ಧಾನ್ಯ ಮತ್ತು ಹತ್ತಿಯ ಬೆಳೆಗಳಲ್ಲಿ ಯೂರಿಯಾವನ್ನು ಬೀಜಬಿತ್ತುವ ಮೊದಲು ನೆಲವನ್ನು ಉತ್ತಂತಹ ಸಮಯದಲ್ಲಿ ಹಾಕಲಾಗಿರುತ್ತದೆ. ಅತಿ ಹೆಚ್ಚು ಮಳೆಬೀಳುವ ಪ್ರದೇಶಗಳಲ್ಲಿ ಮತ್ತು ಮರಳು ಮಣ್ಣಿರುವ ಪ್ರದೇಶಗಳಲ್ಲಿ (ಸಾರಜನಕವು ಪ್ರತ್ಯೇಕಿಸಲ್ಪಡುವಿಕೆಯಿಂದ ನಷ್ಟವಾಗುವ ಪ್ರದೇಶ) ಚೆನ್ನಾಗಿ ಮಳೆಯಾಗುವ ನಿರೀಕ್ಷೆಯಿರುವ ಮತ್ತು ಬೆಳೆಬೆಳೆಯುವ ಋತುವಿನಲ್ಲಿ , ಯೂರಿಯಾವನ್ನು ಮೇಲ್ ಗೊಬ್ಬರವಾಗಿ ಹಾಕಲಾಗುತ್ತದೆ. ಮೇಲ್ಗಡೆ ಗೊಬ್ಬರವು ಹುಲ್ಲು ಮತ್ತು ಮೇವುಗಳ ಬೆಳೆಗಳಿಗು ಪ್ರಸಿದ್ಧವಾಗಿದೆ. ಕಬ್ಬು ಬೆಳೆಯುವಾಗ ಅದನ್ನು ನೆಟ್ಟ ನಂತರ ಯೂರಿಯಾವನ್ನು ಪಕ್ಕದಲ್ಲಿ ಗೊಬ್ಬರವಾಗಿ ಹಾಕಲಾಗುತ್ತದೆ. ಅಲ್ಲದೇ ಪ್ರತಿ ಕೂಳೆ ಕಬ್ಬಿಗೆ ಸಿಂಪಡಿಸಲಾಗುತ್ತದೆ.
ನೀರುಹಾಯಿಸುವಂತಹ ಬೆಳೆಗಳಲ್ಲಿ ಯೂರಿಯಾವನ್ನು ಮಣ್ಣಿಗೆ ನೀರಿನಲ್ಲಿ ಕರಗಿಸದೇ ಹಾಗೆಯೇ ಅಥವಾ ಕರಗಿಸಿ ನೀರುಹಾಯಿಸುವುದರ ಮೂಲಕ ಹಾಕಲಾಗುವುದು. ಯೂರಿಯಾ ಅದರ ತೂಕವನ್ನು ನೀರಿನಲ್ಲಿ ಕರಗಿಸಿಕೊಳ್ಳುವುದು, ಆದರೆ ಅದರ ಸಾರ ಹೆಚ್ಚಾದಂತೆ ಅದನ್ನು ಕರಗಿಸುವುದು ಕಷ್ಟವಾಗುತ್ತದೆ. ಯೂರಿಯಾ ನೀರಿನಲ್ಲಿ ಕರಗುವುದು ಅಂತರುಷ್ಣಕವಾಗಿದೆ. ಇದು ಯೂರಿಯಾ ಕರಗುವ ಸಮಯದಲ್ಲಿ ದ್ರಾವಣದ ಉಷ್ಣಾಂಶವನ್ನು ಕಡಿಮೆಯಾಗುವಂತೆ ಮಾಡುತ್ತದೆ.
ಪ್ರಾಯೋಗಿಕ ಮಾರ್ಗದರ್ಶಿಯಂತೆ , ಭೂಮಿಯನ್ನು ಫಲವತ್ತಾಗಿಸಲು ಯೂರಿಯಾ ದ್ರಾವಣವನ್ನು ತಯಾರಿಸುವಾಗ (ನೀರಾವರಿ ವಲಯಗಳಿಗೆ ಹಾಕುವುದು), ಪ್ರತಿ 100 ಲೀಟರ್ ನೀರಿನಲ್ಲಿ 30 ಕೆಜಿಗಿಂತ ಹೆಚ್ಚಾಗದಂತೆ ಯೂರಿಯಾವನ್ನು ಹಾಕಿ ಕರಗಿಸಿ.
ಎಲೆಗಳ ಸಿಂಪಡಿಕೆಯಲ್ಲಿ , 0.5% – 2.0% ರಷ್ಟು ಯೂರಿಯಾ ಸಾರವನ್ನು ತೋಟಗಾರಿಕೆಯ ಬೆಳೆಗಳಿಗೂ ಬಳಸಲಾಗುತ್ತದೆ. ಯೂರಿಯಾದ ಕಡಿಮೆ ಬೈಯುರೆಟ್ ಪ್ರಮಾಣವನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಸೂಚಿಸಲಾಗುತ್ತದೆ.
ಯೂರಿಯಾ ವಾತಾವರಣದಿಂದ ತೇವಾಂಶ ಹೀರಿಕೊಳ್ಳುವ ಕಾರಣ ಅದನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಹಲಗೆಗಳ ಮೇಲೆ ಮುಚ್ಚಿದ ಚೀಲಗಳಲ್ಲಿ ಅಥವಾ ಟಾರ್ಪಾಲಿನ್ ನಿಂದ ಮುಚ್ಚಿ ಇಡಲಾಗುತ್ತದೆ. ಗಟ್ಟಿಯಾಗಿರುವ ಗೊಬ್ಬರದ ಜೊತೆಯಲ್ಲಿ ತಣ್ಣನೆಯ , ಒಣಗಿದಂತಹ ಚೆನ್ನಾಗಿ ಗಾಳಿಯಾಡುವಂತಹ ಸ್ಥಳದಲ್ಲಿ ಇಡಲಾಗುತ್ತದೆ.
ರಾಸಾಯನಿಕ ಕೈಗಾರಿಕೆ[ಬದಲಾಯಿಸಿ]
ಯೂರಿಯಾ ಅನೇಕ ಪ್ರಮುಖ ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳ ಉತ್ಪಾದನೆಗೆ ಕಚ್ಛಾವಸ್ತುವಾಗಿದೆ. ಉದಾಹರಣೆಗೆ:
- ವಿವಿಧ ಪ್ಲಾಸ್ಟಿಕ್ ಗಳು, ವಿಶೇಷವಾಗಿ ಯೂರಿಯಾ -ಫಾರ್ಮ್ಯಾಲ್ಡಿಹೈಡ್ ರೆಸಿನ್ಸ್ .
- ವಿವಿಧ ಗೊಂದುಗಳು, ಉದಾಹರಣೆಗೆ ಯೂರಿಯಾ-ಫಾರ್ಮ್ಯಾಲ್ಡಿಹೈಡ್ ಅಥವಾ ಯೂರಿಯಾ-ಮೆಲಮೀನ್-ಫಾರ್ಮ್ಯಾಲ್ಡಿಹೈಡ್ ಕಡಲಿನ ಪದರ ಹಲಗೆಗಳಿಗೆ ಬಳಸುತ್ತಾರೆ.
- ಪೊಟ್ಯಾಸಿಯಮ್ ಸೈನೆಟ್ , ಮತ್ತೊಂದು ಕೈಗಾರಿಕೆಯ ಕಚ್ಛಾ ಸಾಮಗ್ರಿ.
- ಯೂರಿಯಾ ನೈಟ್ರೇಟ್, ಸ್ಪೋಟಕ.
ಸ್ವಯಂಚಾಲಿತ ವ್ಯವಸ್ಥೆಗಳು[ಬದಲಾಯಿಸಿ]
ದಹನ ಕ್ರಿಯೆಯಿಂದ ಹೊರಬರುವ ಮಲಿನಕಾರಿ NOx ನ್ನು ಕಡಿಮೆಮಾಡಲು ಯೂರಿಯಾ SNCR ಮತ್ತು SCRನ ಪರಿವರ್ತನೆಯಾಗಿ ಉಪಯೋಗಿಸಲ್ಪಡುತ್ತದೆ. ಉದಾಹರಣೆಗೆ ಶಕ್ತಿಕೇಂದ್ರಗಳಿಂದ ಮತ್ತು ಡೀಸಲ್ ಇಂಜಿನ್ ಗಳಿಂದ. ಡೀಸಲ್ ಇಂಜಿನ್ ನಲ್ಲಿ ಇದನ್ನು ವಿಭಜಿಸಿ ಶೋಧಿಸಿದ ಡೀಸಲ್ ನ ಪುನರುತ್ಪಾದನೆಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಬ್ಲ್ಯೂ ಟೆಕ್ ವಿಧಾನ, ಉದಾಹರಣೆಗೆ ನೀರಿನಲ್ಲಿ ಕರಗಬಲ್ಲ ಯೂರಿಯಾವನ್ನು ನಿಷ್ಕಾಸ ವಿಧಾನಕ್ಕೆ ಹಾಕುವುದು. ಯೂರಿಯಾ ವಿಭಜನೆಯಿಂದ ಉತ್ಪತ್ತಿಯಾಗುವ ಅಮೋನಿಯ ನೈಟ್ರೋಜನ್ ಆಕ್ಸೈಡ್ ನ ಉತ್ಸರ್ಜನಗಳೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ. ಅಲ್ಲದೇ ಇದು ವೇಗವರ್ಧನೆ ಪರಿವರ್ತಕದಲ್ಲಿ ಸಾರಜನಕ ಮತ್ತು ನೀರಾಗಿ ಬದಲಾಗುತ್ತದೆ.
ಇತರ ವಾಣಿಜ್ಯ ಬಳಕೆಗಳು(ಉಪಯೋಗಗಳು)[ಬದಲಾಯಿಸಿ]
ಈ ಲೇಖನದಿಂದ ಬೇರೆ ಯಾವುದೇ ಲೇಖನಕ್ಕೆ ಬಾಹ್ಯ ಸಂಪರ್ಕ ಹೊಂದಿಲ್ಲ. (May 2010) |
- ನೈಟ್ರೊ ಸೆಲ್ಯುಲೋಸ್ ಸ್ಪೋಟಕಗಳಲ್ಲಿ ಸ್ಟೇಬಿಲೈಸರ್.
- ಪ್ರಾಣಿಗಳ ಆಹಾರದ ಘಟಕ,ಬೆಳವಣಿಗೆಯನ್ನು ಹೆಚ್ಚಿಸಲು ಸುಲಭವಾಗಿ ಪಡೆಯಬಹುದಾದ ಸಾರಜನಕವನ್ನು ನೀಡುತ್ತದೆ.
- ರಸ್ತೆಯಲ್ಲಿನ ಮಂಜುಗಡ್ಡೆಯನ್ನು ತೆಗೆಯಲು ಸವೆದು ಹೋಗದ ಕಲ್ಲುಪ್ಪಿನ ಒಂದು ಪರ್ಯಾಯವಾಗಿ, ಹಾಗು ಸ್ನೋಬೋರ್ಡಿಂಗ್ ಗೆ ಹೊಸ ಮೇಲ್ಮೈಯನ್ನು ಹಾಕಲು ಹಾಫ್ ಪೈಪ್ ಗಳು ಹಾಗು ಭೂಪ್ರದೇಶದ ಕೃತಕ ಉದ್ಯಾನಗಳಲ್ಲಿ ಬಳಸಲಾಗುತ್ತದೆ.
- ಸಿಗರೇಟ್ನ ಪರಿಮಳವನ್ನು ಹೆಚ್ಚಿಸುವ ದ್ರವ.
- ಕೊದಲನ್ನು ತೆಗೆಯಲು ಬಳಸುವ ಸಾಧನಗಳ ಮುಖ್ಯ ಘಟಕಾಂಶವಾಗಿದೆ. ಉದಾಹರಣೆಗೆ : ನ್ಯೆರ್ ಅಥವಾ ವೀಟ್
- ಉಪ್ಪಿನ ಬಿಸ್ಕತ್ತುಗಳನ್ನು ತಯಾರಿಸುವ ಕಾರ್ಖಾನೆಗಳಲ್ಲಿ ಕಂದುಸಕ್ಕರೆ ಕಾರಕವಾಗಿದೆ.
- ಕೆಲವು ಹೇರ್ ಕಂಡಿಷನರ್, ಫೆಷಿಯಲ್ ಕ್ಲೆನ್ಸರ್ , ಬಾತ್ ಆಯಿಲ್, ಸ್ಕಿನ್ ಸಾಫ್ಟನರ್ಸ್ ಮತ್ತು ಲೋಷನ್ ಗಳಲ್ಲಿ ಘಟಕಾಂಶವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ.
- ಪ್ರಥಮ ಚಿಕಿತ್ಸೆಗೆ ಬಳಸಲು ಸಿದ್ಧವಿರುವ ಕೆಲವು ಕೋಲ್ಡ್ ಕಂಪ್ರೆಸಸ್ ನ ಪ್ರತಿಕ್ರಿಯಾಕಾರಿಯಾಗಿ ವರ್ತಿಸುತ್ತದೆ.ನೀರಿನಲ್ಲಿ ಬೆರೆಸಿದಾಗ ಅಂತರುಷ್ಣಕದ ಪ್ರತಿಕ್ರಿಯೆಯಿಂದ ಇದು ಸೃಷ್ಟಿಸುತ್ತದೆ.
- ಇತರ ಉಪ್ಪುಗಳ ಜೊತೆಯಲ್ಲಿ ಬಿತ್ತನೆಯ ಮೋಡವಾಗಿದೆ.
- ಅಗ್ನಿ ಶಾಮಕ ವಸ್ತುವಾಗಿದೆ . ಸಾಮಾನ್ಯವಾಗಿ ಇದನ್ನು ಒಣ ರಾಸಾಯನಿಕ ರೂಪದಲ್ಲಿ ಬೆಂಕಿಯನ್ನು ನಂದಿಸಲು ಬಳಸಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ:ಯೂರಿಯಾ- ಪೊಟ್ಯಾಸಿಯಮ್ ಬೈಕಾರ್ಬನೇಟ್ ಗಳ ಮಿಶ್ರಣ.
- ಹಲ್ಲನ್ನು ಬಿಳಿಮಾಡುವ ಅನೇಕ ಉತ್ಪನ್ನಗಳ ಘಟಕಾಂಶವಾಗಿದೆ.
- ಪಾತ್ರೆತೊಳೆಯುವ ಸಾಬೂನುಗಳ ಘಟಕಾಂಶವಾಗಿದೆ.
- ಅಮೋನಿಯಮ್ ಫಾಸ್ಫೇಟ್ ನ ಜೊತೆಯಲ್ಲಿ , ಸಕ್ಕರೆಯನ್ನು ಈತೈಲ್ ಅಲ್ಕೊಹಾಲ್ ಆಗಿ ಕಿಣ್ವಿಸುವ ಕಿಣ್ವ ಪೌಷ್ಠಿಕಾಂಶವಾಗಿದೆ.
- ಜೀಯೋಇಂಜಿನಿಯರಿಂಗ್ ಉದ್ದೇಶಕ್ಕಾಗಿ ಮಾಡಲಾದ ಸಾಗರ ಪೋಷಣೆ ಪ್ರಯೋಗದಲ್ಲಿ ಪ್ಲವಕ ಬಳಸುವಂತಹ ಪೌಷ್ಟಿಕಾಂಶ.
- ಕಾರ್ಯ ಚಟುವಟಿಕೆಯ ತಾಪಮಾನವನ್ನು ಹಾಗು ಹೈಡ್ ಗ್ಲೂ ನ ಓಪನ್ ಟೈಮ್ ನ್ನು ವಿಸ್ತರಿಸಲು ಬಳಸಲಾಗುತ್ತದೆ.
- ದ್ರಾವ್ಯತೆಯನ್ನು ಹೆಚ್ಚಿಸುವ ಹಾಗು ಆರ್ದ್ರತೆಯನ್ನು ಉಳಿಸಿಕೊಳ್ಳುವ ಸಂಯೋಜನಿಯಗಳನ್ನು ಬಟ್ಟೆಗಳಿಗೆ ಬಣ್ಣ ಮತ್ತು ಮುದ್ರೆಗಳನ್ನು ಹಾಕುವ ಬಣ್ಣದಲ್ಲಿ ಅದ್ದಲು ಬಳಸುತ್ತಾರೆ.
ಪ್ರಯೋಗಾಲಯದ ಬಳಕೆಗಳು[ಬದಲಾಯಿಸಿ]
ಯೂರಿಯಾ 10 Mಗಳ ಸಾರತೆಯಲ್ಲಿ ಪ್ರೋಟೀನ್ ನ ಶಕ್ತಿಶಾಲಿ ಸ್ವರೂಪ ಪರಿವರ್ತಕವಾಗಿದೆ.ಇದು ಪ್ರೋಟೀನ್ ನಲ್ಲಿ ಕೋವೆಲನ್ಸಿ ಬಂಧವಲ್ಲದ್ದನ್ನು ಪರಿವರ್ತಿಸುತ್ತವೆ. ಈ ಗುಣವನ್ನು ಕೆಲವು ಪ್ರೋಟೀನ್ ಗಳ ದ್ರಾವ್ಯತೆಯನ್ನು ಹೆಚ್ಚಿಸಲು ಉಪಯೋಗಿಸಲಾಗುತ್ತದೆ. ಯೂರಿಯಾ ಮತ್ತು ಕೋಲೀನ್ ಕ್ಲೋರೈಡ್ ಗಳ ಮಿಶ್ರಣವನ್ನು ತೀವ್ರವಾದ ಯೂಟೆಕ್ಟಿಕ್ ದ್ರಾವಕವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ. ಇದು ಅಯಾನು ರೂಪದ ದ್ರವವಾಗಿದೆ.
ಇಂಧನ ಕೋಶಗಳು ಉತ್ಪಾದಿಸುವ ಶಕ್ತಿಯಲ್ಲಿ ಜಲಜನಕ ಆಧಾರವಾಗಿ ಯೂರಿಯಾ ಪ್ರಮುಖವಾಗಿ ಬಳಸಲ್ಪಡುತ್ತದೆ. ಮೂತ್ರ/ತ್ಯಾಜ್ಯ ನೀರಿನಲ್ಲಿರುವ ಯೂರಿಯಾವನ್ನು ನೇರವಾಗಿ ಬಳಸಬಹುದು. (ಆದಾಗ್ಯೂ ಬ್ಯಾಕ್ಟೀರಿಯ ಸಾಮಾನ್ಯವಾಗಿ ಯೂರಿಯಾವನ್ನು ಸರಳ ಸಂಯುಕ್ತಗಳಾಗಿ ಒಡೆಯುತ್ತದೆ.) ಕಡಿಮೆ ವೋಲ್ಟೇಜ್ (0.37v) ಇರುವಾಗ ವಿದ್ಯುದ್ವಿಚ್ಛೇದನದ ಯೂರಿಯಾ ವಿಲಯನದಿಂದ ಜಲಜನಕವನ್ನು ಉತ್ಪಾದಿಸಲಾಗುತ್ತದೆ. ಇದು ನೀರಿನ ವಿದ್ಯುದ್ವಿಚ್ಛೇದನಕ್ಕಿಂತ ಕಡಿಮೆ ಶಕ್ತಿಯನ್ನು ತೆಗೆದುಕೊಳ್ಳುತ್ತದೆ.[೪]
ವೈದ್ಯಕೀಯ ಉಪಯೋಗಳು[ಬದಲಾಯಿಸಿ]
ಪ್ರಚಲಿತ ಚರ್ಮಶಾಸ್ತ್ರದ ಉತ್ಪನ್ನಗಳಲ್ಲಿ ಯೂರಿಯಾವನ್ನು ಚರ್ಮ ಪುನರ್ಜಲೀಕರಣ ಮಾಡಲು ಬಳಸುತ್ತಾರೆ. ಅಕ್ಲೂಸಿವ್ ಡ್ರೆಸಿಂಗ್ ನಿಂದ ಮುಚ್ಚಲ್ಪಟ್ಟಿದ್ದರೆ ಯೂರಿಯಾದಿಂದ ತಯಾರಿಸಲ್ಪಟ್ಟಂತ 40% ವಸ್ತುಗಳನ್ನು ಶಸ್ತ್ರ ಚಿಕಿತ್ಸೆಗೊಳಪಡಿಸದೆ ಉಗುರನ್ನು ತೆಗೆಯಲೂ ಕೂಡ ಬಳಸಲಾಗುತ್ತದೆ. ಈ ಜೌಷಧವನ್ನು ಕಿವಿಯ ಗುಗ್ಗೆಯನ್ನು ತೆಗೆಯಲೂ ಕೂಡ ಬಳಸಲಾಗುತ್ತದೆ.
ಕೆಲವು ಬಗೆಯ ತಕ್ಷಣಕ್ಕೆ ಬಳಸುವಂತಹ ಕೋಲ್ಡ್ ಫ್ಯಾಕ್ ಗಳು, (ಅಥವಾ ಐಸ್ ಫ್ಯಾಕ್) ನೀರನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಅಲ್ಲದೇ ಯೂರಿಯಾ ಹರಳುಗಳನ್ನು ಬೇರ್ಪಡಿಸುತ್ತವೆ. ಇಂಟರ್ ನಲ್ ವಾಟರ್ ಬ್ಯಾಗ್ ನ ಒಡೆಯುವಿಕೆಯಿಂದ ಅಂತರುಷ್ಣಕ ಪ್ರಕ್ರಿಯೆ ಪ್ರಾರಂಭವಾಗುತ್ತದೆ. ಅಲ್ಲದೇ ಊತವನ್ನು ಕಡಿಮೆ ಮಾಡಲು ಪ್ಯಾಕ್ ನ್ನು ಉಪಯೋಗಿಸುವ ಅವಕಾಶವನ್ನು ನೀಡುತ್ತದೆ.
ಸಲೈನ್ ನಂತೆ , ಯೂರಿಯಾ ಚುಚ್ಚು ಮದ್ದನ್ನು ಗರ್ಭಪಾತಮಾಡಿಸಲು ಬಳಸಲಾಗುತ್ತದೆ.
ಯೂರಿಯಾ ಪರ್ಯಾಯ ಜೌಷಧೋಪಚಾರದ ಮುಖ್ಯ ಘಟವಾಗಿದೆ. ಇದನ್ನು ಮೂತ್ರ ಚಿಕಿತ್ಸೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ರಕ್ತದ ಯೂರಿಯಾ ಸಾರಜನಕ (BUN) ಪರೀಕ್ಷೆಯು ಯೂರಿಯಾದಿಂದ ರಕ್ತದಲ್ಲಿ ಬಂದಿರುವ ಸಾರಜನಕದ ಪ್ರಮಾಣವನ್ನು ಅಳತೆ ಮಾಡಲು ಮಾಪಕವಾಗಿದೆ. ಇದನ್ನು ಮೂತ್ರಪಿಂಡದ ಕಾರ್ಯವನ್ನು ಗುರುತಿಸಲು ಬಳಸಲಾಗುತ್ತದೆ.
ಕಾರ್ಬನ್ -14 ಅಥವಾ ಕಾರ್ಬನ್-13ನ ಪಟ್ಟಿಯಲ್ಲಿ ಸೇರಿಸಲಾಗಿರುವ ಯೂರಿಯಾವನ್ನು ಯೂರಿಯಾ ಉಸಿರಾಟದ ಪರೀಕ್ಷೆಗೆ ಉಪಯೋಗಿಸಲಾಗುತ್ತದೆ . ಇದನ್ನು ಮಾನವರ ಚಿಕ್ಕ ಕರುಳಿನ ಭಾಗದಲ್ಲಿ ಮತ್ತು ಹೊಟ್ಟೆಯಲ್ಲಿ ಇರುವ , ಹುಣ್ಣಿಗೆ ಸಂಬಂಧಿಸಿದಂತಹ ಹೆಲಿಕೊಬ್ಯಾಕ್ಟರ ಪೈಲರಿ (H. pylori ) ಎಂಬ ಬ್ಯಾಕ್ಟೀರಿಯದ ಇರುವಿಕೆಯನ್ನು ಕಂಡುಹಿಡಿಯಲು ಬಳಸಲಾಗುತ್ತದೆ. ಈ ಪರೀಕ್ಷೆಯು ಯೂರಿಸ್ ಕಿಣ್ವದ ವೈಷಿಷ್ಟ್ಯವನ್ನು H. pylori ಮೂಲಕ ಕಂಡುಹಿಡಿಯಲಾಗುತ್ತದೆ. ಇದನ್ನು ಯೂರಿಯಾಾದಿಂದ ಅಮೋನಿಯವನ್ನು ಬಿಡುಗಡೆಮಾಡುವ ಪ್ರಕ್ರಿಯೆಯಿಂದ ಕಂಡುಹಿಡಿಯಲಾಗುತ್ತದೆ. ಇದು ಹೊಟ್ಟೆಯ ಬ್ಯಾಕ್ಟೀರಿಯ ಸುತ್ತಲಿನ pHಅನ್ನು(ಆಮ್ಲತೆಯನ್ನು ಕಡಿಮೆಮಾಡುತ್ತದೆ) ಹೆಚ್ಚಿಸುತ್ತದೆ. ಮಂಗ,ನಾಯಿ,ಬೆಕ್ಕಿನಂತಹ (ದೊಡ್ಡ ಬೆಕ್ಕುಗಳನ್ನು ಒಳಗೊಂಡಂತೆ) ಪ್ರಾಣಿಗಳಲ್ಲಿ H. pylori ಯಂತಹ ಬ್ಯಾಕ್ಟೀರಿಯಗಳನ್ನು ಅದೇ ಪರೀಕ್ಷೆಯ ಮೂಲಕ ಕಂಡುಹಿಡಿಯಬಹುದು.
ಭಯೋತ್ಪಾದನೆ[ಬದಲಾಯಿಸಿ]
ಅಹ್ಮದ್ ರೆಸ್ಸಂ, ಅಲ್-ಖೈದಾ ಸಂಘಟನೆಯ ಸಹಸ್ರಮಾನದ ಬಾಂಬರ್, 1999/2000ದ ಹೊಸ ವರ್ಷದ ಮುನ್ನಾದಿನ ಲಾಸ್ ಏಂಜಲಿಸ್ ಅಂತಾರಾಷ್ಟ್ರೀಯ ವಿಮಾನ ನಿಲ್ದಾಣ ವನ್ನು ಸ್ಫೋಟಿಸಲು ತಯಾರಿ ಮಾಡಿಕೊಂಡಂತಹ ಸ್ಫೋಟಕಗಳಲ್ಲಿ ಯೂರಿಯಾವನ್ನೂ ಸಹ ಒಂದು ರಾಸಾಯನಿಕ ಪದಾರ್ಥವನ್ನಾಗಿ ಬಳಕೆ ಮಾಡಿಕೊಂಡಿದ್ದ; ಈ ಸ್ಫೋಟಕ ಒಂದು ವಿಧ್ವಂಸಕ ಕಾರ್ ಬಾಂಬ್ ಸ್ಫೋಟಕ್ಕಿಂತ 40x ಗೂ ಅಧಿಕ ಪರಿಣಾಮಕಾರಿಯಾಗಿತ್ತು.[೫][೬]
ಸಂಶ್ಲೇಷಿತ ಉತ್ಪಾದನೆ[ಬದಲಾಯಿಸಿ]
ವಿಶ್ವವ್ಯಾಪಿಯಾಗಿ ಯೂರಿಯಾವನ್ನು ವಾರ್ಷಿಕವಾಗಿ 100,000,000 ಟನ್ ಗಳಷ್ಟು ಪ್ರಮಾಣದಲ್ಲಿ ತಯಾರಿಕೆ ಮಾಡಲಾಗುತ್ತದೆ.[೭]
ಕೈಗಾರಿಕಾ ವಿಧಾನಗಳು[ಬದಲಾಯಿಸಿ]
ಕೈಗಾರಿಕೆಗಳಲ್ಲಿ ಬಳಸಲು , ಸಿಂತೆಟಿಕ್ ಅಮೋನಿಯ ಮತ್ತು ಕಾರ್ಬನ್ ಡೈಆಕ್ಸೈಡ್ನಿಂದ ಯೂರಿಯಾವನ್ನು ಉತ್ಪಾದಿಸಲಾಗುತ್ತದೆ. ಕಲ್ಲಿದ್ದಲು ಅಥವಾ ಹೈಡ್ರೋ ಕಾರ್ಬನ್ ನಿಂದ ಅಮೋನಿಯವನ್ನು ತಯಾರಿಸುವಾಗ ಬೃಹತ್ ಪ್ರಮಾಣದ ಕಾರ್ಬನ್ ಡೈಆಕ್ಸೈಡ್ ಉತ್ಪತ್ತಿಯಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ: ಕಚ್ಛಾ ವಸ್ತುಗಳಿಂದ ಪಡೆದಂತಹ ನೈಸರ್ಗಿಕ ಅನಿಲ ಮತ್ತು ಪೆಟ್ರೋಲಿಯಮ್ . ಈ CO2 ನ ಮೂಲಗಳು ಯೂರಿಯಾದ ನೇರ ಸಂಶ್ಲೇಷಣೆಗೆ ದಾರಿ ಮಾಡಿಕೊಡುತ್ತವೆ.
ಮೂಲ ವಿಧಾನವನ್ನು 1922 ರಲ್ಲಿ ಕಂಡುಹಿಡಿಯಲಾಯಿತು. ಇದನ್ನು ಕಂಡುಹಿಡಿದ ನಂತರ ಬಾಶ್ -ಮಿಸರ್ ಯೂರಿಯಾ ವಿಧಾನವೆಂದೂ ಕೂಡ ಕರೆಯಲಾಗುತ್ತದೆ. ಯೂರಿಯಾ ಉತ್ಪತ್ತಿಯಾಗುವ ರೀತಿಯಿಂದ ಹಾಗು ಯಾವ ರೀತಿಯಲ್ಲಿ ಬದಲಾಗದಂತಹ ಪ್ರತಿಕ್ರಿಯಾಕಾರಿಗಳು ಮತ್ತಷ್ಟು ಪ್ರಕ್ರಿಯೆಗೆ ಒಳಪಡುತ್ತವೆ ಎಂಬುದರ ಮೇಲೆ ಯೂರಿಯಾದ ಅನೇಕ ವಿಧಾನಗಳನ್ನು ವಿವರಿಸಲಾಗುತ್ತದೆ. ಈ ವಿಧಾನವು ಪ್ರತಿಕ್ರಿಯಾಕಾರಿಗಳ ಅಪೂರ್ಣ ಪರಿವರ್ತನೆಯ ಜೊತೆಯಲ್ಲಿ ಎರಡು ಮುಖ್ಯ ಸಮತೋಲನ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಒಳಗೊಂಡಿದೆ. ಮೊದಲನೆಯದು ದ್ರವರೂಪದಲ್ಲಿರುವ ಅಮೋನಿಯದ ಬಹಿರುಷ್ಣಕ ಪ್ರತಿಕ್ರಿಯೆಯಾಗಿದೆ . ಇದು ಅಮೋನಿಯಮ್ ಕಾರ್ಬನೇಟ್ಅನ್ನು ರೂಪಿಸುವ ಡ್ರೈ ಐಸ್ಅನ್ನು ಒಳಗೊಂಡಿದೆ .(H2N-COONH4):[೮]:
- 2 NH3 + CO2 ↔ H2N-COONH4 ()
ಎರಡನೆಯದು ಅಮೋನಿಯಮ್ ಕಾರ್ಬನೇಟ್ ಯೂರಿಯಾ ಮತ್ತು ನೀರಾಗಿ ವಿಭಜನೆಯಾಗುವ ಅಂತರುಷ್ಣಕ ಪ್ರತಿಕ್ರಿಯೆಯಾಗಿದೆ:
- H2N-COONH4 ↔ (NH2)2CO + H2O
ಎರಡು ಪ್ರತಿಕ್ರಿಯೆಗಳು ಬಹಿರುಷ್ಣಕವಾಗಿ ಸಂಯೋಜಿಸಲ್ಪಟ್ಟಿವೆ.[೭]
ಪರಿವರ್ತನೆಯಾಗದ ಪ್ರತಿಕ್ರಿಯಾಕಾರಿಗಳನ್ನು ಇತರ ಉತ್ಪನ್ನಗಳ ತಯಾರಿಕೆಯಲ್ಲಿ ಬಳಸಬಹುದು. ಉದಾಹರಣೆಗೆ:ಅಮೋನಿಯಮ್ ನೈಟ್ರೇಟ್ ಅಥವಾ ಸಲ್ಫೇಟ್. ಅಲ್ಲದೇ ಒಟ್ಟು ಮರುಬಳಕೆಯ ವಿಧಾನದಲ್ಲಿ ಯೂರಿಯಾವನ್ನು ಸಂಪೂರ್ಣವಾಗಿ ಪರಿವರ್ತಿಸಬಹುದು.
ಯೂರಿಯಾಾವನ್ನು ಪ್ರಿಲ್ ಗಳ, ಸಣ್ಣ ಕಾಳುಗಳ, ಗೋಲಿಗಳ, ಹರಳುಗಳ, ಮತ್ತು ಕರುಗುವ ರೂಪದಲ್ಲಿ ಉತ್ಪಾದಿಸಬಹುದು. ಘನ ರೂಪದಲ್ಲಿರುವ ಯೂರಿಯಾವನ್ನು ಪ್ರಿಲ್ ಗಳು ಅಥವಾ ಸಣ್ಣಕಣಗಳೆಂದು ಗುರುತಿಸಲಾಗುತ್ತದೆ. ಸಾಮಾನ್ಯವಾಗಿ ಪ್ರಿಲ್ಸ್ ನಿಂದ ಆಗುವ ಲಾಭವೇನೆಂದರೆ ಅವುಗಳನ್ನು ಸಣ್ಣಕಣಗಳಿಗಿಂತ ಹೆಚ್ಚು ಅಗ್ಗದಲ್ಲಿ ಉತ್ಪಾದಿಸಬಹುದು. ಉದಾಹರಣೆಗಾಗಿ, ಲಕ್ಷಣಗಳಾದ ಪ್ರಭಾವಿ ಶಕ್ತಿ, ಪುಡಿಮಾಡುವ ಶಕ್ತಿ ಮತ್ತು ಸ್ವತಂತ್ರವಾದ ನಡವಳಿಕೆ ಇವೆಲ್ಲವು ನಿರ್ದಿಷ್ಟವಾಗಿ ಉತ್ಪನ್ನಗಳ ನಿರ್ವಹಣೆ, ಸಂಗ್ರಹಣೆ ಹಾಗು ಬೃಹತ್ ಪ್ರಮಾಣದ ಸಾಗಾಣಿಕೆಗೆ ಅತ್ಯವಶ್ಯಕವಾಗಿದೆ. ಉತ್ಪಾದನೆಯಲ್ಲಿನ ವಿಶೇಷವಾದ ಅಶುದ್ಧತೆಯು ಬೈಯುರೆಟ್ ಮತ್ತು ಐಸೋನಿಕ್ ಆಮ್ಲವಾಗಿದೆ:
- 2 H2CONH2 → H2CONHCONH2 + NH3
- H2CONH2 → HNCO + NH3
ಬೈಯುರೆಟ್ ಯಾವಾಗಲೂ ಗೊಬ್ಬರವನ್ನು ಹಾಕುವಂತಹ ಪ್ರತಿ ಗಿಡಗಳಿಗೆ ವಿಷವಾಗಿ ಪರಿಣಮಿಸಬಹು. ಆದ್ದರಿಂದ ಇದೊಂದು ಗಮನಿಸಬೇಕಾದ ಅಂಶವಾಗಿದೆ. ಯೂರಿಯಾಾವನ್ನು ಬೈಯುರೆಟ್ ಅಂಶಗಳ ಆಧಾರದ ಮೇಲೆ ವಿಂಗಡಿಸಲಾಗಿದೆ.
ಪ್ರಾಯೋಗಿಕ ಪ್ರಕ್ರಿಯೆಗಳು[ಬದಲಾಯಿಸಿ]
ಯೂರಿಯಾಗಳು ಸಾಮಾನ್ಯ ಅಭಿಪ್ರಾಯದಂತೆ ಪ್ರಯೋಗಾಲಯದಲ್ಲಿ ಫೋಸ್ಜೀನ್ ನ ಪ್ರತಿಕ್ರಿಯೆಯಲ್ಲಿ ಪ್ರಾಥಮಿಕ ಅಥವಾ ದ್ವಿತಿಯಾರ್ಥಕ ಅಮೈನ್ಗಳ ಮೂಲಕ ಪ್ರಭಾವಕ್ಕೆ ಒಳಗಾಗುತ್ತದೆ. ಇದು ಐಸೊಸಯಾನೆಟ್ ಮಧ್ಯಂತರ ಸಂಯುಕ್ತತೆಯ ಮೂಲಕ ಕಾರ್ಯವಿಧಾನವು ನಡೆಯುತ್ತದೆ. ಅಸಮ್ಮತೀಯ ಯೂರಿಯಾಗಳನ್ನು ಐಸೊಸಯಾನೆಟ್ ಜೊತೆಗಿನ ಪ್ರಾಥಮಿಕ ಅಥವಾ ದ್ವಿತಿಯಾರ್ಧಕ ಅಮೈನ್ ಗಳ ಪ್ರತಿಕ್ರಿಯೆಯ ಮೂಲಕ ಪ್ರಭಾವಕ್ಕೆ ಒಳಪಡಿಸಲಾಗುತ್ತದೆ.
ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು[ಬದಲಾಯಿಸಿ]
ಆಣ್ವಿಕ ಮತ್ತು ಹರಳಿನ ರಚನೆ[ಬದಲಾಯಿಸಿ]
ಯೂರಿಯಾ ಅಣುಗಳು ಸಮತಲದ ಆಕಾರದಲ್ಲಿದೆ. ಘನಾಕಾರದ ಯೂರಿಯಾದಲ್ಲಿ, ಆಮ್ಲಜನಕ ಕೇಂದ್ರವು ಎರಡು N-H-O ಜಲಜನಕ ಬಂಧಕಗಳೊಂದಿಗೆ ಸೇರಿಕೊಂಡಿದೆ. ಇದರ ಫಲವಾಗಿ, ಹೆಚ್ಚು ಸಾಂಧ್ರತೆ ಮತ್ತು ಶಕ್ತಿಶಾಲಿಯಾದ ಜಲಜನಕ-ಬಂಧಕ ಜಾಲವು, ಆಣ್ವಿಕ ಪ್ಯಾಕಿಂಗನ ಬದಲಿಗೆ ಸ್ಥಾಪಿಸಲಾಗಿದೆ: ಈ ರಚನೆಯು ಮುಕ್ತವಾಗಿದೆ, ಇಲ್ಲಿ ಚೌಕಟ್ಟಾದ ಅಡ್ಡಕೊಯ್ತ ಹೊಂದಿರುವ ಸುರಂಗಗಳಂತಿವೆ. ಯೂರಿಯಾದಲ್ಲಿರನ ಇಂಗಾಲವನ್ನು sp2ಮೂಲದಲ್ಲಿ ಸಂಕರೀಕೃತಗೊಳಿಸಲಾಗಿದೆ, C-N ಬಂಧಕಗಳು ಗಮನಾರ್ಹವಾದ ದ್ವಿ-ಬಂಧಕ ಗುಣಲಕ್ಷಣವನ್ನು ಹೊಂದಿದೆ, ಕಾರ್ಬೊನೈಲ್ ಆಮ್ಲಜನಕವು ಫೊರ್ಮಾಲ್ಡಿಹೈಡ್ಗೆ ಹೋಲಿಸಿದರೆ ಮೂಲಭೂತ ರೂಪದಾಗಿದೆ. ಯೂರಿಯಾದ ಹೆಚ್ಚಿನ ನೀರಿನ ವಿಲೇಯತೆಯು, ನೀರಿನೊಂದಿಗೆ ವಿಸ್ತೃತ ಜಲಜನಕ ಬಂಧನದಲ್ಲಿ ಸೇರುವ ಕ್ಷಮತೆಯ ನಿದರ್ಶನವನ್ನು ನೀಡುತ್ತದೆ.
ರಂಧ್ರಗಳುಳ್ಳ ಚೌಕಟ್ಟುಗಳನ್ನು ರಚಿಸಿಕೊಳ್ಳುವ ಪ್ರವೃತ್ತಿಯ ಕಾರಣ, ಯೂರಿಯಾ ಹಲವು ಸಾವಯವ ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳನ್ನು ಸೆರೆಹಿಡಿಯುವ ಕ್ಷಮತೆ ಹೊಂದಿದೆ. ಕ್ಲ್ಯಾಥ್ರೇಟ್ ಎನ್ನಲಾದ ಸಂಯುಕ್ತಗಳಲ್ಲಿ, ಪರಸ್ಪರ-ಛೇದಿಸುವ, ಜಲಜನಕ-ಬಂಧಕಗಳುಳ್ಳ ಯೂರಿಯಾ ಅಣುಗಳನ್ನು ಹೊಂದಿರುವ ಹೀಲಿಕ್ಸ್ಗಳು ರಚಿಸುವ ಕೊಳವೆಗಳಲ್ಲಿ ಸಾವಯವ ಅತಿಥಿ ಅಣುಗಳನ್ನು ಹಿಡಿದುಕೊಳ್ಳುತ್ತವೆ. ಮಿಶ್ರಣಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲು ಈ ವರ್ತನೆಯನ್ನು ಬಳಸಬಹುದಾಗಿದೆ. ಉದಾಹರಣೆಗೆ, ವಾಯುಯಾನ ಇಂಧನ ತಯಾರಿಕೆ ಹಾಗೂ ಘರ್ಷಣೆ-ನಿರೋಧಕ ತೈಲಗಳ ತಯಾರಿಕೆ ಹಾಗೂ ಪ್ಯಾರಾಫಿನ್ಗಳನ್ನು ಪ್ರತ್ಯೇಕಗೊಳಿಸಲು ಇದನ್ನು ಬಳಸಬಹುದಾಗಿದೆ.
ಹೆಲಿಕ್ಸ್ಗಳು ಪರಸ್ಪರ ಸಂಪರ್ಕದಲ್ಲಿರುವುದರಿಂದ, ಹರಳಿನಲ್ಲಿರುವ ಎಲ್ಲಾ ಹೆಲಿಕ್ಸ್ಗಳು ಅದೇ ಆಣ್ವಿಕ ರೂಪವನ್ನು ಹೊಂದಿರತಕ್ಕದ್ದು. ಹರಳನ್ನು ಬೀಜೀಕರಿಸಿದಾಗ ಇದನ್ನು ನಿರ್ಣಯಿಸಲಾಗುತ್ತದೆ. ಬೀಜ ಬಿತ್ತುವುದರ ಮೂಲಕವೂ ಇದನ್ನು ನಡೆಸಬಹುದು. ರೆಸಿಮೀಯ ಮಿಶ್ರಣವನ್ನು ಪ್ರತ್ಯೇಕಿಸಲು ಈ ಹರಳುಗಳನ್ನು ಬಳಸಲಾಗಿದೆ.
ಪ್ರತಿಕ್ರಿಯೆಗಳು[ಬದಲಾಯಿಸಿ]
ಯೂರಿಯಾ, ಅಲ್ಕೋಹಾಲ್ ಜೊತೆಗೆ ಪ್ರತಿ ಪರಿಣಾಮಕ್ಕೊಳಪಡುವುದರ ಜೊತೆಗೆ ಯೂರಿಥೆನ್ ಗಳನ್ನು ರೂಪಿಸುತ್ತದೆ. ಯೂರಿಯಾ ಮಾಲೋನಿಕ್ ಎಸ್ಟರ್ ಗಳ ಜೊತೆ ಪ್ರತಿ ಪರಿಣಾಮಕ್ಕೊಳಪಟ್ಟು ಬಾರ್ಬಿಟ್ಯೂರಿಕ್ ಆಸಿಡ್ಗಳನ್ನು ಸೃಷ್ಟಿಸುತ್ತದೆ.
ಸುರಕ್ಷತೆ[ಬದಲಾಯಿಸಿ]
ಯೂರಿಯಾ ಚರ್ಮ, ಕಣ್ಣು ಮತ್ತು ಶ್ವಾಸೇಂದ್ರಿಯ ಪ್ರದೇಶಕ್ಕೆ (ರೆಸ್ಪಿರೆಟರಿ ಟ್ರಾಕ್ಟ್) ಉರಿಯುಂಟು ಮಾಡಬಹುದು. ಗೊಬ್ಬರದ ರೂಪದಲ್ಲಿನ ಯೂರಿಯಾದ ಜೊತೆ ಪದೇಪದೇ ಮತ್ತು ದೀರ್ಘ ಕಾಲದ ಸಂಪರ್ಕದಿಂದಾಗಿ ಚರ್ಮಕ್ಕೆ ಡರ್ಮಾಟೈಸಿಸ್ ಉಂಟಾಗುವ ಸಾಧ್ಯತೆಯಿದೆ.
ರಕ್ತದಲ್ಲಿ ಇದರ ಪ್ರಮಾಣ ಹೆಚ್ಚಾದರೆ, ಹಾನಿಯುಂಟಾಗುತ್ತದೆ. ಮನುಷ್ಯರ ಮೂತ್ರದಲ್ಲಿ (ಯುರೀನ್) ಇರುವ ಯೂರಿಯಾ ಪ್ರಮಾಣದಷ್ಟು ಅಲ್ಪ ಪ್ರಮಾಣದ ಯೂರಿಯಾ ಸೇವಿಸಿದ ಸ್ವಲ್ಪ ಹೊತ್ತಿನಲ್ಲಿಯೇ ನೀರನ್ನು ಜಾಸ್ತಿಯಾಗಿ ಸೇವಿಸಿದರೆ ಯಾವುದೇ ಅಪಾಯ ಸಂಭವಿಸುವುದಿಲ್ಲ. ಬಹುತೇಕ ಪ್ರಾಣಿಗಳು (ಉದಾಹರಣೆಗೆ ನಾಯಿಗಳು), ಹೆಚ್ಚು ಸಾಂದ್ರತೆಯಿರುವ ಮೂತ್ರವನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಇದಲ್ಲದೆ,ಪ್ರಾಣಿಗಳಲ್ಲಿ ಸಾಮಾನ್ಯ ಮನುಷ್ಯನ ಮೂತ್ರದಲ್ಲಿನ ಯೂರಿಯಾಾದ ಪ್ರಮಾಣಕ್ಕಿಂತ ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದ ಯೂರಿಯಾ ಇರುತ್ತದೆ. ಹೀಗಾಗಿ, ಇದು ಜೀವಕ್ಕೆ ಅಪಾಯವಾಗವ ಸಂದರ್ಭಗಳಲ್ಲಿ(ಮರುಭೂಮಿ ಅಂತಹ), ಇದನ್ನು ಸೇವಿಸುವುದು ಅಪಾಯಕಾರವಾಗುತ್ತದೆ.
ಯೂರಿಯಾಾ ಆಲ್ಗಾಲ್ ಬ್ಲೂಮ್ ವಿಷಕಾರಕವಾಗಲು ಕಾರಣವಾಗುತ್ತದೆ. ಆನೇಕ ವರ್ಷಗಳಿಂದ ರಾಸಾಯಿನಕ ಗೊಬ್ಬರ ಬಳಸಲಾಗುತ್ತಿರುವ ಭೂಮಿಯಿಂದ ಹರಿದುಹೋಗುವ ಅಂಶಗಳಿಂದಾಗಿ ವಿಷಕಾರಕ (ಟಾಕ್ಸಿಕ್)ಬ್ಲೂಮ್ಗಳು ಹೆಚ್ಚಾಗುತ್ತವೆ. [೯]
ಈ ವಸ್ತುವು ಕರಗುವ ಬಿಂದುಗಿಂತ ಹೆಚ್ಚಾದ ತಾಪಮಾನದಲ್ಲಿ ಇದು ವಿಷಕಾರಕ ಅನಿಲಗಳನ್ನು ಉತ್ಪತ್ತಿಮಾಡುತ್ತದೆ. ಅಷ್ಟೆ ಅಲ್ಲದೆ, ಇದು ಆಕ್ಸಿಡಾನ್ಟ್, ನೈಟ್ರೈಟ್ಸ್, ಇನ್ಆರ್ಗಾನಿಕ್ ಕ್ಲೋರೈಡ್, ಕ್ಲೋರೈಟ್ಸ್, ಮತ್ತು ಪರ್ಕ್ಲೋರೇಟ್ಗಳೊಂದಿಗೆ ಉಗ್ರವಾಗಿ ಕ್ರಿಯೆಗೆ ಒಳಪಟ್ಟು (ರಿಯಾಕ್ಟ್ ಆಗಿ), ಬೆಂಕಿ ಮತ್ತು ಸ್ಪೋಟನ ಉಂಟಾಗುತ್ತದೆ.[ಸೂಕ್ತ ಉಲ್ಲೇಖನ ಬೇಕು]
ಆಕರಗಳು[ಬದಲಾಯಿಸಿ]
- ↑ Williams, R. (2001-10-24). "pKa Data" (PDF). Archived from the original (PDF) on 2003-08-24. Retrieved 2009-11-27.
- ↑ Nicolaou, Kyriacos Costa (2008). Molecules That Changed The World. Wiley-VCH. p. 11. ISBN 978-3-527-30983-2.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ Sakami W, Harrington H (1963). "Amino acid metabolism". Annual Review of Biochemistry. 32: 355–98. doi:10.1146/annurev.bi.32.070163.002035. PMID 14144484.
- ↑ "ರಿಸರ್ಚರ್ಸ್ ಡೆವಲಪ್ ಯೂರಿಯಾ ಫ್ಯುಯೆಲ್ ಸೆಲ್". Archived from the original on 2017-06-29. Retrieved 2010-06-02.
- ↑ U.S. Court of Appeals for the Ninth Circuit (February 2, 2010). "U.S. v. Ressam" (PDF). Archived from the original (PDF) on ಅಕ್ಟೋಬರ್ 4, 2012. Retrieved February 27, 2010.
- ↑ "Complaint; U.S. v. Ressam" (PDF). NEFA Foundation. December 1999. Archived from the original (PDF) on ಮಾರ್ಚ್ 1, 2012. Retrieved February 26, 2010.
- ↑ ೭.೦ ೭.೧ ಜೋಜೆಫ್ H. ಮೀಸ್ಸೇನ್ ಹಾಗು ಹರ್ರೋ ಪೀಟರ್ಸನ್ “ಯೂರಿಯಾ” ಇನ್ ಉಲ್ಮನ್'ಸ್ ಎನ್ಸೈಕ್ಲೋಪೆಡಿಯ ಆಫ್ ಇಂಡಸ್ಟ್ರಿಯಲ್ ಕೆಮಿಸ್ಟ್ರಿ 2002, ವಿಲೆಯ್-VCH, ವೆಯಿನ್ಹೆಯಿಮ್. doi:10.1002/14356007.a27_333
- ↑ "ಆರ್ಕೈವ್ ನಕಲು". Archived from the original on 2011-04-05. Retrieved 2010-06-02.
- ↑ newscientist.com – US ಸೆಟ್ ಟು ಟ್ರ್ಯಾಕ್ ಟಾಕ್ಸಿಕ್ ಆಲ್ಗಲ್ ಬ್ಲೂಮ್ಸ್
ಹೊರಗಿನ ಕೊಂಡಿಗಳು[ಬದಲಾಯಿಸಿ]
- MSDS ಶೀಟ್ ಆನ್ ಯೂರಿಯಾ Archived 2011-05-15 ವೇಬ್ಯಾಕ್ ಮೆಷಿನ್ ನಲ್ಲಿ.
- ಯೂಸ್ ಆಫ್ ಯುರಿಯ ಇನ್ ಹ್ಯಾಂಡ್ ಡೈಯಿಂಗ್
- CS1 errors: unsupported parameter
- Articles without InChI source
- Articles without EBI source
- Articles without KEGG source
- Articles without UNII source
- Articles with changed CASNo identifier
- Chembox and Drugbox articles with a broken CheMoBot template
- ECHA InfoCard ID from Wikidata
- E number from Wikidata
- Chemical articles with unknown parameter in Chembox
- Articles containing unverified chemical infoboxes
- Articles with unsourced statements from January 2010
- Articles with invalid date parameter in template
- Articles needing additional references from May 2010
- All articles needing additional references
- ವೆಬ್ ಆರ್ಕೈವ್ ಟೆಂಪ್ಲೇಟಿನ ವೇಬ್ಯಾಕ್ ಕೊಂಡಿಗಳು
- ಸಾರಜನಕ ಚಯಾಪಚಯ
- ಯೂರಿಯಾಾಗಳು
- ಕಾರ್ಯಾತ್ಮಕ ಗುಂಪುಗಳು
- ವಿಸರ್ಜನೆ
- ಮಣ್ಣಿನ ಗುಣವರ್ಧಕಗಳು
- ಗೊಬ್ಬರಗಳು
- ರಸಾಯನಶಾಸ್ತ್ರ
- ಕೃಷಿ